Pneumonie communautaire pendant la grossesse
WHEC Bulletin de pratique et de directives cliniques de gestion pour les fournisseurs de soins de santé. Subvention accordée par l'éducation pour la santé des femmes et l'éducation Center (WHEC).
Bien que la morbidité et la mortalité par pneumonie a diminué depuis 1901, la pneumonie dans le monde entier la grossesse reste un problème majeur de santé. Pneumonie dans la population enceintes et non enceintes est une maladie courante, avec une morbidité et une mortalité considérables. Pneumonie classification comprend: pneumonies communautaires (PAC) lors de la santé des individus par ailleurs, liées aux soins de santé pneumonie (HCAP) en développement en établissements de soins ambulatoires, la pneumonie hôpital, la maison-pneumonie soins infirmiers, et associée à la pneumonie sous ventilation (1) . Améliorer la prise en charge des patients adultes atteints de la PAC a fait l'objet de nombreuses organisations différentes, et plusieurs ont élaboré des lignes directrices pour la gestion de la PAC. Deux d'entre les plus couramment utilisés sont ceux de l'Infectious Diseases Society of America (IDSA) et de l'American Thoracic Society (ATS). En réponse à la confusion concernant les différences entre leurs orientations respectives, l'IDSA et l'ATS a convoqué un comité conjoint pour élaborer un document d'orientation unifiée de la PAC. L'enthousiasme pour l'élaboration de ces directives découle, en grande partie, à partir de preuves que les précédentes lignes directrices de la PAC ont conduit à l'amélioration des résultats cliniquement pertinents. Constamment effets bénéfiques sur le plan clinique paramètres pertinents suite à l'introduction d'un protocole global qui a augmenté le respect des lignes directrices publiées. La première recommandation est donc que les lignes directrices de gestion de la PAC être adaptées localement et mis en œuvre. avantages documentés sont les suivants: lignes directrices de la PAC doit répondre à un ensemble complet d'éléments dans le processus de soins plutôt que sur un seul élément dans l'isolement et l'élaboration de lignes directrices de la PAC locales doit être orientée vers l'amélioration des résultats spécifiques et cliniquement pertinente. Comprendre la relation entre le volume de l'hôpital et de mortalité pour des conditions médicales aux Etats-Unis est cruciale pour les cliniciens et les décideurs, car ils subissent des pressions croissantes pour identifier des stratégies pour améliorer la qualité des soins. En outre, parce que trois des raisons les plus courants et coûteux pour une hospitalisation chez les bénéficiaires de Medicare sont une infection aiguë du myocarde, insuffisance cardiaque et la pneumonie, d'identifier les facteurs associés à une meilleure qualité des soins a une grande signification. Pour mieux comprendre la relation entre le volume de l'hôpital et la mortalité des patients, de nombreuses études ont examiné si l'admission dans les hôpitaux à volume élevé est associé à une réduction de la mortalité à 30 jours pour les bénéficiaires de Medicare qui ont été hospitalisés pour infarctus du myocarde, insuffisance cardiaque ou une pneumonie.
Le but de ce document est de se concentrer sur les pneumonies communautaires (PAC) pendant la grossesse. recommandations récentes de l'Infectious Diseases Society of America (IDSA) et de l'American Thoracic Society (ATS) sur la gestion de la PAC adresse des techniques de diagnostic et de gestion pour les pneumonies bactériennes et virales sont abordées. Ces lignes directrices sont examinées dans le cadre de la femme enceinte avec la PAC. Il est largement admis que les femmes enceintes ne tolèrent pas les infections pulmonaires ainsi, et, partant, la pneumonie peut se traduire par une plus grande morbidité et de mortalité. Pour cette raison, la plupart recommander un niveau de surveillance et d'intervention sera pratiquée pour les femmes enceintes.
Fond
Il ya environ 4 millions de cas de la PAC dans les États-Unis chaque année, entraînant environ 1 million d'hospitalisations. la gestion des patients hospitalisés de la pneumonie est plus de 20 fois plus cher que les soins ambulatoires et les coûts d'un montant estimé à 9 milliards par an (1)(2) . Les efforts d'amélioration dans les soins sont garantis, parce que la PAC, avec la grippe, reste la principale cause septième de mort aux États-Unis (2) . Selon une estimation, 915.900 épisodes de la PAC se produire chez les adultes de 65 ans chaque année aux États-Unis. Malgré les progrès de l'antibiothérapie, le taux de mortalité dus à la pneumonie n'ont pas diminué de manière significative depuis la pénicilline est devenue couramment disponibles. La pneumonie est une complication relativement commune dans la grossesse et représente 4,2% des admissions pour antepartum-obstétrique complications non (2) . Heureusement, au cours des 50 dernières années, les taux de mortalité, de la PAC chez les femmes enceintes ont diminué d'environ 20% à moins de 4% par des antimicrobiens appropriés et services de soins intensifs (3) . Aux États-Unis, l'incidence de la PAC avant l'accouchement en moyenne d'environ 1 pour 1.000 grossesses et varie de 0,5 à 1,5 pour 1000 en fonction de la population étudiée (3) . La plupart recommander un niveau de surveillance et d'intervention sera pratiquée pour les femmes enceintes. Acquises dans la communauté résistant à la méthicilline influenza aureus-pneumonie associée S a été signalé pour avoir un taux de létalité de 25% (9) .
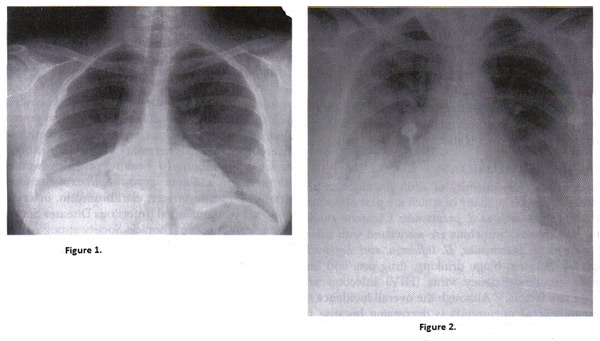
Figure 1. Radiographie du thorax de la pneumonie à pneumocoques droit; Figure 2. Radiographie du thorax de la femme enceinte à la varicelle pneumonie. Note les infiltrats nodulaires et interstitiels similaires à d'autres pneumonies virales.
La plupart des étiologies commune de la pneumonie communautaire (PAC)
Dans la plupart des cas, la PAC se développe lorsque l'accès infectieuses gains agent des voies respiratoires inférieures par inhalation d'aérosols ou de l'aspiration des voies aériennes supérieures microbes. Moins fréquemment, il peut y avoir une dissémination hématogène. Le système de défense de l'hôte, y compris les obstacles anatomiques et mécaniques et innée et l'immunité humorale, est submergé par une combinaison de facteurs tels que la virulence de l'agent pathogène, l'altération de l'défense de l'hôte, et les grandes inoculums bactériens. Les facteurs de comorbidité, comme l'asthme, le tabagisme, la malnutrition, les maladies du foie, maladie pulmonaire obstructive chronique, et d'accroître la grossesse de la susceptibilité aux complications. Une fois l'agent infectieux atteint les voies respiratoires inférieures, des lésions pulmonaires et les résultats directs inflammation interstitielle, conduisant à un shunt intrapulmonaire et d'hypoxie. Le vaste éventail d'organismes qui peuvent causer une pneumonie pendant la grossesse (voir la liste ci-dessous). La plupart d'entre eux sont rencontrés que rarement, mais l'agent étiologique est identifié dans seulement 40-60% de la PAC (4) . Chez les adultes, 60-80% de la PAC est causée par une bactérie, 10-20% est atypique, et 10-15% est virale. La commune unique agent pathogène le plus est le Streptococcus pneumoniae, qui est responsable de 30-50% des cas identifiés. Il est suivi par Haemophilus influenza et Mycoplasma pneumoniae.
| Patient Type | Etiologie |
|---|---|
| Type Type | Streptococcus pneumoniae Mycoplasma pneumoniae Haemophilus influenzae Chlamydophila pneumoniae virus respiratoires (grippe A et B, adénovirus, virus respiratoire syncytial, virus parainfluenza et). |
| En milieu hospitalier (non-USI) | S. pneumoniae M. pneumoniae C. pneumoniae H. influenzae espèces de Legionella Aspiration virus respiratoires (Influenza A et B, adénovirus, virus respiratoire syncytial, virus parainfluenza et) |
| Unité d'hospitalisation de soins intensifs (USI) | S. pneumoniae Staphylococcus aureus espèces de Legionella bacilles à Gram négatif H. influenzae |
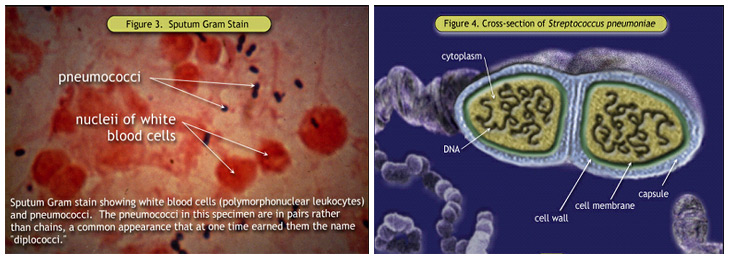
Figure 3. Coloration de Gram des crachats; Figure 4. Coupe de Streptococcus pneumoniae
certaine adaptation de la fonction immunitaire pendant la grossesse peuvent également jouer un rôle dans la susceptibilité à la pneumonie et de son évolution clinique. T cytotoxiques des cellules sont supprimées, et le type T-helper 2 cellules prédominent sur le type T-helper cellules 1 par un ratio de 4:1, ce qui entraîne une diminution de la sécrétion de l'interleukine-2, l'interféron γ-et facteur de nécrose tumorale- β. l'activité des cellules tueuses naturelles est également diminué (5) . Bien que la suppression de certaines fonctions immunitaires humorale et à médiation cellulaire est pensé pour permettre un logement ou la tolérance de la greffe du fœtus, une susceptibilité accrue aux infections éventuellement certains est clairement indésirable.
Critères de pneumonie grave acquise dans la communauté (PAC)
Plusieurs critères ont été proposés pour définir graves de la PAC. La plupart des séries de cas ont défini simplement comme la PAC qui nécessite unité de soins intensifs (USI). Des critères objectifs pour identifier les patients à l'admission aux soins intensifs notamment de la définition initiale des ATS sévère de la PAC, et ses modifications ultérieures, le trottoir (la confusion, l'urémie, la fréquence respiratoire, tension artérielle) des critères, et de la pneumonie Severity Index (PSI) classe de gravité V (ou IV et V) (6) . Le PSI est basée sur des données qui sont généralement disponibles à la présentation et la stratification des patients en cinq classes de risque dans laquelle les taux de mortalité de 30 jours allant de 0,1% à 27,0%. Plus le score est élevé, plus le risque de décès, l'admission aux soins intensifs, et la réadmission et plus la durée du séjour. Un algorithme qui utilise le PSI pour juger de la pertinence de l'admission est utile dans la gestion des patients. Les patients en classes de risque I, II et III sont à faible risque de la mort et la plupart peuvent être traités en ambulatoire en toute sécurité en l'absence de circonstances atténuantes.
* critères mineurs: fréquence respiratoire **> 30 respirations / min; ratio PaO2/FIO2 ** <250; infiltrats multilobaire; confusion / désorientation; urémie (niveau BUN,> 20 mg / dL); leucopénie *** (numération des globules blancs, <4000 cellules/mm3), thrombocytopénie (numération plaquettaire, <100.000 cellules / mm 3); l'hypothermie (température centrale <36 ° C); hypotension nécessitant une réanimation liquidienne agressive.
Les critères majeurs: la ventilation mécanique invasive; choc septique avec la nécessité de vasopresseurs
NOTE: BUN, urée sanguine; PaO2/FIO2, la pression artérielle en oxygène / fraction d'oxygène inspiré; WBC, des globules blancs.
* D'autres critères à considérer sont l'hypoglycémie (chez les patients non diabétiques), l'alcoolisme aigu / sevrage alcoolique, hyponatrémie, acidose métabolique inexpliquée ou d'une élévation des lactates, la cirrhose et asplénie.
** La nécessité d'une ventilation non invasive peut se substituer à une fréquence respiratoire 130 respirations / min ou un PaO2/FIO2 ratio <250.
*** En raison de l'infection seule.
Évaluation de la pneumonie communautaire (PAC)
L'évaluation de la PAC est initié à partir des symptômes du patient. Les symptômes de la pneumonie bactérienne pendant la grossesse sont les mêmes que chez les personnes non enceintes. Légère supérieure plaintes respiratoires précèdent les symptômes comprennent la toux dans plus de 90%, la production d'expectorations de 66%, la dyspnée chez 66%, et douleur thoracique dans 50% (7) . Des symptômes non respiratoires, y compris des maux de tête, fatigue, myalgies, des sueurs et des nausées. Virales et fongiques pneumonies peuvent présenter de la même fonction sur les causes spécifiques. L'examen physique doit inclure la détermination vitale signe d'évaluer la fièvre et le statut du volume intravasculaire. Une fréquence respiratoire, cyanose, l'utilisation des muscles accessoires, le torchage du nez, et les rétractations Sterna sont autant de marqueurs de détresse respiratoire. examen thoracique peut révéler des preuves de la consolidation de matité à la percussion, de E à A changements, et le souffle bronchique sons compatibles avec une pneumonie bactérienne. Les femmes avec des infections virales ou à mycoplasme ont souvent un examen normal. L'examen physique à elle seule une très faible sensibilité et spécificité pour le diagnostic de pneumonie, mais, utilisé en conjonction avec l'histoire radiographie du thorax, et le diagnostic de laboratoire, il reste une des pierres angulaires du diagnostic.
En plus d'une constellation de signes cliniques évocateurs, un infiltrat démontrable par radiographie pulmonaire ou autre technique d'imagerie, avec ou sans l'appui des données microbiologiques, est nécessaire pour le diagnostic de pneumonie. Une radiographie du thorax est nécessaire pour l'évaluation de routine des patients qui sont susceptibles d'avoir une pneumonie, pour établir le diagnostic et d'aide à différencier de la PAC à partir d'autres causes fréquentes de toux et de fièvre, telles que la bronchite aiguë. Les radiographies pulmonaires sont parfois utiles pour suggérer l'agent étiologique, le pronostic, d'autres diagnostics, et les conditions associées. Rarement, la radiographie thoracique d'admission est clair, mais l'aspect toxique du patient suggère que plus de la bronchite. tomodensitométrie peut être plus sensible, mais la signification clinique de ces résultats, lorsque des résultats de la radiographie sont négatifs n'est pas claire. Pour les patients qui sont hospitalisés pour une pneumonie suspectée mais qui ont des effets négatifs conclusions radiographie du thorax, il peut être raisonnable de traiter leur condition présumée avec des antibiotiques et répéter l'imagerie dans 24 - 48 heures. Les études microbiologiques peuvent appuyer le diagnostic de la pneumonie due à un agent infectieux, mais les tests de routine sont souvent faussement négatif et sont souvent non spécifiques. Une histoire de Voyage récent ou endémiques d'exposition, si toujours cherché, peut identifier des étiologies spécifiques potentiels qui seraient autrement inattendus comme une cause de la PAC.
Recommandé tests de diagnostic pour Etiologie: Les patients atteints de la PAC doit être étudiée pour des pathogènes qui modifierait sensiblement standard (empirique) les décisions de gestion, lorsque la présence de des agents pathogènes tels est suspectée sur la base de résultats cliniques et des indices épidémiologiques. La nécessité pour les tests de diagnostic pour déterminer l'étiologie de la PAC ne peut être justifiée sous plusieurs angles. La principale raison de ces tests est de savoir si les résultats vont changer la gestion des antibiotiques pour un patient individuel. Le spectre de l'antibiothérapie peut être élargi, réduit ou totalement modifié sur la base des tests de diagnostic. L'altération de la thérapie, qui est potentiellement le plus bénéfique pour l'individu est une escalade ou de passer de l'empirique régime habituel à cause d'agents pathogènes inhabituels (par exemple, les champignons endémiques ou Mycobacterium tuberculosis) ou des problèmes de résistance aux antibiotiques. Large couverture empirique, telle que préconisée dans ces lignes directrices, ne fournirait pas le traitement optimal pour certaines infections, comme la psittacose ou de la tularémie. Augmentation de la mortalité (8) et un risque accru d'échec clinique sont plus fréquentes avec une antibiothérapie appropriée. Gestion de l'échec initial d'antibiotiques est grandement facilitée par un diagnostic étiologique à l'admission. tests d'antigène urinaire (UAT) sont disponibles commercialement et ont été approuvés par la Food and Drug Administration américaine (FDA) pour la détection de S. pneumoniae et L. pneumophila sérogroupe 1 (9) . tests UAT semble avoir un rendement plus élevé de diagnostic chez les patients présentant une maladie plus grave.
Les indications cliniques de diagnostic tests plus poussés (9) :
| Indication | Hémoculture | Culture des expectorations | Legionella UAT | Pneumocoque UAT | Autres |
|---|---|---|---|---|---|
| Admission aux soins intensifs | X | X | X | X | X a |
| Le défaut de consultation externe antibiothérapie | X | X | X | ||
| Cavitaire infiltrats | X | X | X b | ||
| Leucopénie | X | X | |||
| l'abus d'alcool Active | X | X | X | X | |
| Les maladies chroniques graves du foie | X | X | |||
| Obstructive sévère ou de maladie du poumon de structure | X | ||||
| Asplénie (anatomique ou fonctionnelle) | X | X | |||
| Voyage récent (dans les 2 dernières semaines) | X | X c | |||
| Legionella positive UAT résultat | X d | NA | |||
| Résultat positif UAT pneumocoque | X | X | NA | ||
| épanchement pleural | X | X | X | X | X e |
NA, ne s'applique pas; UAT, épreuve à l'antigène urinaire.
- Endotrachéale aspirer si intubé, éventuellement bronchoscopie ou nonbronchoscopic lavage broncho-alvéolaire.
- Fongiques et les cultures de la tuberculose.
- Consultez les lignes directrices par l'OMS et du CDC pour plus de détails. ( http://www.cdc.gov et http://www.who.int)
- Les supports spéciaux pour Legionella.
- Thoracentèse et pleural cultures fluide.
Stratification du risque et la décision d'hospitaliser
Environ 30% à 50% des patients qui sont hospitalisés atteints de pneumonie ont un risque faible des cas, dont beaucoup pourraient être gérés à la maison (7) . Notre politique générale est d'hospitaliser les femmes enceintes souffrant de pneumonie pendant au moins une observation de 23 heures. L'évaluation comprend une radiographie pulmonaire, numération formule sanguine complète, les électrolytes, l'évaluation de l'oxygénation, et des cultures de sang si sepsis clinique est suspectée. Pour tous les patients, les hémocultures sont positives dans seulement 5-15%; hémocultures positives sont plus fréquentes chez ceux qui ont de graves PAC (9) . La coloration de Gram des crachats peut être utile de choisir une couverture antibiotique initial, mais il a généralement un faible rendement (10) . Au cours de la saison grippale, les tests sérologiques rapide de la grippe A et B est raisonnable. cultures d'expectorations, les tests sérologiques, l'identification des agglutinines froides, test de l'antigène bactérien, et la réaction en chaîne par polymérase sont effectuées uniquement lorsque cela est cliniquement indiqué.
Unité de soins intensifs (USI) La décision d'admission
L'admission directe à une unité de soins intensifs est nécessaire pour les patients en choc septique nécessitant vasopresseurs ou présentant une insuffisance respiratoire aiguë nécessitant intubation et ventilation mécanique. L'admission directe à une unité de soins intensifs ou unité de suivi de haut niveau est recommandée pour les patients avec 3 des critères sévères pour les mineurs de la PAC énumérés ci-dessus. La décision d'admission de deuxième niveau est de savoir si à la place du patient aux soins intensifs ou une unité de suivi de haut niveau plutôt que sur un plancher de médecine générale. Environ 10% des patients hospitalisés pour une PAC doivent être admis aux soins intensifs, mais les indications varient fortement en fonction des patients, des médecins, des hôpitaux, et les différents systèmes de soins de santé. Certains de la variabilité des résultats entre les institutions de la disponibilité de haut niveau de contrôle ou unités de soins intermédiaires appropriés pour les patients à risque accru de complications. Parce que l'insuffisance respiratoire est la principale raison de retard de transfert aux soins intensifs, les unités simples de surveillance cardiaque ne répondrait pas aux critères d'une unité de suivi de haut niveau pour les patients souffrant de graves PAC. L'un des importants facteurs déterminants les plus de la nécessité pour les soins de réanimation est la présence de comorbidités chroniques (11) . Cependant, environ un tiers des patients souffrant de graves PAC étaient auparavant en bonne santé.
La raison d'être particulièrement graves définition de la PAC est de 4 volets:
- placement approprié des patients permet d'optimiser l'utilisation des ressources limitées aux soins intensifs.
- Transfert à l'unité de soins intensifs pour insuffisance respiratoire retardée ou retarder l'apparition du choc septique est associée à une augmentation de la mortalité (9) . Bien que les admissions aux soins intensifs à faible acuité se produisent, la préoccupation majeure est de l'admission initiale à l'unité de médecine générale, avec transfert ultérieur à l'USI. Autant que 45% des patients atteints de la PAC qui, finalement, besoin d'être admis aux soins intensifs ont d'abord été admis dans un établissement non-USI. De nombreux transferts de retard à l'unité de soins intensifs représentent la pneumonie rapidement évolutive qui n'est pas évident à l'admission. Toutefois, certains ont des résultats subtile, y compris ceux inclus dans les critères mineurs (voir ci-dessus), qui pourrait justifier une admission directe à l'USI.
- La répartition des étiologies microbiennes diffère de celle de la PAC en général (10) , avec des implications importantes pour les tests diagnostiques et empiriques choix antibiotique. Prévention de la thérapie antibiotique approprié a également été associée à une mortalité plus faible.
- Les patients atteints de PAC approprié pour le traitement immunomodulateur doit être identifié (11) . La réponse inflammatoire systémique / critères sepsis sévère généralement utilisé pour les essais sepsis génériques ne peuvent être appropriées lorsqu'elles sont appliquées spécifiquement à sévère de la PAC. Par exemple, les patients atteints de pneumonie lobaire unilatérale risque d'avoir une hypoxémie sévère suffisante pour répondre à des critères de lésion pulmonaire aiguë, mais pas une réponse systémique.
Traitement antibiotique
Traitement antimicrobien empirique: Empirique des recommandations aux antibiotiques n'ont pas changé de manière significative de ceux dans les précédentes orientations. L'augmentation de la preuve a renforcé la recommandation pour la combinaison de traitement empirique de sévères de la PAC. Seulement 1 a récemment publié aux antibiotiques a été ajouté aux recommandations: ertapénème, comme un b-lactamines alternative acceptable pour les patients hospitalisés présentant des facteurs de risque d'infection par des agents pathogènes gram-négatives autres que Pseudomonas aeruginosa (12) . À l'heure actuelle, le comité attend encore évaluation de l'innocuité de la télithromycine par la US Food and Drug Administration (FDA) avant de faire sa recommandation finale au sujet de cette drogue. Les recommandations sont généralement pour une classe d'antibiotiques plutôt que pour un médicament spécifique, à moins que les données de résultat clairement favorable à un médicament. Parce que l'efficacité globale reste bonne pour de nombreuses classes d'agents, les drogues les plus puissantes sont donné la préférence à cause de leur bénéfice dans la réduction du risque de sélection pour la résistance aux antibiotiques.
Traitement ambulatoire
- Auparavant en bonne santé et sans facteurs de risque contre les souches résistantes de S. pneumoniae (DRSP) infection:
- A la famille des macrolides (azithromycine, clarithromycine, l'érythromycine ou) (forte recommandation, preuves de niveau I)
- Doxycycline (recommandation faibles, le niveau de preuve III)
- Présence de comorbidités, comme les chroniques du cœur, du poumon, du foie ou une maladie rénale, diabète sucré, l'alcoolisme; tumeurs malignes; asplénie; conditions immunosuppresseurs ou l'utilisation de médicaments immunosuppresseurs; utilisation d'antimicrobiens au cours des 3 derniers mois (dans ce cas, une solution de rechange à partir d'un classe différente doit être sélectionné), ou d'autres risques d'infection DRSP:
- Une fluoroquinolone respiratoire (moxifloxacine, gémifloxacine, ou [lévofloxacine 750 mg]) (forte recommandation, preuves de niveau I)
- Un b-lactamines, plus un macrolide (fortement recommandé; preuves de niveau I) (-dose d'amoxicilline haut [par exemple, 1 g 3 fois] tous les jours ou amoxicilline-acide clavulanique [2 g 2 fois] tous les jours est préféré; options incluent la ceftriaxone, cefpodoxime, et céfuroxime [500 mg 2 fois] tous les jours; doxycycline niveau de preuves [II] est une alternative à la famille des macrolides)
- Dans les régions avec un taux élevé (> 25%) d'infection par le haut niveau (CMI,> 16 mg / mL) résistantes aux macrolides de S. pneumoniae, envisager l'utilisation d'agents de remplacement, y compris ceux sans comorbidités. (Recommandation modéré; niveau de preuve III)
le traitement des patients hospitalisés, non-USI
- Une fluoroquinolone respiratoire (forte recommandation, preuves de niveau I).
- Un b-lactamines, plus un macrolide (fortement recommandé; preuves de niveau I) (b-lactamines agents préférés comprennent céfotaxime, ceftriaxone, et à l'ampicilline, l'ertapénème chez des patients sélectionnés, avec [doxycycline niveau] des preuves III comme une alternative à la famille des macrolides. Une des voies respiratoires fluoroquinolone doit être utilisé pour les patients allergiques à la pénicilline.) Augmenter les taux de résistance ont suggéré que le traitement empirique avec un macrolide seul peut être utilisé uniquement pour le traitement des patients soigneusement sélectionnés hospitalisée pour une affection sans gravité et sans facteurs de risque d'infection par pharmacorésistante pathogènes. Cependant, la monothérapie ne peut être recommandé de façon systématique (12) .
En milieu hospitalier, le traitement aux soins intensifs
- Un b-lactamines (céfotaxime, ceftriaxone, ou à l'ampicilline-sulbactam) plus, soit azithromycine (niveau de preuve II) ou une fluoroquinolone (preuves de niveau I) (forte recommandation) (Pour les allergiques à la pénicilline patients, une fluoroquinolone respiratoire et l'aztréonam sont recommandés).
- Pour l'infection à Pseudomonas, utilisez un antipneumococcique, antipseudomonal b-lactamines (pipéracilline-tazobactam, céfépime, imipénème ou méropénème) et la ciprofloxacine ou lévofloxacine (-mg dose de 750) (14) .
Ou
Le b-lactamines ci-dessus plus un aminoside et l'azithromycine.
Ou
Le b-lactamines ci-dessus plus un aminoside et une fluoroquinolone antipneumococcique (pour les patients allergiques à la pénicilline, l'aztréonam substituer aux b-lactamines ci-dessus). (Recommandation modéré; niveau de preuve III). - Pour acquises dans la communauté résistant à la méthicilline infection à Staphylococcus aureus, ajouter la vancomycine ou le linézolide. (Recommandation modéré; niveau de preuve III).
Note de l'éditeur: tétracycline (doxycycline, minocycline) et aminoglycosides (gentamicine, tobramycine, amikacine) doit être évitée pendant la grossesse.
Temps à la dose de premier antibiotique
- Pour les patients admis aux urgences (ED), la première dose d'antibiotiques doivent être administrés tout à l'urgence. (Recommandation modéré; niveau de preuve III). Plutôt que de désigner une fenêtre spécifique dans lequel d'initier le traitement, la commission estime que les patients hospitalisés pour une PAC devrait recevoir la première dose d'antibiotiques dans l'ED.
Changer de voie intraveineuse à la thérapie orale
- Les patients doivent être sous tension de la voie intraveineuse à la thérapie orale quand ils sont hémodynamique stable et une amélioration clinique, sont capables d'ingérer des médicaments, et ont un fonctionnement normalement tractus gastro-intestinal. (Forte recommandation, niveau de preuve II) (15) .
- Les patients doivent être rejetées dès qu'ils sont cliniquement stables, n'ont pas d'autres problèmes médicaux actifs, et avoir un environnement sécuritaire pour les soins continus. d'observation en milieu hospitalier tout en bénéficiant d'une thérapie par voie orale n'est pas nécessaire. (Recommandation modéré; niveau de preuve II).
Durée de l'antibiothérapie
- Les patients atteints de la PAC doivent être traités pendant un minimum de 5 jours (preuves de niveau I), devraient être afébriles pendant 48 - 72 heures, et devrait faire signer au plus 1 CAP-associé de l'instabilité clinique avant l'arrêt du traitement (niveau de preuve II). (Recommandation modéré) (16) .
- Une plus longue durée du traitement peut être nécessaire si le traitement initial n'a pas été actif contre le pathogène identifié ou si elle a été compliquée par une infection extrapulmonaire, comme la méningite ou une endocardite. (Recommandation faible, le niveau de preuve III).
Épidémiologie de la non-réponse pneumonie
Le terme «pneumonie non-réponse" est utilisé pour définir une situation dans laquelle une réponse clinique inadéquate est présent malgré le traitement antibiotique. L'absence d'une claire définition et validées dans la littérature fait de non-réponse difficile à étudier. L'absence de réponse varie également selon le site de traitement. L'absence de réponse des patients non hospitalisés est très différente de celle chez les patients admis aux soins intensifs. Le moment de l'évaluation est également importante. La fièvre persistante après le premier jour du traitement diffère sensiblement de la fièvre persistante (ou récurrents) au jour 7 de traitement. Deux modes de réponse inacceptables sont observés chez les patients hospitalisés (17) . Le premier est la pneumonie progressive ou réelle aggravation clinique, une insuffisance respiratoire aiguë nécessitant une assistance respiratoire et / ou de choc septique, survenant habituellement dans les 72 premières heures d'hospitalisation. Comme il est indiqué ci-dessus, autant que 45% des patients atteints de la PAC qui, finalement, besoin d'être admis aux soins intensifs sont d'abord admis dans un établissement non-USI et sont transférés en raison de la détérioration. La détérioration et le développement d'une insuffisance respiratoire ou hypotension 172 heures après le traitement initial est souvent liée à des complications inter-courant, la détérioration de la maladie sous-jacente, ou le développement de surinfection nosocomiale. Le deuxième modèle est celui de la persistance ou non de répondre pneumonie. La non-réponse peut être définie comme l'absence ou retard dans la réalisation de la stabilité clinique. Lorsque ces critères ont été utilisés, le temps médian pour atteindre la stabilité clinique a été de 3 jours pour tous les patients, mais un quart des patients ont plus de 6 jours pour répondre à tous ces critères de stabilité. définitions strictes pour chacun des critères et des scores plus élevés PSI ont été associés à des délais plus longs pour atteindre la stabilité clinique.
En raison des limites des tests de diagnostic, la majorité de la PAC est encore traitée de façon empirique. Critique à la thérapie empirique est une compréhension de la gestion des patients qui ne suivent pas le modèle de réponse normale. Bien que difficile à définir, la non-réponse n'est pas rare. Dans l'ensemble, 6% - 15% des patients hospitalisés avec de la PAC ne répondent pas à l'antibiotique le traitement initial (17) . L'incidence de l'échec du traitement chez les patients atteints de la PAC qui ne sont pas hospitalisés n'est pas bien connue, parce que les études basées sur la population sont nécessaires. Almirall et al. (18) décrit un taux global d'hospitalisation de 60% dans une étude basée sur la population, mais le taux d'échec parmi les 30% de patients qui avaient initialement présenté à leur médecin de soins primaires n'ont pas été fournis. La fréquence de l'antibiothérapie préalable chez les patients Medicare admis à l'hôpital avec de la PAC est de 24% - 40%, mais le pourcentage qui ont reçu une antibiothérapie préalable pour l'épisode aigu de la pneumonie se versus d'autres indications n'est pas claire. Pour les patients initialement admis aux soins intensifs, le risque d'absence de réponse est déjà élevé; autant que 40% se détériorera, même après la stabilisation initiale en réanimation. Mortalité chez les patients non-réponse est augmenté de plusieurs fois par rapport à celle des patients ayant répondu (18) . Les taux de mortalité globale plus élevé que 49% ont été signalés pour toute une population de non-réponse des patients hospitalisés avec de la PAC, et le taux de mortalité rapportés dans une étude de l'échec au début était de 27% (9) .
Compte tenu de ces résultats, les craintes concernant la non-réponse doivent être tempérés avant 72 heures de traitement. changements aux antibiotiques au cours de cette période devrait être envisagée que pour les patients atteints de détérioration ou dans lesquels les données nouvelle culture ou des indices épidémiologiques suggèrent autres étiologies. Enfin, la non-résolution ou à faible résolution de la pneumonie a été utilisé pour faire référence aux conditions de patients qui présentent une persistance des infiltrats pulmonaires 130 jours après un syndrome ressemblant à la pneumonie initial (18) . Jusqu'à 20% de ces patients peut être condamné pour des maladies autres que la PAC lorsque soigneusement évaluée.
Gestion des non-répondants pneumonie
La non-réponse aux antibiotiques dans la PAC entraînera généralement> 1 de 3 réponses cliniques: 1) le transfert du patient à un niveau supérieur de soins, 2) d'autres tests diagnostiques, et 3) l'escalade ou changement de traitement. Les questions relatives à l'hospitalisation et le transfert aux soins intensifs sont discutés ci-dessus. Une réponse de l'hôte insuffisante, plutôt que l'antibiothérapie inappropriée ou micro-organismes inattendue, est la cause la plus fréquente de l'échec apparent des antibiotiques lorsque directrice recommandé la thérapie est utilisée. Les décisions relatives à d'autres tests de diagnostic et des changements aux antibiotiques / escalade sont intimement liés et doivent être discutées en tandem. En plus des procédures de diagnostic microbiologique, plusieurs autres tests semblent être utiles pour certains patients atteints de la non-réponse:
- Poitrine tomodensitométrie (TDM). En plus de pouvoir à une embolie pulmonaire, un scanner peut révéler d'autres raisons de l'échec des antibiotiques, y compris épanchement pleural, abcès du poumon, ou obstruction des voies aériennes centrales. Le schéma des opacités peuvent également suggérer d'autres maladies non infectieuses, comme la bronchiolite oblitérante organiser une pneumonie.
- Thoracentèse. Empyème et effusions parapneumonic sont des causes importantes de non-réponse (19) , et thoracentèse doit être effectuée lorsque significative liquide pleural est présent.
- La bronchoscopie avec lavage alvéolaire bronchique (BAL) et des biopsies transbronchiques. Si le différentiel de non-réponse comprend la pneumonie non infectieuses imite, bronchoscopie fournira des informations plus diagnostic de routine des cultures microbiologiques. BAL peut révéler des entités non infectieuses, telles que l'hémorragie pulmonaire aiguë ou la pneumonie à éosinophiles, ou des conseils des maladies infectieuses, telles que lymphocytaire plutôt que alvéolite neutrophile pointant vers virus ou une infection Chlamydophila. biopsies transbronchiques peut également donner un diagnostic précis.
L'antibiothérapie de non-réponse dans la PAC n'a pas été étudié. L'écrasante majorité des cas de situation de non-réponse sont dues à la gravité de la maladie à la présentation ou un retard dans la réponse au traitement liés à des facteurs d'accueil. Autres que l'utilisation de la thérapie de combinaison pour une pneumopathie à pneumocoque (20) , il n'existe aucune documentation que les antibiotiques supplémentaires pour entraîner une détérioration trop rapide pour un meilleur résultat. La présence de facteurs de risque pour les micro-organismes potentiellement non traitées peuvent justifier l'élargissement temporaire empirique de l'antibiothérapie jusqu'à ce que les résultats des tests de diagnostic sont disponibles.
Prévention de la pneumonie
Schémas prophylactiques spécifiques aux antimicrobiens sont disponibles que pour quelques-uns des grand nombre d'agents pathogènes qui peuvent causer la pneumonie, en est un exemple pour la prophylaxie Pneumocystis jirovecii (anciennement carinii) pneumonie (PCP) chez les femmes atteintes liées à l'infection à VIH. Le vaccin antipneumococcique, un vaccin polysaccharidique 23-valent conjugué, est recommandé pour les femmes enceintes qui sont immunodéprimés, sont des fumeurs, d'alcoolisme, de diabète ou cardiaque, pulmonaire, ou d'une maladie rénale, ou qui sont splénectomisés (par exemple, les femmes avec la drépanocytose la maladie). Le vaccin a été démontré à 60-70% d'efficacité, mais il est nettement sous-utilisés. Ce vaccin est nécessaire qu'une seule fois dans la vie d'une femme. La prévention primaire, y compris le lavage des mains et de limiter le contact de personnes malades, offre une certaine protection, mais aucune mesure de prévention est efficace.
Toutes les personnes> 50 ans d'âge, d'autres à risque de complications de la grippe, les contacts familiaux des personnes à risque élevé, et les travailleurs des soins de santé devraient recevoir le vaccin grippal inactivé tel que recommandé par le Comité consultatif en matière d'immunisation (ACIP), les centres de lutte contre la maladie et Prevention (CDC). (Forte recommandation, preuves de niveau I). Les vaccins ciblant les maladies à pneumocoques et la grippe demeure la pierre angulaire pour la prévention de la PAC. vaccin polysaccharidique contre le pneumocoque et le vaccin grippal inactivé sont recommandés pour tous les adultes plus âgés et pour les jeunes personnes atteintes de troubles médicaux qui les placent à risque élevé de morbidité et de mortalité la pneumonie (21) . Le nouveau vaccin contre la grippe atténué vivant est recommandé pour les personnes en bonne santé 5 - 49 ans d'âge, y compris les travailleurs de la santé (21) . permis d'études épidémiologiques-Post ont documenté l'efficacité des vaccins polysaccharidiques contre le pneumocoque pour la prévention de l'infection invasive (bactériémie et la méningite) chez les personnes âgées et les jeunes adultes de certaines maladies chroniques (22) . L'efficacité globale contre les maladies invasives à pneumocoques chez les personnes de 65 ans est de 44% - 75% (22) , bien que l'efficacité peut diminuer avec l'âge. L'efficacité du vaccin contre le pneumocoque chez les personnes immunodéprimées est moins claire, et les résultats des études évaluant l'efficacité contre la pneumonie sans bactériémie ont été mitigés. Le vaccin a été montré pour être rentable pour la population générale des adultes de 50 - 64 ans de l'âge et> 65 ans (21) (22) . Une deuxième dose du vaccin polysaccharidique contre le pneumocoque après un intervalle de plus de 5 ans a été montré pour être sûr, avec seulement un peu plus de réactions locales que sont observés après la première dose. Parce que la sécurité d'une troisième dose n'a pas été démontrée, les directives actuelles ne suggèrent pas répétées revaccination. Le vaccin conjugué contre le pneumocoque est sous enquête pour utilisation chez les adultes mais n'est actuellement autorisé pour utilisation chez les jeunes enfants (23) . Cependant, son utilisation chez les enfants de <5 ans a considérablement réduit les bactériémies à pneumocoque invasive chez les adultes et (23) .
La pneumonie virale
La plupart des cas de pneumonie virale pendant la grossesse sont causés par des virus de la grippe, et ceux-ci sont particulièrement fréquentes pendant la saison grippale, qui aux Etats-Unis est de Décembre à Mars. La présentation clinique n'est pas modifié par la grossesse, avec une période d'inoculation de 1 à 4 jours après l'exposition. Les patients sont généralement infectieuse le jour avant l'apparition des symptômes et pendant 5 jours par la suite. La pneumonie, primaires ou superposées bactérienne virale, est la complication la plus commune, et il se développe dans environ 12% des femmes enceintes à la grippe (9) . La grippe non compliquée chez la femme enceinte est traitée avec des antipyrétiques et des soins de soutien. profils de résistance aux antiviraux, ces dernières années ont fluctué en fonction du type de la grippe. Actuellement, un traitement antiviral est recommandé pour une utilisation chez les femmes enceintes à la grippe. Thérapie raccourcit l'évolution de la maladie par une moyenne de 1 jour et peut réduire le risque de pneumonie. L'amantadine (amantadine et rimantadine) et inhibiteurs de la neuraminidase (oseltamivir et zanamivir) sont les médicaments actuellement disponibles pour utilisation pendant la grossesse. pneumonie grippale primaire ne répond pas très bien être un traitement antiviral, et la mortalité reste élevée. Heureusement, la grippe sévère primaire est rare. Superposé une pneumonie bactérienne doit être traitée avec le régime approprié.
-Zoster Virus de la varicelle est le virus à ADN qui cause la varicelle a été rapporté avoir eu une prévalence de 0,5-0,7 pour 1.000 grossesses avant la vaccination généralisée a commencé (24) . A et la vie en danger de complication grave est la pneumopathie varicelleuse, qui se développe dans 10% des femmes enceintes (24). Il s'agit d'une complication grave chez les femmes enceintes - les taux de mortalité d'environ 15%, même à l'ère de la thérapie antivirale. Pourtant, ce n'est nettement diminué par rapport au taux de mortalité de 35-40% avant la disponibilité des agents antiviraux. Gestion de la pneumopathie varicelleuse comprend le traitement à l'acyclovir par voie intraveineuse, 10 mg / kg toutes les 5 heures (4) . En plus de la transmission périnatale, l'infection intra-utérine a été documentée dans varicelle-zona les femmes infectées par le virus, avec ou sans pneumonie. Si l'immunoglobuline varicelle-zona est donnée dans les 96 heures suivant l'exposition à la varicelle, il peut atténuer ou prévenir l'infection chez les femmes enceintes vulnérables. Aux Etats-Unis, les CDC recommandent l'utilisation d'une immunoglobuline varicelle-zona immunitaire (VariZIG) produites au Canada et disponibles en vertu d'un protocole d'accès élargi. Les vaccins vivants atténués contre la varicelle sont contre-indiqués pendant la grossesse.
La pneumonie fongique et parasitaire
Fongiques et parasitaires sont les pneumonies et les infections opportunistes sont généralement de plus grande conséquence chez les sujets immunodéprimés, en particulier chez les femmes infectées par le VIH. Blatomycose et l'histoplasmose sont les pneumonies fongiques les plus courantes compliquant la grossesse et sont généralement auto-limitée. Coccidioïdomycose se produit dans les zones endémiques et peut causer une pneumonie. La plupart des pneumonies fongiques présentes similaire à la pneumonie virale et bactérienne. Les femmes enceintes présentant des complications des infections fongiques, y compris une maladie disséminée, sont traités avec le kétoconazole et de l'amphotéricine B, bien que les données de sécurité pour l'utilisation à long terme de la grossesse sont limitées (25) . Avec le nombre croissant de femmes enceintes infectées par le VIH, la pneumonie à Pneumocystis carinii (PCP) est la principale cause du syndrome d'immunodéficience acquise (sida)-connexes décès chez les femmes enceintes aux États-Unis (26) . Le taux de mortalité de ceux avec du PCP est à l'avenant à environ 50%. Le traitement est au triméthoprime-sulfaméthoxazole ou la pentamidine. Les patients avec le VIH + des lymphocytes T CD4 inférieur à 200/uL, une histoire de la candidose oropharyngée, ou d'une maladie liée sida devraient recevoir une prophylaxie (26) . Le schéma prophylactique recommandé est le triméthoprime-sulfaméthoxazole, un comprimé à double concentration par jour. La prophylaxie est de 90-95% efficace pour prévenir la PCP.
Complications de la grossesse et de la pneumonie
La pneumonie est associée à une large gamme de complications chez l'individu non enceintes, y compris la méningite, l'arthrite, l'emphysème, l'endocardite, septicémie, insuffisance cardiaque, syndrome de détresse respiratoire aiguë sévère (SRAS), et une insuffisance rénale. Elles se produisent en nombre similaire de la femme enceinte. En outre, la PAC peut entraîner un certain nombre de complications liées à la grossesse. Le plus grand risque de travail prématuré et de livraison. Le travail prématuré taux aussi élevés que 44% ont été rapportés chez les femmes atteintes de la PAC, et l'accouchement prématuré se produit dans près d'un tiers des femmes (27) . Certains éléments de preuve indiquent que la prématurité est plus fréquente quand la femme souffrant de pneumonie a un facteur de comorbidité. Récemment, la rupture prématurée et durée de membranes a été démontré que chez les femmes a augmenté et bactériennes pneumonie virale (28) . poids à la naissance du nouveau-né nés de femmes de la PAC seraient sensiblement inférieurs à la moyenne, et il existe un risque presque deux fois plus élevé pour la restriction de croissance fœtale (risque relatif 1,86, IC 95% 1.01 à 3.45) (28)(29). Bien que l'hémoglobine fœtale a été une affinité accrue pour l'oxygène, ce qui favorise l'oxygène transplacentaire du fœtus, marquée hypoxémie maternelle peut conduire à la souffrance foetale. Afin d'assurer une oxygénation adéquate, nous essayons de maintenir une PaO 2 maternelle de plus de 65 mm Hg. Certains experts ont suggéré de livraison chez la femme gravement malade avec de la PAC. Ce doit être individualisée parce que les données font défaut au profit de la femme et le foetus. L'association entre le volume de l'hôpital et le taux de mortalité pour les patients qui sont hospitalisés pour infarctus aigu du myocarde, insuffisance cardiaque ou une pneumonie reste floue. Il est également connu de savoir si un seuil de volume d'une telle association existe. Dans cette étude récente (30) , l'admission à l'hôpital à volume plus élevé était associé à une réduction de la mortalité de l'infarctus aigu du myocarde, insuffisance cardiaque, et la pneumonie, bien qu'il y ait un seuil de volume dessus de laquelle et augmenté de volume spécifiques hôpital condition n'était plus significativement associée à une mortalité réduite.
Résumé
Les indicateurs de performance sont des outils pour aider les utilisateurs à mesurer les lignes directrices dans la mesure et les effets de la mise en œuvre des lignes directrices. Ces outils ou des mesures peuvent être des indicateurs du processus lui-même, les résultats, ou les deux. Les écarts par rapport aux recommandations sont attendues dans une proportion de cas, et la conformité dans 80% - 95% des cas est généralement approprié, en fonction de l'indicateur. Quatre indicateurs de performance spécifiques ont été retenus pour les orientations de la PAC, dont 3 se concentrer sur les questions de traitement et 1 qui traite de la prévention:
- Publication traitement empirique de la PAC devrait être conforme aux recommandations de ligne directrice. Des données existent qui prennent en charge le rôle de lignes directrices de la PAC et qui ont démontré des réductions de coûts, la durée moyenne de séjour (DMS), et la mortalité lorsque les directives sont suivies. Raisons de l'écart par rapport à ces lignes directrices devraient être clairement documentés dans le dossier médical.
- La première dose du traitement pour les patients qui sont admis à l'hôpital devrait être accordée à l'urgence. Contrairement aux lignes directrices antérieures, un délai précis n'est pas recommandée. L'initiation du traitement serait prévue dans les 6 - 8 heures de la présentation chaque fois que le diagnostic à l'admission est susceptible de la PAC. Une ruée vers le traitement sans un diagnostic de la PAC ne peut, cependant, suite à l'utilisation inappropriée des antibiotiques avec une augmentation concomitante des coûts, effets indésirables des médicaments, augmentation de la pression de sélection antibiotique, et, éventuellement, une résistance accrue aux antibiotiques. Il faudrait envisager un suivi du nombre de patients qui reçoivent des antibiotiques empiriques à l'urgence, mais sont admis à l'hôpital sans un diagnostic infectieux.
- Les données de mortalité pour tous les patients admis à la PAC quartiers, unités de soins intensifs ou des unités de suivi de haut niveau devraient être collectées. Bien que des outils pour prédire la mortalité et la gravité de la maladie existent, tels que le PSI et les critères de trottoir, respectivement, aucune n'est infaillible. Les taux de mortalité globale pour tous les patients avec PAC admis à l'hôpital, y compris les services de médecine générale, devraient être suivis et comparés avec les normes ajustée sur la gravité. En outre, une attention particulière devrait être accordée à la proportion de patients souffrant de la PAC, telle que définie dans le présent document, qui sont admis au départ à un non-USI ou une unité de suivi de haut niveau et à leur taux de mortalité.
- Il est important de déterminer quel est le pourcentage de patients à risque dans sa pratique a effectivement reçu la vaccination pour la grippe ou une infection à pneumocoques. Prévention de l'infection est nettement plus souhaitable que d'avoir à traiter établie infection, mais il est clair que les groupes cibles sont sous-vaccinés. Essayer d'augmenter le nombre de personnes protégées est un point final souhaitable et, par conséquent, un objectif valable. Cela est particulièrement vrai pour la grippe, parce que les données vaccin sont plus convaincants, mais il est important d'essayer de protéger contre l'infection pneumococcique ainsi. Couverture de 90% des adultes de plus de 65 ans devrait être la cible.
Accusé de réception:
Exprimé sa gratitude au Dr. Robert P. Hoffman Président, les maladies infectieuses, Mercy Medical Center, Springfield, MA (USA) pour les avis d'experts, l'examen et de soutien dans la préparation de ce manuscrit.
Lecture suggérée
World Health Organization
Streptococcus pneumoniae: Initiative for Vaccine Research (IVR)
U.S. Centers for Disease Control and Prevention
Pneumonia Can Be Prevented -- Vaccines Can Help
Références
- Anand N, Kollef MH. The alphabet soup of pneumonia: CAP, HAP, HCAP, NHAP and VAP. Semin Respir Crit Care Med 2009;30:3-9
- Gazmararian JA, Petersen R, Jamieson DJ, et al. Hospitalizations during pregnancy among managed care enrollees. Obstet Gynecol 2002;100:94-100
- Shariatzadeh MR, Marrie TJ. Pneumonia during pregnancy. Am J Med 2006;119:872-876
- Goodnight WH, Soper DE. Pneumonia in pregnancy. Crit Care Med 2005;33:S390-397
- File TM. Community-acquired pneumonia. Lancet 2003;362:1991--2001
- Lim WS, van der Eerden MM, Laing R, et al. Defining community acquired pneumonia severity on presentation to hospital: an international derivation and validation study. Thorax 2003;58:377--82
- Halm EA, Teirstein AS. Clinical Practice. Management of community-acquired pneumonia. N Engl J Med 2002;347:2039-2045
- Roson B, Carratala J, Fernandez-Sabe N, et al. Causes and factors associated with early failure in hospitalized patients with community-acquired pneumonia. Arch Intern Med 2004;164:502--8
- Mandell LA, Wunderink RG, Anzueto A, et al. Infectious Diseases Society of America/American Thoracic Society Consensus Guidelines on the management of community-acquired pneumonia in adults. Clin Infect Dis 2007;44(suppl):S27-72
- Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. Am J Respir Crit Care Med 2005;171:388--416
- Mortensen EM, Coley CM, Singer DE, et al. Causes of death for patients with community-acquired pneumonia: results from the Pneumonia Patient Outcomes Research Team cohort study. Arch Intern Med 2002;162:1059--64
- van der Eerden MM, Vlaspolder F, de Graaff CS, et al. Comparison between pathogen directed antibiotic treatment and empirical broad spectrum antibiotic treatment in patients with community acquired pneumonia: a prospective randomized study. Thorax 2005;60:672--8
- Fields BS, Benson RF, Besser RE. Legionella and Legionnaires' disease: 25 years of investigation. Clin Microbiol Rev 2002;15:506--26
- Arancibia F, Bauer TT, Ewig S, et al. Community-acquired pneumonia due to gram-negative bacteria and Pseudomonas aeruginosa: incidence, risk, and prognosis. Arch Intern Med 2002;162:1849--58
- Ramirez JA, Bordon J. Early switch from intravenous to oral antibiotics in hospitalized patients with bacteremic community-acquired Streptococcus pneumoniae pneumonia. Arch Intern Med 2001;161:848--50
- File TM. Community-acquired pneumonia. Lancet 2003;362:1991--2001
- Mene´ndez R, Torres A, Rodrı´guez de Castro F, et al. Reaching stability in community-acquired pneumonia: the effects of the severity of disease, treatment, and the characteristics of patients. Clin Infect Dis 2004;39:1783--90
- Almirall J, Bolibar I, Vidal J, et al. Epidemiology of community-acquired pneumonia in adults: a population-based study. Eur Respir J 2000;15:757--63
- Arancibia F, Ewig S, Martinez JA, et al. Antimicrobial treatment failures in patients with community-acquired pneumonia. Am J Respir Crit Care Med 2000;162:154--60
- Waterer GW, Somes GW, Wunderink RG. Monotherapy may be suboptimal for severe bacteremic pneumococcal pneumonia. Arch Intern Med 2001;161:1837--42
- Harper SA, Fukuda K, Uyeki TM, et al. Prevention and control of influenza: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR Recomm Rep 2005;54:1--40
- US Department of Health and Human Services. Sepsis and CAP: partnerships for diagnostics development. RFA no. RFA-AI-04-043. Available at: http://grants.nih.gov/grants/guide/rfa-files/RFA-AI-04-043.html Accessed 15 August 2010
- Lexau CA, Lynfield R, Danila R, et al. Changing epidemiology of invasive pneumococcal disease among older adults in the era of pediatric pneumococcal conjugate vaccine. JAMA 2005; 294:2043--51
- Harger JH, Ernest JM, Thurnau GR, et al. Risk factors and outcome of varicella-zoster virus pneumonia in pregnant women. J Infect Dis 2002;185:422-427
- Whitt ST, Koch GA, Fender B, et al. Histoplasmosis in pregnancy. Arch Intern Med 2004;164:454-458
- Ahmad H, Mehta NJ, Mikal VM, et al. Pneumocystis carinii pneumonia in pregnancy. Chest 2001;120:666-671
- Banhidy R, Acs N, Puho EH, et al. Maternal acute respiratory infectious diseases during pregnancy and birth outcomes. Eur J Epidemiol 2008;23:29-35
- Sheffield JS, Cunningham FG. Community-acquired pneumonia in pregnancy. Obstet Gynecol 2009;114:915-922
- Jin Y, Carriere KC, Marrie TJ, et al. The effects of community acquired pneumonia during pregnancy ending with a live birth. Am J Obstet Gynecol 2003;188:800-806
- Ross JS, Normand ST, Wang Y, et al. Hospital volume and 30-day mortality for three common medical conditions. N Engl J Med 2010;362:1110-1118
Publié: 21 September 2010
Dedicated to Women's and Children's Well-being and Health Care Worldwide
www.womenshealthsection.com


