Thrombophilies héréditaires de la grossesseBulletin WHEC pratique et de directives cliniques de gestion pour les fournisseurs de soins de santé. Subvention à l'éducation fournie par la santé des femmes et de l'Education Center (WHEC). Identification des thrombophilies héréditaires a augmenté notre compréhension d'un étiologie potentiel de thromboembolie veineuse (TEV) et de l'hypercoagulabilité en général. Certaines mutations qui contribuent, y compris la mutation facteur V Leiden, mutation G20210A de la prothrombine, et la méthylène tétrahydrofolate réductase C677T polymorphisme (MTHFR), sont très courants dans la population générale. Au cours des 10 dernières années, certaines études ont suggéré que thrombophilie héréditaire peut être associée à la pré-éclampsie et d'autres effets indésirables de la grossesse. Il ya peu de preuves pour guider le dépistage et la gestion de ces pathologies pendant la grossesse. La grossesse réussie, il faut éviter d'hémorragie lors de l'implantation, le remodelage cytotrophoblaste endovasculaire des artères spiralées maternelles, et au cours de la troisième phase du travail, mais exige également le maintien d'une circulation de fluide utéroplacentaire. Maintien de l'équilibre hémostatique pendant la grossesse exige des modifications dans les deux locaux de l'utérus et systémique de la coagulation, ainsi que des protéines anticoagulantes et fibrinolytiques. Il ya une forte association entre thrombophilies héréditaires et la maladie thromboembolique veineuse, ce qui rend la détection de ces mutations d'une cible logique pour des stratégies de prévention. La thrombose est supposée être le mécanisme le plus commun sous-jacent de paralysie cérébrale dans de nombreux cas de thrombophilie maternelle ou foetale; pour cette raison, la compréhension de l'impact de la maternelle et ftale thrombophilie sur la grossesse est d'une importance primordiale lors du counseling des patients. Le but de ce document est d'examiner thrombophilies communes et leur association avec le risque thrombo-embolie veineuse maternelle et les résultats défavorables de la grossesse, les indications pour le dépistage pour détecter ces conditions, et les options de gestion de la grossesse. Est-ce qu'un maternelle et ftale thrombophilie travail jusqu'à nécessaire chez les femmes qui donnent naissance à un nourrisson né à terme avec la paralysie cérébrale? Des études prospectives sont nécessaires pour évaluer si tel est le cas. Dans cette revue, la littérature sur les ftus thrombophilie et son rôle dans l'explication de certains cas d'AVC périnatal que le plomb, en fin de compte, à la paralysie cérébrale sont également discutés. fondLa grossesse est marquée par la coagulation accrue, une diminution de l'activité anticoagulante, et une diminution de la fibrinolyse (1). Le potentiel thrombotique de la grossesse est exacerbée par la stase veineuse des membres inférieurs dues à la compression de la veine cave inférieure et des veines pelviennes par l'utérus qui s'élargit, une augmentation de l'hormone de médiation dans la capacitance veineuse, résistance à l'insuline, et l'hyperlipidémie. Ainsi, il n'est pas surprenant que la maladie thromboembolique veineuse complique environ 1 1.600 naissances et est une cause majeure de morbidité maternelle dans les Etats-Unis (2). Prévalence de communes thrombophilies héréditaires est la suivante: Thrombophilies héréditaires et issues défavorables de grossesseLe rôle que thrombophilies héréditaires ou acquises peuvent jouer dans la pathogenèse de la prééclampsie a été soigneusement étudié pendant plusieurs années. Les données de cette étude (11) montrent que la thrombophilie est associée à une augmentation de plus de 2,5 fois du risque de récidive de prééclampsie. Les résultats étaient similaires dans le sous-ensemble des femmes ayant le facteur V Leiden et du facteur mutations II, la forme la plus commune de thrombophilie héréditaire. L'observation que les patients qui ont déjà eu la pré-éclampsie sont à risque accru de développement ultérieur d'épisodes thrombo-emboliques est en outre preuves épidémiologiques reliant thrombophilie et la pré-éclampsie. Facteur V Leiden et du facteur II et mutations thrombophilie augmentera le risque de récidive de prééclampsie, et les femmes qui ont des antécédents de prééclampsie devraient être examinés pour thrombophilie pour identifier un groupe à risque élevé de femmes qui peuvent être admissibles à des essais d'intervention (11) . Les méta-analyses et une étude de cohorte rétrospective ont révélé une association entre thrombophilies héréditaires et pertes au premier trimestre de grossesse (12) . Le Eunice Kennedy Shriver National Institute of Child Health et materno-foetale sur le développement humain de la médecine Réseau d'unités testées femmes à faible risque avec une grossesse unique de moins de 14 semaines de gestation. La médecine maternelle et foetale Réseau d'unités identifié 134 femmes qui étaient hétérozygotes pour le facteur V Leiden parmi les 4,885 femmes enceintes, et n'a trouvé aucune augmentation de l'incidence de la perte du foetus (13) . Des résultats similaires de pas de risque accru de perte ftale ont été notées pour les transporteurs maternelle de la prothrombine G20210A mutation du gène(13). Examiner les études cas-témoins multiples, de cohorte et systématique n'ont pas réussi à détecter une association significative entre le facteur V Leiden et la restriction de croissance intra-utérin (RCIU) inférieur au 10e percentile ou moins que le 5e percentile (14) . Un manque similaire de l'association a été notée entre la prothrombine G20210A mutation et RCIU (14) . Dans l'ensemble, il ya suffisamment de preuves pour établir un lien entre thrombophilie et le décollement placentaire. Analyses prospectives de cohortes de facteur V Leiden, la prothrombine G20210A , et issue de la grossesse n'ont trouvé aucune association avec un décollement placentaire (15). L'étude homocystéine Hordaland trouvé une association entre un décollement placentaire et l'hyperhomocystéinémie supérieure à 15 micromoles association / L, mais minimal entre l'homozygotie pour le polymorphisme C677T MTHFR et le décollement placentaire(15). Considérations cliniquesDépistage des thrombophilies dans la controverse. Il est utile uniquement lorsque les résultats auront une incidence sur les décisions de gestion, et n'est pas utile dans les situations où le traitement est indiqué pour d'autres facteurs de risque. Le dépistage peut être pris en compte dans les paramètres cliniques suivants: Dans d'autres situations, les tests thrombophilie n'est pas systématiquement recommandée. Test de thrombophilies héréditaires chez les femmes qui ont subi des pertes ftales récurrentes ou décollement placentaire n'est pas recommandé. Bien qu'il puisse y avoir une association dans ces cas, il n'y a pas suffisamment de preuves cliniques que la prophylaxie antepartum avec l'héparine non fractionnée ou héparine de bas poids moléculaire (HBPM) prévient la récidive chez ces patients (17) . Cependant, le dépistage des anticorps antiphospholipides peut être appropriée chez les patients qui subissent une perte ftale. En outre, il n'y a pas de preuves suffisantes d'une association, et, par conséquent, suffisamment de preuves pour soit l'écran ou de traiter les femmes avec thrombophilies héréditaires et des histoires obstétricales qui incluent des complications telles que la prééclampsie ou IUGR. Tests de laboratoire pour thrombophiliesChaque fois que possible, des tests de laboratoire doivent être effectués à distance (après 6 semaines) de l'événement thrombotique et alors que la patiente n'est pas enceinte et ne prenant pas d'anticoagulation ou la thérapie hormonale. Les tests recommandés sont énumérés ci-dessous(18): 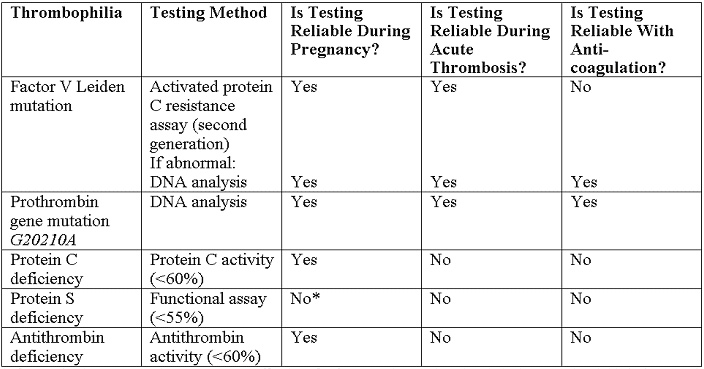 *NOTE - Si le dépistage pendant la grossesse est nécessaire, des valeurs seuils pour les niveaux protéine S libre antigène dans les deuxième et troisième trimestres ont été identifiées à moins de 30% et moins de 24%, respectivement. Schémas anticoagulants pour les femmes enceintesÉtant donné le risque et le ratio bénéfice de l'héparine non fractionnée, HBPM est généralement l'agent préféré pour la prophylaxie pendant la grossesse. Tous les patients atteints de thrombophilies héréditaires devraient subir une évaluation individualisée des risques, qui peuvent modifier les décisions de gestion. La nécessité d'ajuster la dose en fonction de HBPM anti-Xa est controversée. Divers l'héparine non fractionnée et les schémas d'HBPM sont décrites ci-dessous (18): 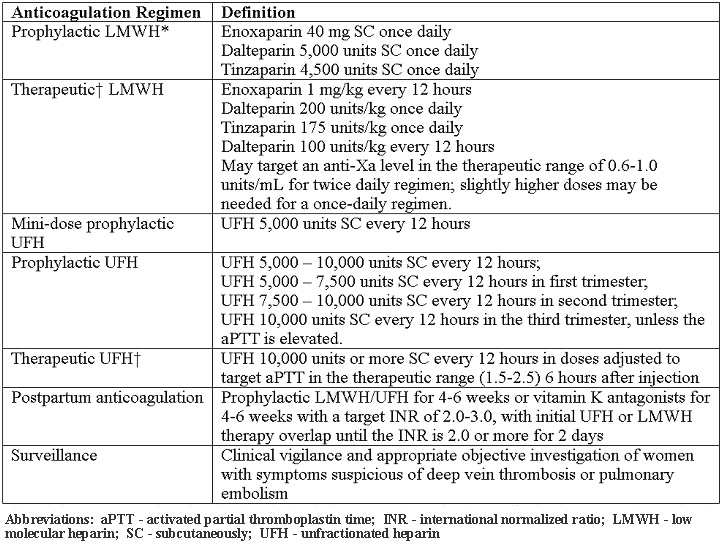 *Bien que dans des conditions extrêmes de poids corporel, la modification de la dose peut être nécessaire On parle aussi de poids ajusté, la dose de traitement complet Thromboprophylaxie recommandée pour les grossesses compliquées par thrombophilies héréditaires:La décision de traiter avec une thromboprophylaxie, un traitement anticoagulant, ou pas de traitement pharmacologique (surveillance prénatale) est influencée par l'histoire thrombo-embolie veineuse, la gravité de la thrombophilie héréditaire, et les facteurs de risque supplémentaires. Tous les patients atteints de thrombophilie héréditaire devraient subir une évaluation individualisée des risques, qui peuvent modifier les décisions de gestion. La décision concernant l'intensité du traitement peut être influencé par d'autres facteurs de risque, tels que l'accouchement par césarienne, une immobilité prolongée, l'obésité et des antécédents familiaux de thrombophilie ou thrombo-embolie veineuse. Nos recommandations sont les suivantes: Gestion intrapartum pour les patients thrombophiliquesL'utilisation de bottes pneumatiques de compression ou des bas élastiques doit être envisagée chez les patients ayant une thrombophilie connue jusqu'à ce qu'ils soient post-partum ambulatoire. En outre, la prophylaxie intrapartum avec l'héparine non fractionnée doit être envisagée chez les patients à risque élevé. Peu importe si le patient reçoit des doses prophylactiques, intermédiaires, ou thérapeutiques d'HBPM, il faudrait envisager de substituer une dose comparable de l'héparine non fractionnée à 36 semaines de gestation afin de permettre l'induction de l'anesthésie neuraxiale travail et l'accouchement (19) . Sinon, à dose ajustée sous-cutanée ou HBPM l'héparine non fractionnée peut être interrompu 24-36 heures avant l'induction du travail ou d'une césarienne planifiée afin d'éviter l'effet anticoagulant pendant la grossesse. Les patients recevant une anticoagulation prophylactique doit être 'instruction de suspendre leurs injections au début du travail. Si l'accouchement vaginal ou par césarienne est plus de 4 heures après une dose prophylactique d'héparine non fractionnée, le patient n'est pas un risque important de complications hémorragiques. Au-delà de 12 heures après une dose prophylactique ou 24 heures après une dose thérapeutique d'une HBPM, la rachianesthésie ne doit pas être retenu parce que le risque de la procédure liée à une hémorragie est limitée (20) . Les patients recevant l'héparine non fractionnée ou une HBPM qui ont besoin d'inversion rapide de l'effet anticoagulant de livraison peuvent être traitées avec du sulfate de protamine (20) . En outre, l'antithrombine concentrés peuvent être utilisés dans l'anti-thrombine patients déficients en cours de la période périnatale. Post-partum de gestionDoses du post-partum de l'héparine non fractionnée ou une HBPM doit être égale ou supérieure à la thérapie prénatale. L'héparine non fractionnée ou une HBPM peuvent être redémarrés en 4-6 heures après l'accouchement par voie vaginale ou 6-12 heures après l'accouchement par césarienne. Les patients qui seront traités par la warfarine peut commencer le traitement immédiatement après l'accouchement. La dose initiale de warfarine doit être de 5 mg par jour pendant 2 jours, avec les doses suivantes déterminées par le suivi du rapport international normalisé (RIN). Pour éviter la thrombose paradoxal et nécrose de la peau de l'effet C antiprotein début de la warfarine, les femmes devraient être maintenus sur les doses thérapeutiques d'héparine non fractionnée ou une HBPM pendant 5 jours et jusqu'à ce que l'INR soit thérapeutique (2,0-3,0) pour 2 jours consécutifs. Parce que la warfarine, des HBPM et l'héparine non fractionnée ne s'accumulent pas dans le lait maternel et ne pas provoquer un effet anticoagulant chez le nourrisson, ces anticoagulants sont compatibles avec l'allaitement (21), (22). Le risque de TEV chez les femmes utilisant l'oestrogène de contraceptifs oraux contenant augmente de 35 à 99 fois et 16 fois chez les femmes hétérozygotes pour le facteur V Leiden et G20210A de la prothrombine mutation, respectivement (23) . Le risque annuel de la TEV est de 5,7 pour 10.000 chez les porteurs du facteur V Leiden, par rapport à 28,5 pour 10.000 chez les femmes de facteur V Leiden hétérozygotes en utilisant des contraceptifs contenant des strogènes, le risque relatif de 34,7 (24) . Par conséquent, des méthodes alternatives, telles que les dispositifs intra-utérins (y compris ceux contenant un progestatif), les pilules progestatives ou implants, et les méthodes de barrière, doit être considéré. Cependant, le dépistage pour toutes les femmes avant d'initier la contraception thrombophilies association n'est pas recommandée. Ftale thrombophilie, paralysie périnatale des maladies et cérébraleThrombophilie décrit un spectre de troubles de la coagulation congénitaux ou acquis liés à la thrombose veineuse et artérielle. Ces troubles peuvent se manifester chez la mère ou du foetus, ou dans les deux simultanément. Ftale thrombophilie a une incidence de 2,4 à 5,1 cas pour 100.000 naissances (25) . Alors que la mère de thrombophilie a une incidence plus élevée par la suite, à la fois maternelle et ftale thrombophilie peut conduire à des effets indésirables maternels et ftaux. Thrombophilie conduit à une thrombose à l'interface maternelle ou foetale. Lorsque la thrombose se produit du côté maternel, la conséquence peut être sévère pré-éclampsie, RCIU, décollement placentaire, ou de la perte du foetus. Thrombose sur le côté du ftus peut être une source d'embolie qui contournent hépatique et la circulation pulmonaire et les voyages vers le cerveau du foetus (25) . En conséquence, le nouveau-né peut soutenir un événement catastrophique tel que la course artérielle périnatale par une thrombose artérielle, thrombose veineuse cérébrale du sinus, ou une thrombose veineuse rénale. AVC périnatal est défini comme un événement vasculaire cérébral qui se produit entre 28 semaines de gestation et 28 jours d'âge postnatal (26) . L'incidence est d'environ 17 à 93 cas pour 100.000 naissances vivantes (26) . accident vasculaire cérébral néonatal survient chez environ 1 sur tous les 4000 naissances vivantes. En outre, 1 dans tous les nouveau-nés de 2300 à 4000 est donné un diagnostic d'AVC ischémique dans la pépinière (26) . Artérielle AVC ischémique dans les comptes-nés pour 50% à 70% des cas de paralysie cérébrale congénitale hémiplégique. Facteur V Leiden mutation, mutation du gène de la prothrombine, et un déficit de la protéine C, protéine S, antithrombine III et ont pris en commun dans deux études, été identifiés dans plus de 50% des accidents vasculaires cérébraux ischémiques cérébraux (27) . En plus de ces thrombophilies, les facteurs de risque importants d'accident vasculaire cérébral périnatale et néonatale comprennent: Quelles sont les causes périnatales course? Le mécanisme sous-tend que l'AVC périnatal est un événement thrombo-embolique qui provient soit d'un navire intracrânienne ou extracrânienne, le cur, ou le placenta (27) . Une récente méta-analyse a révélé une corrélation statistiquement significative entre déficit en protéine C, MTHFR C677T, et la première occurrence d'accident vasculaire cérébral ischémique artérielle dans la population pédiatrique (28) . Le cerveau est l'organe le plus important et les plus vulnérables du foetus sensibles à thrombus qui se forment dans le placenta soit ou ailleurs. La présence de lésions vasculaires sévères ftales étroitement corrélée à une atteinte neurologique et la paralysie cérébrale. Une constatation pathologique, du ftus vasculopathie thrombotique (FTV), a été associée à une lésion cérébrale. La paralysie cérébrale est la déficience motrice chronique la plus fréquente de l'enfance. Environ 2 à 2,5 enfants sur 1000 sont donnés un diagnostic de ce trouble chaque année (29) . La condition apparaît tôt dans la vie, ce n'est pas le résultat d'une maladie évolutive reconnue. Les facteurs de risque pour la paralysie cérébrale sont multiples et hétérogènes: la prématurité, l'hypoxie et l'ischémie, et la thrombophilie. Bien que la thrombophilie est un facteur de risque reconnu pour la paralysie cérébrale, la force de l'association n'a pas encore été pleinement étudié. Malheureusement pour les patients et de leur progéniture, des preuves sur la relation entre thrombophilie et un résultat neurologique défavorable n'est pas suffisamment forte pour offrir beaucoup de la manière de formuler des recommandations définitives pour les obstétriciens. Nous suggérons, certaines recommandations provisoires sur la gestion: envisager le dépistage lorsque la paralysie cérébrale se produit en association avec AVC périnatal, le dépistage du ftus et la mère de la thrombophilie peut être réalisée (27) , (30) . Le panneau comprend recommandée thrombophilie tests pour: Dépistage familial a également été suggéré dans les cas suivants: 1) plusieurs facteurs de risque prothrombotiques dans un nouveau-né affectés, et 2) une histoire familiale positive. Le rapport coût-efficacité du dépistage de la thrombophilie n'a pas été évalué dans des études prospectives, car la valeur prédictive positive d'un tel dépistage est extrêmement faible. RésuméThrombophilies héréditaires sont un groupe hétérogène de troubles de la coagulation qui prédisposent les individus à des événements thrombo-emboliques. Ils sont facteurs de risque majeurs de thrombo-embolie pendant la grossesse et le post-partum. En outre, thrombophilies ont été impliqués dans une variété d'événements obstétricaux indésirables, y compris la perte de la grossesse (en particulier la mort du ftus), la pré-éclampsie, décollement placentaire, et RCIU. La physiopathologie est incertaine, mais on pense à associer une thrombose dans la circulation utéro-placentaire, ce qui conduit à un infarctus et d'insuffisance placentaire. Par conséquent, un traitement anticoagulant a le potentiel pour améliorer les résultats obstétriques chez les femmes atteintes héréditaires thrombophilies. Issues de la grossesse chez les femmes asymptomatiques ayant thrombophilies héréditaires sont souvent bonnes. Par conséquent, le traitement de routine avec une thromboprophylaxie ne peut être justifiée chez ces femmes. Hérité des tests thrombophilie chez les femmes qui ont subi des pertes ftales récurrentes ou décollement placentaire n'est pas recommandé car il est difficile de savoir si l'anticoagulation réduit la récurrence. En raison de l'absence d'association entre la mutation MTHFR et les résultats négatifs de grossesse, le dépistage avec les niveaux d'homocystéine à jeun ou des analyses de mutation MTHFR n'est pas recommandé. Dépistage des thrombophilies héréditaires doivent inclure le facteur V Leiden mutation; prothrombine G20210A mutation, et l'antithrombine, protéine C, protéine S et les carences. Tous les patients atteints de thrombophilies héréditaires devraient subir une évaluation individualisée des risques, qui peuvent modifier les décisions de gestion. Post-partum de la warfarine, HBPM, et l'anticoagulation l'héparine non fractionnée peut être utilisé chez les femmes qui allaitent. Une mère dont le bébé a reçu un diagnostic de thrombophilie et les accidents cérébrovasculaires ftale ou néonatale peut être offert thromboprophylaxie (héparine et l'aspirine) pendant toute la grossesse suivante. L'utilité de cette intervention n'a pas été bien étudié et repose uniquement sur ??l'opinion d'experts, cependant, il est donc impératif de conseiller les patients sur les risques et les avantages de la thérapie prophylactique avance. Remerciements: nous remercions le Dr. John R. Higgins, professeur d'obstétrique et de gynécologie, Chef du Collège de médecine et de la santé, University College Cork, Cork Hôpital Maternité Université, Wilton, Cork, pour servir à titre de réviseur et des suggestions utiles pour la compilation du manuscrit. Références
|