甲状旁腺疾病在妊娠WHEC实践公报和临床医疗服务管理的准则。 教育的拨款 , 由妇女健康和教育中心号巡逻艇(WHEC)。 甲状旁腺疾病是罕见怀孕,可能会产生重大的围产期和产妇发病率和死亡率如果没有诊断和适当的管理。原发性甲状旁腺功能亢进症(PHP)的,是在育龄妇女中罕见的疾病。该疾病的发病率不详,但肯定是罕见的,以及已报告的单一的以文献复习补充病例。 150多起,已载于英文文献,直到1999年(1),从那时起,个别病例报告。两个最新生儿发病率在PHP中常见的原因是早产和新生儿低血钙,与产妇血钙水平后者。甲状旁腺激素(PTH)(84个氨基酸,分子量9500),是由合成连续切割的亲甲状旁腺的甲状旁腺。循环甲状旁腺由至少有三种形式:1)完整激素(1-84,这是生物活性的半衰期为10分钟,生活),实际上10%的电镀池,2)的氨基末端片段,这亦是生物活性的,也有类似的半衰期短,代表10%的电镀池及3)羧基端片段,这些生物不活跃,弥补80%的电镀池。在循环PTH的形式代表了异质性的代谢和这种激素的灭活认识的一个重大问题。然而,最近一项对甲状旁腺的完整和生物活性形式的免疫放射发展澄清了这悬而未决的问题。 本文件的目的是审查钙稳态,原发性甲状旁腺功能亢进,甲状旁腺功能低下症,在怀孕期间和骨质疏松。普通话推广的骨骼钙的吸收。因此,甲状旁腺行动的所有事件都是针对提高血钙水平。在PHP的成功治疗产妇可瞬时改善先兆子痫和早产的临床发现。 钙代谢妊娠:血清钙是严格规范和内甲状旁腺激素(PTH)和维生素D的正常范围内保持着大约50%的血清钙蛋白的约束,主要是为了白蛋白,10%的络合的阴离子和40%的自由流通的离子钙。在怀孕期间,有一个积极的产妇钙转移到胎儿。阿足月婴儿,需要25至30克的钙在怀孕的过程中新骨矿化。妊娠期血清总钙为8%,低于产后的水平(2)。正常钙的上限是9.5毫克/毫升。这种血清总钙下降的原因是次要的生理低蛋白血症的血管扩张量正常在怀孕早期发现。离子钙的水平,但是,在整个妊娠保持不变。在生理活性的维生素D的形成1,25(OH)2的 D第3这是增加肠道吸收钙的责任,也骨吸收。在甲状旁腺,甲状旁腺素的生产,是刺激低钙血症和钙,镁浓度高镇压,1,25(OH)2的 D第3,也由低镁血症。甲状旁腺素的影响,不仅直接重新接纳骨骼,而且还刺激1,25(OH)2的 D第3形成钙代谢。有三种主要形式钙循环,即电离,蛋白结合,和螯合分数。电离分数的生理活性和homeostatically监管。孕妇血清甲状旁腺素水平,当一个敏感的检测准确完整甲状旁腺措施的水平来衡量,都略有下降,在怀孕的头一半(约20%的平均非怀孕值)和恢复正常的妊娠中期(3)。 1,25(OH)2的 D第3(骨化三醇)增加早期妊娠,作为肾1刺激的结果?-羟化酶活性的雌激素,胎盘生乳素和甲状旁腺素,以及钙三醇由胎盘合成血液水平(4)。既自由和总1,25(OH)2的 D第3是增加在怀孕期间,由于增加了总维生素D结合蛋白。 虽然机制胎盘钙负责运输知之甚少,钙,磷大量反对从母亲的浓度梯度转移给胎儿,胎儿的净积累长期被25至30克(主要集中在第三钙三个月)。产妇钙的吸收增加,通过甲状旁腺和怀孕期间1,25(OH)2的 D第3合成介导的上升,以满足这些要求。根据钙的摄入量,怀孕的母亲骨骼上的净影响可能是正面还是负面,在正常情况下有骨矿物质含量的影响不大。并联的血清白蛋白下降,血清总钙离子浓度下降,在妊娠期间,在离子钙(2)变化不大。在回答胎盘钙的转移,以及扩大的细胞数量,增加尿中钙的流失,甲状旁腺素浓度升高产妇在怀孕期间。血清25(OH)D的浓度基本上维持不变,而1,25(OH)2的 D第3水平也上升怀孕期间,在短期见顶,可能有胎盘贡献后者。有在怀孕降钙素含量的变化并不一致。 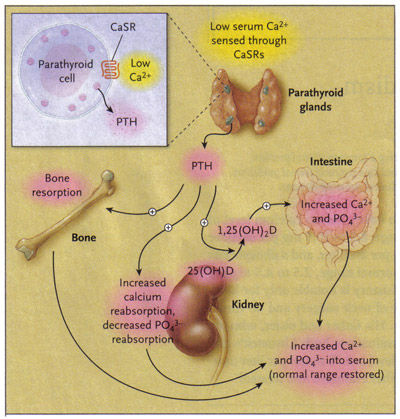 控制矿物质代谢的甲状旁腺激素,血清离子钙(Ca 2 +),甲状旁腺激素(PTH),1,25双羟维生素D(1,25 [羟基] 2个D),钙敏感受体(CaSRs),磷(以PO 4 3 - ),25羟维生素D(25 [俄亥俄州]深)。 胎儿甲状旁腺组织已确认了6周的妊娠,和骨骼矿化,由8周明显。道达尔和钙离子浓度升高,在胎儿期和减少新生儿期正常。普通话水平低,胎儿和出生后的增加。降钙素是架空的胎儿。在哺乳期的平均牛奶中的钙在人体每天损失220到340毫克。有一个小血钙下降,受甲状旁腺增长和1,25(OH)2的 D第3浓度陪同。这是总结如下: 矿物质钙稳态和激素的:
*胎盘转移; 甲状旁腺激素相关蛋白(PTHrP的),一个多肽的高钙血症负责在许多恶性肿瘤,增加早孕。阿血浆值的稳定增长是观察整个怀孕,在妊娠晚期和脐血(3)(2)高的峰值。在产后期血药浓度直接有关的程度母乳哺育。对孕妇血清PTHrP的来源是多方面的,既胎儿和产妇的网站已经假定(胎盘,羊膜,蜕膜,胎儿甲状旁腺,乳腺癌,脐带)。相关蛋白起着胎盘钙运输的作用,也可能在保护母亲在怀孕期间的骨架作用,因为羧基端PTHrP的一部分("素")已被证明能抑制破骨细胞性骨吸收(3)。相关蛋白可能参与了产妇钙转移到母乳。在钙和骨代谢的改变伴随着人类哺乳期是一个生理反应,是钙的摄入无关。 钙的调解子宫收缩的作用是行之有效的(8),如所引起的钙通道阻滞剂的使用,逮捕早产(9)。相比之下,钙,甲状旁腺激素和维生素的作用,血压调节D是不太清楚(10)。虽然胞浆钙调节血管张力,这是未知之数系统性钙或维生素D缺乏可引起高血压。这些缺陷已经假定增加先兆子痫的危险,但孕妇补钙没有证明的预防(11)(10)。 甲状旁腺功能亢进原发性甲状旁腺功能亢进症(PHP)的通常是由一个孤立的相关腺瘤(发生率80%)只涉及一个腺体,导致高钙血症和高钙(5)与过量PTH的自主生产。四个账户甲状旁腺增生小学约15%的病例报告,3%是由于多种腺瘤,只有因甲状腺癌少数的个案有文献报道。在成年人中,从0.15%不等甲状旁腺功能亢进症患病率为1%。尽管条件是2至3倍的妇女,在怀孕期间PHP的常见是罕见的。近70%的患者是在症状未孕状态,诊断是通过生化筛查常规使用的。在怀孕,因为常规钙不执行决定的,该病的表现已出现在几乎70%的患者确诊。甲状腺癌是一种罕见的甲状旁腺功能亢进的原因,但很少的个案有文献报道。在这种情况下血钙水平显着高于在(6)PHP(六)其他原因。围产儿死亡率和发病率要高得多。高钙血症的值大于13毫克/在一个存在明显的颈部肿块毫升应提高对甲状腺癌的强烈怀疑。相反,甲状腺结节是在温和的高钙血症和颈部肿块,颈部的病变最常见的原因存在。另外一个特点甲状腺癌的临床特点是,病人的反应冷淡,如密集的水化和循环利尿剂通常的临床治疗措施。手术是唯一有效的疗法。 常见症状及甲状旁腺功能亢进症介绍包括:肾结石,胰腺炎,骨头疼痛,肌肉无力,高血压和hypercalcemic危机。甲状旁腺功能亢进症,应考虑急性胰腺炎的鉴别诊断怀孕期间。急性胰腺炎据报道,在13%的妇女原发性甲状旁腺功能亢进症(7)。在非妊娠妇女甲状旁腺功能亢进症发病率约为1.5%,小于1%,在正常妊娠。这种并发症是与新生儿和产妇发病率(7)重大率。这是较常见的谁曾多次怀孕妇女的产妇。用PHP急性胰腺炎是最有可能发生在怀孕或产后期间的最后三个月,而且已在怀孕的头三个月报道,模仿妊娠剧吐。血清钙水平应取得任何重大的持续孕妇恶心,呕吐,腹痛。 Hyperparathyroid危机,PHP的严重并发症,据报道,在妊娠期间和产后,是严重的恶心和呕吐,全身乏力,精神状态的变化特点,并严重脱水。 为了总结高钙血症产妇特点: 泌尿系统:肾结石,肾钙化和尿; 鉴别诊断的高钙血症:虽然与高钙血症最年轻妇女有PHP的,其他不寻常的原因应该排除,主要是内分泌失调,维生素D或A过量,对噻嗪类利尿剂,或肉芽肿病的使用。因怀孕3个罕见的原因是:家族hypocalciuric血症(FHH),产后甲状旁腺功能低下症和相关蛋白血症引起的高钙血症。与怀孕无关的其他原因包括:恶性肿瘤,内分泌-甲亢和/或肾上腺皮质功能低下,维生素D和A过量,药物-噻嗪类利尿剂,锂,肉芽肿疾病-结节病,结核病,组织胞浆菌病,球孢子菌病,奶碱综合征急性和慢性肾功能衰竭和全肠外营养。 FHH是一种常染色体和一对高血钙高外显率的主要条件。这种紊乱与在该基因的失活突变钙传感器受体(12)。该受体的主要职能是通过在甲状旁腺变化和肾脏的钙平衡调节。轻度高钙血症,轻度升高血清甲状旁腺素,温和的高镁血症,低尿钙排泄是典型的结果。有四个甲状旁腺中度增生。总甲状旁腺很少表示由于疾病(12)良性过程。出生与FHH的母亲,可能会与不同的临床表现婴儿。第一无症状高血钙可发展受影响的后代如果母亲是一个FHH载体。第二种情况是,严重的新生儿低钙血症可能发生在一个FHH综合征的母亲。虽然新生儿低钙血症可能是严重的,新生儿甲状腺功能恢复正常,几个星期后交货。在第三种情况,严重的新生儿血钙,也称为新生儿重症甲状旁腺功能亢进症,发生在婴儿的FHH基因缺陷纯合子。一些婴儿需要甲状旁腺出生后不久。 产后可能出现高钙血症与甲状旁腺功能低下症治疗(13)妇女。对于高钙血症机制不能很好地理解。恶心和呕吐发展分娩后数天,脱水随之而来,和其他形式的高血钙发展,主要是心理的变化。血钙可明显升高。甲状旁腺功能低下症患者的治疗应遵循与血清钙测定产后和维生素D应该停止,如果发生高钙血症。在严重的情况下,静脉注射液和糖皮质激素治疗需要(14)。 高血钙少数情况下,PTHrP的介导,在怀孕期间和产后期已报告(13)(12)。在一个案例中,开发高血钙连续两次怀孕。在第二次怀孕,血清PTHrP水平升高3倍正常和婴儿是用温和的高钙血症的24小时内恢复正常分娩后出生的。在其他情况下,一个25岁的女子在24孕周大量双边隆乳。她的血清钙水平为14.3毫克/毫升,但她的血清甲状旁腺素水平检测到。怀孕期间,她经历了(12)双边乳房切除术。免疫组织化学研究表明,在乳腺组织相关蛋白抗原性的活动。 甲状旁腺功能亢进症的并发症和婴儿母亲的影响:在怀孕期间严重未经处理的PHP已经被报告导致高达67%,产妇并发症率,高达83%胎儿并发症发生率,以及高达53%的新生儿并发症发生率(其中约30%,占新生儿死亡(15)。孕产妇的并发症包括:吐,早产,先兆子痫和子痫,全身乏力,肾结石,胰腺炎和精神问题。总的产妇死亡率仍然很低,然而,胎儿发病率和死亡率显着。新生儿低钙血症的抽搐通常是一个短暂的现象,从有关的产妇,胎儿高钙血症导致胎儿甲状旁腺抑制,可能更长时间的成熟婴儿或与婴儿出生窒息。 管理:对于甲状旁腺功能亢进症在怀孕期间提出,标准做法,主张手术治疗。在第二和第三孕期甲状旁腺,是照顾怀孕的病人的症状标准,严重PHP和高钙血症超过12毫克/毫升(16)。不过,也有关于产妇/由于手术和长期的胎儿全身麻醉并发症的关注。然而,手术后的妊娠结果显示,4 - 5倍减少产妇/胎儿并发症发生率(17)。 PHP在妊娠成功利用微创治疗甲状旁腺由甲状旁腺腺瘤和串行普通话测量术前定位术中监护之前的报道。在本报告(17)妊娠术前肿瘤定位使用锝- 99m -异丁基异腈扫描获得了成功。优势包括避免不必要的手术探查,降低并发症发生率,缩短麻醉时间。低剂量和半衰期短减少胎儿辐射暴露(18)。串行测量术普通话很容易获得,确认完全取消的腺瘤,并排除multiglandular疾病。患者接受手术治疗,低钙血症,尽管短暂,后可能会出现在某些情况下手术。血清钙应检查每6小时,如果病人在发展葡萄糖酸钙,10至20一10%溶液毫升形式的低血钙症状,静脉注射钙,应可在5至10分钟内作出。间歇输注5%葡萄糖或等渗盐水和输注1毫克不断/公斤体重每小时体重。在骨疾病患者,手术后低钙血症可能是深远的,积极的治疗是需要的。这些患者可能需要数天前,维生素采取干预行动,在骨化三醇0.25至0.5微克形成维生素D /天。 轻度症状患者进行保守治疗,也有人建议。在治疗危及生命高钙血症可能会有问题,可能需要水化,速尿,磷酸盐,甚至血液透析。药物治疗是保留给那些具有重大高钙血症患者手术谁不是候选人。口腔作为1.5至2.5克/天已经显示出剂量无机磷磷酸盐治疗可有效地控制高血钙(12)。口服磷酸盐治疗的副作用包括恶心,呕吐,低血钾。这些问题可以很容易地避免减少药物剂量。在例病人手术是不可取的,重要的是防止血钙升高。良好的水化,泌尿道感染的早期治疗,避免药物已知会导致血清钙,如维生素D,维生素A,氨茶碱和噻嗪类利尿剂海拔都是重要的治疗措施。血清钙应确定定期。 甲状旁腺功能低下症获得性甲状旁腺功能减退症是最常见的结果不慎删除或不可逆转的破坏腺体,通常他们的血液供应,在甲状腺,甲状旁腺切除术,或根治性颈清扫术。手术后的永久性甲状旁腺功能低下症的定义有所不同,但普遍接受的定义是不够的普通话,以维持6个月后normocalcemia手术。据估计,甲状旁腺功能低下症后,会出现大约0.5至6.6%,占甲状腺,这一并发症的比率甚至更高一系列在某些情况下,而报告了高产量内分泌外科手术中心率0.9至1.6%(19)。特发性甲状旁腺功能减退症是一种疾病更常见的原因,经常与其他自身免疫性endocrinopathies相关作为多腺体自身免疫综合征1型的一部分。抗体针对甲状旁腺钙敏感受体已与56%的患者特发性甲状旁腺功能减退症检测。对于补充钙和维生素D可能在某些但并非所有的妇女减少甲状旁腺功能低下症,在怀孕和哺乳期的后半期的要求。在少数情况下,低血钙症状改善有妊娠进展。 临床特点包括抽搐,这可能是潜在的形式使用Chvostek引起的(面神经窃听)和特鲁索的测试(内三分钟,缺血诱导的抽搐发生在上肢)。其他症状包括感觉异常,喘鸣,肌肉痉挛,坦诚的精神,包括心理的变化。可显示的心电图QT间期延长。 诊断是由低钙,磷水平相结合,低甲状旁腺激素,1,25(OH)2的 D第3和nephrogenous cAMP的浓度。血浆碱性磷酸酶通常是正常的。低钙血症的鉴别诊断包括佝偻病,骨软化和低镁血症。显着低血钙症可能发生在病情严重的病人。其病因不明确,以恢复正常的血清钙是以下从急性事件(13)恢复统治。尿中钙,镁,肌酐测定在24小时收集也可以在甲状旁腺功能低下症的诊断有帮助。 甲状旁腺功能低下症的并发症和婴儿母亲的影响:维生素D缺乏症的母亲一直伴随着降低胎儿生长发育(20)。孕妇血清钙可能是正常怀孕期间或略有下降。之间存在着正相关产妇血清离子钙水平和冠脚跟的新生儿,说明缺乏维生素D的长度可能干扰通过对产妇钙稳态的影响胎儿生长发育。新生儿甲状旁腺功能亢进症可能发展中学产妇低钙血症。这可能会导致胎儿骨矿和增长的限制。这虽然是短暂的,骨骨折,可能会出现并发症死亡(20)。演示文稿可以充满变数,从临床及影像沉默案件等重症新生儿疾病和骨骨矿化。 管理:甲状旁腺功能低下症治疗并不不同于非妊娠状态,包括正常高钙饮食和维生素D的补充。怀孕的正常补充钙,约为1.2克/天。维生素D的要求可能会降低一些患者在怀孕的下半年。骨化1至3微克/天,是最经常使用与甲状旁腺功能低下症(21)受影响的大多数病人。骨化必须有单一或分次给药,因为它的半衰期比维生素D维生素D短,如果使用的剂量范围内的5.0万国际单位,是150,000 /周。与药物应该大力强调,尤其是当三醇的规定,在其半衰期短的看法,生活的重要性。在甲状旁腺功能低下症的治疗主要问题是高钙血症与低钙血症的发生。因此,血清钙的决定因素,应定期进行。维生素D中毒最常见的症状是恶心,便秘,疲劳,头痛,更严重的情况下,呕吐和脱水。重要的是要评估在怀孕期间血清钙,磷,特别是在产后时期,检测血钙(21)早发型。 急性症状低钙血症是临床急症,应以静脉注射钙处理; 10毫升10%葡萄糖酸钙对由一个0.5到2.0毫克注射后/千克/小时的钙元素,与葡萄糖稀释,以避免刺激静脉10分钟(21)。哺乳期服用维生素D可能会因禁忌母亲,因为维生素D 1,25(OH)2的 D第3代谢物中检测到了高浓度的母亲母乳中以50000国际单位维生素D。不管订明表格维生素D,钙测定血清应在产后期,特别是在哺乳期的母亲。维生素D高的水平,母乳可能会导致高钙血症,并损害了婴儿线性增长。 甲状旁腺功能减退症是对的激素替代疗法没有现成的少数endocrinopathies之一。只有少数小,随机试验评估了注射人甲状旁腺(1-34,巴赫姆加州与此条件(23)病人)使用。在为期3年的试验比较三醇甲状旁腺激素(1-34),均给予补充钙,每12小时,无论治疗维持在或略低于正常范围(七月六日至八月八号毫克/毫升[1月9日至二月二日的血清钙水平mmol每升]),但普通话的使用而减少尿钙排泄。虽然普通话显着增加骨代谢生化指标(如无显着变化与三醇相比),有在各组之间的骨(23)骨密度无差异。肌酐清除率并无明显差异之间的群体,他们在研究期间两组稳定。甲状旁腺激素(1-34)不批准美国食品和药物管理局(FDA)的使用。 假性:假性包括作为共同的几个不同的靶器官抗甲状旁腺功能有不同程度的障碍。体细胞的变化出现在一些综合征形式,包括身材矮小,肥胖,圆面,短指症,以及智力迟钝,脑钙化。这种变异被称为奥氏综合症1A型。大多数病人患有低钙血症,由于肾1错乱?-羟化酶和骨化三醇的生产。少数病例报告在怀孕期间(12)(13)。自发normocalcemia 2例发生在四次怀孕。的作者提供了骨化三醇胎盘合成的证据以考虑到normocalcemia。在这两个病人,血清甲状旁腺素,这是怀孕前显着增加,由50%降低妊娠期。脐血血清钙,磷,骨化三醇浓度在正常范围内。这些婴儿在子宫内胎儿甲状旁腺功能亢进症的风险,因为相对低血钙症可能是产妇在怀孕期间。 骨质疏松症在怀孕期间:在过去几年,一直是在怀孕和哺乳期骨质疏松症的临床几个方面的兴趣增加。一般来说,骨质疏松症是在怀孕的时候怀疑病人患有严重,持久性的或臀部疼痛,X线检查显示骨质疏松的迹象礼物。在每个测量的研究在怀孕三个月calcitrophic激素和生化指标骨重吸收和产后期显示,在孕晚期,在骨量略有下降,由在头6个月产后(22)恢复之后。诊断骨质疏松症可能是在怀孕期间或产后期。无论这些是两个不同的综合征或代表同一临床实体不清楚,因为这些症状可能在怀孕期间开始,但诊断为分娩后第一次提出。骨质疏松症诊断怀孕期间可能会在臀部本地化,腰椎,或两者兼而有之。在一个髋关节疼痛或背痛,是在大多数情况下的症状通常在妊娠下半年。自然恢复是通常当然是产后几个月。对骨质疏松症的影响泌乳是有争议的。鉴于争议,医疗服务提供者必须决定是否停止哺乳是骨质疏松症的管理是可取的。肝素相关骨质疏松症的报道(24)。这可能与肝素的总剂量。补钙治疗或骨化,虽然没有证实,可能会有所帮助那些接受肝素治疗的患者。 摘要:在与甲状旁腺功能亢进的甲状旁腺功能低下症患者进行初步评估应该包括详细的家族病史,这可能意味着某种遗传原因和有关的病史,特别是关于颈部手术和自体免疫疾病。实验室试验应包括测量血清总钙和离子,白蛋白,磷,镁,完整普通话水平。阿原因和PHP和先兆子痫或早产效应关系是可能的。产妇PHP的成功医治,可瞬时改善先兆子痫和早产的临床发现。维生素D代谢物和类似物是必不可少的甲状旁腺功能低下症的管理。并发症的关键是避免维生素D中毒(高钙血症和高钙尿症与肾脏和中枢神经系统的不利影响)。骨化三醇是优于维生素D 2或D 3,因为它的效力和迅速开始行动失调和。尽管骨质疏松症已被确诊怀孕期间,怀孕unmasks而不是骨量低的原因。在怀孕期间姿势的变化,包括增加前凸,当在一个小骨量减少和瞬时叠加,可能导致疼痛,甚至骨折。肝素在不利的影响大约三分之一的病人暴露的骨骼密度。 参考文献:
|