的死胎评价和管理WHEC实践公报和临床管理准则的医疗保健提供商。教育补助金所提供妇女保健和教育中心( WHEC ) 。 死胎是最具有毁灭性的,以及常见的产科并发症之一,影响超过300万每年在世界各地(1)怀孕。尚未回答的主要问题是最佳的诊断评估的情况下,死胎。重要的心理和情绪问题出现时处理的怀孕导致胎死腹中。夫妇经常遇到焦虑,失败,内疚,忧虑时考虑怀孕后,死产婴儿的感情。很多女性没有得到全面的辅导死胎的原因,因为一个不完整的评价是,在50%的情况下的原因仍然不明。这是很难为临床医生律师,评估和管理最佳,因为随后的怀孕后死胎妊娠结局非常知之甚少。有几个方面的原因,它可以很难确定一个"事业"死胎。首先,死胎的原因是复杂的,多因素的。同时发生的几个条件可能有助于到一个给定的死胎和它可能不能够确定一个单一的近因。其次,许多条件,而不是死胎的原因是"风险因素"。这些条件往往是在怀孕与活产婴儿。例子包括吸烟,肥胖,或控制糖尿病。三,死亡的原因可能不被识别,即使经过了充分的评价死胎。最后,还有一些可能的原因的死胎,还没有被发现。 本文件的目的是审查死胎上的当前信息,包括定义和管理,胎死腹中的评价,以及预防的战略。有一个缺乏的结果,怀孕后死胎的信息。之前死胎与2倍〜10倍的增加的风险在未来怀孕死胎。风险取决于在之前的死胎,胎儿生长受限的存在,孕周的前死胎,和种族的病因。家长团体之间的长期死胎是首选,最近的研究工作已经开始使用这个词的地方胎儿死亡。因此,在本文档中,术语死胎被使用。必须强调的是,标准为死胎并不意味着一个点的可行性和选择,以方便统一的数据收集。在美国,胎儿终止妊娠的劳动previable胎膜早破的致命胎儿畸形和归纳的损失明确排除从死产统计,被列为终止妊娠。 流行病学死胎死产是在美国最常见的不良妊娠结局的发生在每200怀孕,这相当于每年约26,000死胎(2) 。在美国的死产率在过去的15年里,1000名活产婴儿的6.2%,在2003年(2)的速度略有下降。这是近1 160个怀孕。减少死胎,主要是在妊娠28周后的死胎。许多死产是由遗传原因。这些包括非整倍体综合征,畸形,和单基因(包括孟德尔)紊乱。死产构成的所有围产儿死亡率的一半,50%的死亡原因不明。死胎率有显着的种族差异率,非西班牙裔黑人妇女的两倍多,非西班牙裔白人妇女 (2). 死胎率有较大幅度下降(20每1000名出生的婴儿)从20世纪50年代到80年代与改善的条件,例如,红细胞同种免疫,糖尿病和先兆子痫的护理。然而,死产率一直比较稳定,在过去的20年里,在美国达到一个高原。率早期死胎(2027周)的,自1990年以来,一直稳定在1000名出生的婴儿约3.2%,而后期死胎率(28周或以上)从4.3下降到3.1,每1000名出生婴儿。2004年,在美国的死胎率是6.2%,1000下跌至6.4每1000名出生于2002年(2) 。在发达国家中,最常见的危险因素与死胎非西班牙裔黑人,初产妇,高龄产妇和肥胖。从公共健康的角度来看,肥胖,吸烟,药物和酒精的使用是常见的潜在的可改变的危险因素的不良妊娠结局。在2001年,非裔美国人遭受了死胎率12.1每1000名出生的婴儿相比,5.5%1,000的白人 (3). 定义在不同的国家不同的死产的定义(和死产率),根据胎龄。在美国,死胎(定义为胎死宫内孕> 20周)影响约1 160怀孕(6-7每1000名出生的婴儿)。在大多数高收入国家,每1000名出生婴儿(3-5)率是相似的,而且是相当高的,每1000名出生婴儿(20-100)在低收入和中等收入国家(1) 。美国国家卫生统计中心的定义胎儿死亡(死胎)交付的胎儿没有生命迹象的情况下呼吸,心脏跳动,搏动的脐带,或具有明确的自愿肌肉的运动(4)。没有国家之间出生体重和胎龄的胎儿死亡报告准则方面的完全统一。然而,所建议的要求是在20周或更大妊娠(如果胎龄是已知的),或大于或等于至350克的重量如果不知道胎龄报告胎儿死亡。截止350克的重量在妊娠20周第50个百分。 分类死胎在许多情况下,它是死胎的病因难以确定。首先,很多情况下是无法解释的,尽管深入调查的潜在原因。其次,在个别情况下多于一个的条件可能有助于死胎。例如,感染可能发生在胎儿18三体综合征。它可能无法精确地确定哪些障碍是直接的损失负责。事实上,这是有可能的死胎,有些情况下,由于多种因素的贡献。最后,条件可以与死胎不直接导致它们的情况下。这些担忧导致多种分类系统的发展,死胎的原因。没有一个单一的分类系统是全世界公认的,每个人都有长处和短处。1980年威格尔斯沃和合作伙伴介绍了9类的分类系统,是目前最常用的报告围产期死亡率 (5). I。威格尔斯沃分类:
Gardosi等人最近提出的一种新的分类方案,其中新生儿死亡(6)被排除在外。虽然这个分类中提到的编码原发性和继发性的"原因",死胎,我们的目标是在子宫内死亡时间在确定有关的条件。它是一个分层分类的层次结构从直接影响胎儿的条件,并向外移动,在解剖组。作者威格尔斯沃的分类相比,表现出显着减少时,未分类的死胎。这些作者强调的重要贡献,约50%的死胎与胎儿生长受限胎儿生长受限. II。RECODE(死亡)的相关条件分类:
*TORCH: 弓形体病,其他感染,风疹,巨细胞病毒,疱疹病毒 风险因素致的人口因素包括种族,社会经济地位,足够的产前保健,教育程度较低,高龄产妇(7)为死胎。非裔美国妇女拥有率,死胎率的两倍多为白人母亲。在某种程度上,这可能是由于次要危险因素,如社会经济地位和缺乏产前保健.
常用报道了产妇的危险因素和原因的死胎 (8):
染色体和基因异常约8-13%的死产(9),可以发现异常核型。在胎儿解剖异常染色体核型异常率超过20%的增长限制在那些,但在一个大的系列(9),在正常形成胎儿染色体异常的发现率是4.6%。如果出现异常核型的发现与死胎,最常见的异常是单倍体X(23%),21三体综合征(23%),18三体(21%),13三体(8%)。密闭胎盘嵌合体也已与死产的风险增加,但目前还不是标准测试(10)的一部分。遗传性异常染色体核型分析低估的贡献,死胎,因为在企图染色体核型细胞培养至50%是不成功的(10) 。细胞培养提高产量的一个策略是在发货前进行羊膜穿刺术。这是典型的后的女人有机会来处理她的婴儿死亡后硬膜外腔放置。在一个大的荷兰的一项研究中,入侵检测有更大的组织培养胎儿出生后(28%)的组织取样率(85%)比。此外,单基因缺陷和微缺失的例行评估,目前不推荐,因为不确定性的作用,这些基因异常。然而,它很可能是没有单基因缺陷是可能负责一个显着比例的死胎。具体的异常的遗传评价应遵循的临床病史,发现胎儿畸形。大约有20%的死产胎儿有畸形或骨骼异常,15%至20%有重大畸形 (11). 先天性畸形虽然有些人建议在选定的情况下,广泛产后对胎儿进行评估,频频发生的意外和意外的发现是常规的,全面的评估,死胎(12)的参数。使用这种方法,将有大约20%的死产检测先天性畸形胎儿的死亡原因。一个畸形的死亡原因被认为是基于特定的标准,履行下列其中一个是足够的,假设一个特定的过程是因果关系:
如果多个条件得到满足,过程中造成死亡的可能性会增加。 产妇年龄超过35岁旧的产妇年龄与死产的风险增加,在未产妇和多产的妇女(13) 。中老年妇女看到一个显着比例的围产儿死亡的致命的先天性染色体异常有关。率较低这种类型的围产儿死亡人口为基础的筛查染色体异常的引进做出了贡献。大规模的研究表明,中老年妇女的风险增加,不明原因的死胎在怀孕后期仍然存在,即使在控制的危险因素,如高血压,糖尿病,前置胎盘,多胎妊娠(13), (14) 。此外,还有似乎是第一次生育,高龄产妇的风险增加(13) ,将primiprous老年妇女之间的相互作用 。根据一项研究,死产的风险估计是在40岁未生产过的女性在妊娠37周后,1 116 1 304相同的年龄(13岁)在一个多产的女人。 感染已与死产在发达国家(15)的 10%至25%的感染。在发展中国家,是相当高的百分比。感染可能会引起死胎在多种方式。一个重要的器官,胎儿畸形,胎盘感染,导致胎盘功能减退,孕妇严重的全身性感染导致败血症,感染导致早产,产时胎儿死亡的损害,其中包括直接感染胎儿。它可以是困难的死胎,以确定是否是因感染,因为存在一些生物体有正常怀孕的健康妇女。请注意,建议在就任之前,感染是死胎的原因。 细菌感染: 许多细菌已被牵连的死胎的原因。这些都是阴道内的菌群,达到通过子宫颈上生殖道。他们可能会感染蜕膜和绒毛组织中,最终到达胎儿通过羊水。这些微生物包括大肠杆菌,克雷白杆菌, B组链球菌,支原体hominus,解脲脲原体,和杆菌物种。在极少数情况下,如单核细胞增生李斯特氏菌的细菌可以到达胎儿血行传播。这些生物可能会导致临床明显的羊膜腔内感染,发热,腹痛,子宫收缩。然而,症状可能是含糊其辞,使诊断困难,尤其是在相对 缓慢的生物,如支原体,Ureaplasmas,和李斯特菌感染的病例。 病毒感染: 最常见的病毒感染巨细胞病毒(CMV)。胎儿感染通常是与主要的孕产妇感染,这是发生在大约1%的孕妇在美国(16) 。虽然许多巨细胞病毒感染的胎儿受到不良影响,死胎是罕见的。由于胎儿巨细胞病毒感染是常见的,大多数婴儿能够存活,巨细胞病毒在胎儿和胎盘的组织学证据应该是存在的,如果死胎是可以归结为CMV。细小病毒B19是最常见的与怀孕的损失。该病毒攻击红细胞的前体和心肌细胞,导致贫血,心肌功能障碍,水肿,严重的情况下,死胎。细小病毒B19,据报道,目前在瑞典的一项研究,用聚合酶链反应来评估感染(17)在7.5%的胎儿死亡。已与许多其他病毒的零星死胎。柯萨奇病毒A和B型流感病毒可导致胎盘炎症,心肌炎,水肿和死亡。其他病毒,包括腺病毒,埃可病毒,肠道病毒,水痘,麻疹(麻疹),腮腺炎和风疹疫苗。在与这些病毒死胎的风险可以大大降低疫苗接种。人类免疫缺陷病毒(HIV)感染胎儿在子宫内,但很少导致死胎。相比之下,单纯疱疹病毒很少感染,但可引起死胎。 其他感染: 有几个常见的感染原因的死胎,螺旋体,寄生虫和其他类型的生物体。梅毒由梅毒螺旋体引起的,是与死胎。螺旋体可以穿过胎盘在怀孕后期。死产的发生可能是由于直接感染胎儿或胎盘感染的的胎盘炎症和血管病变。,死胎的风险,因为随着胎龄的增加,梅毒,梅毒螺旋体仍然会导致在美国,偶尔死胎率约10%100,000 (18)患有先天性梅毒。这是相当多见于一些流行地区,如密西西比河三角洲地区,弱势市区,在美墨边境地带,以及在发展中国家的发病率较高的条件。其他如在莱姆病的病原体伯氏疏螺旋体,螺旋体,零星死胎。刚地弓形虫是一种寄生虫,通过未煮熟的肉类或通过猫的粪便。它可能穿过胎盘娩出后产妇感染,导致胎儿感染和死亡。胎儿感染发生在约40%的情况下,更可能后来在酝酿(19) 。然而,胎儿感染的后果更为严重,在怀孕早期。据估计,5%的胎儿感染10至24周的妊娠会导致严重的问题,包括死亡(19) 。弓形虫病是罕见的在美国(约1),它可能是一个罕见的原因死胎(15) 。在其他国家的发病率是相当高的。 全身感染: 孕妇严重的全身性感染也可导致死胎。大多数的全身性感染胎儿的耐受性良好。然而,败血症可导致子宫缺血和胎盘灌注减少,导致在产前死胎。另外,全身性感染有时会引发早产和分娩。尤其是在设置的一个previable的婴儿,这可能会导致在产死胎。
评价胎死腹中最重要的测试评估的死胎,胎儿尸检,检查的胎盘,脐带和膜;和染色体核型评价。此外,出生缺陷和形态异常,提示遗传或发育异常的识别,尸检确定和/或确认的许多其他原因的死胎。问关于他们的具体问题和原因拒绝尸检的家庭是有帮助的。在许多情况下,可以减轻他们的恐惧与教育或修改的程序。在尸检被拒绝的情况,其中,部分尸检或产后磁共振成像(MRI)可以提供大量的信息(20) 。一个完整的尸检时,应遵循准则围产儿尸检。病理学家应该知道的临床病史,怀疑是遗传诊断,以及任何必要的组织收集,需要进行更多的分析。下面给出评价的一种算法 (11).
流程图的胎儿和胎盘评价 (11): 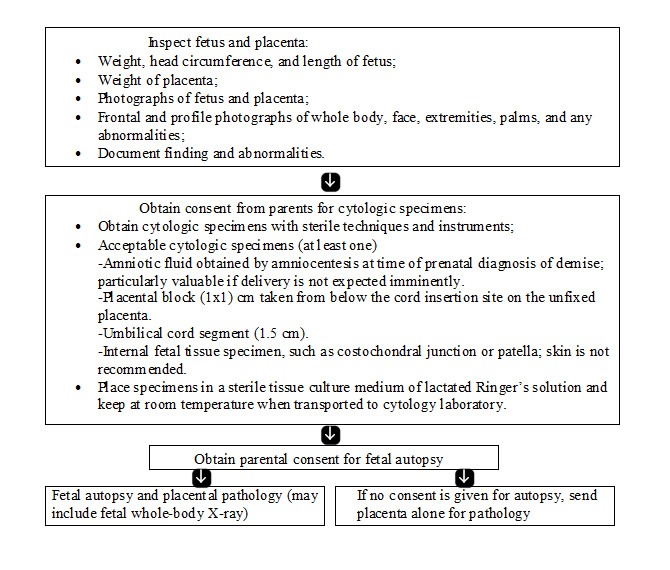 个完整的尸检替代品肉眼和显微镜检查,胎盘是一个必不可少的组成部分,任何死胎的评价,应包括审查的膜和脐带证实了尸检结果。即使家庭拒绝胎儿尸体解剖,组织学研究的胎盘通常是可以接受的,并找出潜在的病因,可以是有价值的。
胎儿的实验室研究胎儿染色体核型是有价值的,特别是在例其特征在于,不进行尸检。染色体异常是本死产(21)在至少6至12% 。异常核型的风险是较高的胎儿结构异常,畸形特征或死在妊娠早。这些危险因素可以用来分层的风险,如果成本是一个问题。组织最有可能成功地在培养基中培养的细胞,它可以提供包括胎盘(特别绒毛膜板),阔筋膜,皮肤的颈背,和肌腱。理想情况下,一个受过训练的病理学家应派组织染色体核型的胎儿和胎盘的总评价。如果这是不可能的,临床医生应注意不要把胎盘或胎儿组织可尝试在福尔马林,使培养细胞。比较基因组杂交显示了巨大的承诺,死胎染色体异常的识别,其中胎儿细胞不能成功地培养(22) 。在细胞培养不成功的情况下,临床医师应进行调查,比较基因组杂交是否可在其中心。无法识别的遗传异常染色体核型几乎肯定有助于某些情况下死胎。通过围产儿尸检提出怀疑的基础上,额外的基因检测特定条件下,可适当。然而,广泛的测试,单基因遗传病,缺失,而且只限于胎盘嵌合体仍然被认为是实验性的,在常规基础上提供这些测试的证据不足。胎儿染色体核型也很重要,如果家长进行一个平衡的染色体重排(如转或反转),或有马赛克的染色体核型。样品的羊水,脐带,胎儿组织,或胎盘可能获得为染色体和任何其他相关的测试。羊膜穿刺胎儿染色体核型具有最高的产量和是特别有价值的,如果交付的预期即将发生的 (9). 产妇的评价寻找已知条件或已与死胎这些症状,应采取一个彻底的母亲。死胎史和评估的重要组成部分和要素是:
本次妊娠胎儿宫内死亡的管理大多数女性都喜欢进行交付的胎儿后,胎儿死亡的诊断。这是一个没有自生能力的胎儿,尤其是在妊娠后期情绪紧张的进行。重要的是要提供两个选项,经历了胎死宫内的妇女分娩和期待。期待管理风险包括宫内感染和产妇凝血功能障碍。由于期待的管理相对不频繁的,这些风险差的特点。报告在两个星期内胎儿死亡(3) ,80-90%的女性会自发地劳动。但是,此"延迟时间"期间可能是足够长的。这似乎是明智的执行感染和凝血功能障碍在期待治疗的妇女进行监控。实例包括序列评估的产妇的温度,腹痛,出血,劳动。一般的办公室访问(如每周)可能是有用的,情感上的支持和医学监察。当局建议串口(如每周)测定全血计数,血小板计数和纤维蛋白原水平。这是不确定的用处。据报道,在谁保留一个死了的胎儿超过4周(23) ,但条件是在临床实践中是罕见的,通常不伴有临床后遗症患者的25%,消耗性凝血。纤维蛋白原水平低于100mg/dL被认为是凝血功能障碍的证据。应建议患者立即报告的症状,如发热,疼痛,出血,宫缩,漏出的液体,或犯规放电。 交付后胎儿死亡的方法和时机取决于胎龄死亡事件发生,对产妇的历史,以前的瘢痕子宫,和母亲的偏爱。虽然大多数患者的愿望,交货及时,交付时间是至关重要的;长期的胎儿保留与凝血功能障碍是罕见的。在孕中期,如果一个有经验的供应商,可以提供扩张和疏散,但应告知患者,扩张和疏散可能限制尸检的疗效宏观胎儿畸形检测。引产在以后的胎龄是适当的。在妊娠28周以前,阴道米索前列醇似乎是最有效的方法归纳,,不管宫颈Bishop评分(24) ,高剂量的催产素滴注虽然也是一个可以接受的选择。使用米索前列醇的典型剂量是200-400微克阴道,每4-12小时。在妊娠28周后,引产,应根据通常产科协议的管理。剖腹产胎儿死亡,应保留不寻常的情况下,因为它是没有任何胎儿的好处与潜在的孕产妇发病率。一些研究已经评估了使用米索前列醇400微克的剂量,每6小时的妇女与死胎之间的24和28周的妊娠和之前的疤痕子宫(25) 。现有的证据来自随机临床试验支持使用阴道米索前列醇作为非可行妊娠医疗终止妊娠24周前(25) 。需要进一步研究,以评估有效性和安全性,最佳的给药途径,剂量。在妊娠28周后的患者,宫颈成熟与宫颈导尿管一直伴随着子宫破裂率相比,自然分娩和在不利的子宫颈癌检查(26)的患者,这可能是有用的辅助。因此,基于有限的数据与前期低点横向剖宫产患者,审理劳动仍然是一个有利的选择。有有限的数据来指导临床实践与之前的古典剖宫产的病人,应该是个性化的交付计划。 随着胎龄,这些晚期胎儿死亡和半妊娠32周后的风险死胎发生在长期,尤其是年龄超过35岁的中老年妇女(13) 。理论上可以被避免长期死胎引产通过明智地使用,死胎预防的心脏位于许多公认的迹象引产的。然而,一旦孩子出生后,他或她面临着新的死亡风险,往往可能决定部分由出生时胎龄的风险。确定最佳的交付时间,以减少死胎的风险,一定要考虑孩子出生后面临的死亡风险。对于非异常足月出生的婴儿中,最常见的死亡原因是窒息,感染和婴儿猝死综合症(SIDS)。价格的感染和小岛屿发展中国家随孕周增加来看,在37周(31)率最高的。新生儿和婴幼儿死亡的风险,在多个研究已经显示出,以减少在任期,但随孕周增加再次妊娠41周(31), (32) 。胎龄和婴儿死亡之间的关系驱动的事实,小岛屿发展中国家是在非异常的婴儿(33)后新生儿死亡的主要原因。(34)这最近的一项研究估计的多个方面所面临的风险进行比较时,怀孕的妇女和她们的医疗服务提供者的风险死胎足月分娩后婴儿死亡的风险。得出的结论是,婴儿死亡率在39,40,妊娠41周低于1周的准管理的整体死亡风险。目前的研究表明,交付更大的死亡风险比在怀孕37周的准管理,在妊娠38周进行相当的风险,但在妊娠39周及以后变得有利。 丧亲之痛便利的丧亲之痛是一个重要的机会,为临床医生,以帮助家庭。病人的支持应包括情感上的支持和清晰的沟通测试结果。推荐丧亲之痛的辅导员,宗教领袖,同伴支持小组,或精神健康专业人士管理的悲伤和抑郁症可能是明智的。在经历了围产儿死亡的父母的内疚或愤怒的感情是常见的,当有一个不正常的孩子或遗传缺陷,可能会被放大。这是有帮助的,特别是在单位很少提供胎儿死亡(27)制定的标准协议。患者应提供的机会,以保持他们的婴儿和保持纪念品,如图片,脚和手印,以及石膏。有些家长可能在尸检结果欢迎讨论和救济的。测试的结果是重要的,即使在没有被识别特定的诊断。患者应该允许,使尽可能多的选择,有可能对他们的经验。长期住院是不必要的,应避免对产后病房的恢复。 随后的妊娠管理几乎所有的不良妊娠结局的风险的影响之前,产科史,死胎也不例外。复发死产风险没有得到很好的研究和个别病人的可靠数字往往是不可用的。最近来自密苏里州的人口为基础的研究指出死胎率22.7%1000前死胎的妇女,奇偶比为4.7,恕不另行死胎的妇女(28) 。,指出在非裔美国人(35.9 / 1,000)(28)与白人相比,增加复发风险。咨询会妨碍足够的信息,关于前死胎的病因。在许多情况下,现有的死胎可能是原因不明的,尽管一个彻底的评估。以下是管理的关键组成部分:
总结尽管在产前及产时监护,死胎在子宫内胎儿死亡定义为妊娠20周或更大,遗迹和重要的,主要是自发的,在产科和尖锐的问题的情况有所改善。在2004年,超过26000死胎的报道在美国。虽然有几个条件已与死胎,在许多情况下,它是很难界定的确切病因。本文综述了已知的和怀疑的死胎的原因,包括遗传异常,感染,胎儿孕产妇的出血,以及各种在母亲的医疗条件。进行定义和系统评价的中心,有一个诊断解释的死产的比例是较高的。在不明原因的死胎低风险的妇女,在妊娠20周后复发死胎的风险估计为7.8-10.5这种风险发生在妊娠37周前每1000名出生的婴儿。最流行的危险因素,非西班牙裔黑人的种族,初产妇,高龄产妇和肥胖与死胎。随后死胎的风险是以前的生活出生,生长受限的婴儿,比之前死胎的妇女妊娠32周前的妇女高两倍。羊膜穿刺术产前诊断具有最高的产量是特别有价值的,如果预计不会立即交付。 在孕中期,可提供扩张和疏散。引产是适当的,在以后的胎龄,,如果孕中期扩张和疏散是不可用的,或根据患者的意愿。阴道米索前列醇引产在低横向疤痕子宫妊娠28周前事先剖宫产术的患者是安全和有效的。死胎"后处理"的最佳是不确定的。最重要的测试在评价的死胎,胎儿尸检检查的胎盘,脐带和胎膜和染色体核型评价。其他测试,以考虑包括抗体筛查,Kliehauer-Betke,梅毒血清学,抗心磷脂抗体,狼疮抗凝屏幕,检测为遗传thrombophilias,尿毒理学屏幕和细小病毒血清学检查。随后的怀孕可能增加死胎和产科并发症的风险。治疗的基本的医疗保健,产科条件,产前监测,诱导劳动与胎儿成熟度可能会提高的结果。病人的支持应包括情感上的支持和清晰的沟通测试结果。推荐丧亲之痛的辅导员,宗教领袖,同伴支持小组,或精神健康专业人士管理的悲伤和抑郁症可能是明智的。 承认: 感谢: Dr. Robert M. Silver, 妇产科教授,主任,母胎医学科大学犹他大学健康科学中心,盐湖城,犹他州(美国)的贡献和有益的建议,在准备的稿子。特别感谢董事会的研究和开发提供资金。
推荐阅读
参考文献
|