Dispositifs pathologiques de Cancer utérinBulletin de pratique en matière de WHEC et directives cliniques de gestion pour des fournisseurs de soins de santé.La concession éducative a fourni par Health de Women's et centre d'éducation (WHEC). Pendant l'âge de grossesse, l'endometrium normal subitune série de changements séquentiels du cours du cycle ovulatory qui le préparent pour recevoir l'ovule. Si l'ovule n'est pas fertilisé, l'endometrium proliferative est moulé enlevé par la menstruation, et le cycle se répète. Un cycle endometrial normal est associé aux changements des deux glandes etstroma endometrial qui permettent au pathologiste de diagnostiquer au microscope la phase du cycle menstruel. La saignée utérine anormale beaucoup de fois est comme résultat d'une lésion identifiable telle que l'endométriose, le myoma submucous, le polype endometrial, ou le cancer en particulier dans les patients postmenopausal. De la plupart des série, approximativement 5% à 15% des caisses de la saignée postmenopausal sont dus au carcinome endometrial et à une proportion semblable avec les polypes endometrial (1). Le but de ce document est d'augmenter l'arrangement du hyperplasia endometrial et du neoplasia endometrial (cancer). Le plus comparateur, la stimulation ininterrompue prolongée d'oestrogène a comme conséquence le hyperplasia endometrial. Toutes les gradations de ce phénomène se produisent, s'étendant d'un distingué seulement avec la difficulté d'un endometrium proliferative exubérant normal (prétendu endometrium proliferative désordonné) à atypique qui approchel'aspect de l'adénocarcinome. Hyperplasia D'Endometrial :L'enseignement classique a été que les hyperplasias endometrial représentent un continuum de sévérité morphologique; la forme la plus grave nommée hyperplasia ou carcinome adénomateux atypique in situ, a été considérée le précurseur immédiat du carcinome endometrial (2). Depuis le milieu des années 80, ce concept de continuum a été défié. Les étudesde indépendant par Kurman et autres et Ferenczy et autres ont suggéré qu'il y ait le risque 1.6% de progression au carcinome dans les patients exempts d'atypia cytologic, comparé à un risque de 23% dans les patients avec l'atypia cytologic. Cette étude a également constaté que 29% de femmes avec le hyperplasiaatypique complexe continuent pour développer le cancer endometrial, et la recommandation standard pour des femmes avec le hyperplasia atypique complexe est hystérectomie et (3) salpingo-oopherectomy bilatéral : - Le hyperplasia d'Endometrial et le neoplasia endometrial sont les deux maladies biologiquement différentes.
- Le seul dispositif de distinction important est la présence ou l'absence de l'atypia cytologic.
- Le hyperplasia endometrial de condition est utilisépour n'importe quel degré de prolifération glandulaire exempt d'atypia cytologic et le neoplasia intraepithelial endometrial de condition pour des lésions avec l'atypia cytologic.
Dans la pratique journalière de la pathologie, le problème de différencier les quatre sous-types du hyperplasia estproduit seulement sporadiquement, et la reproductibilité diagnostiqueest très insuffisante. Les données suggèrent que la plupart des femmes avec le hyperplasia endometrial répondent à la thérapie de progestine. Les patients qui ne répondent pas sontà un sensiblement plus grand risque de progrès au cancer invahissantet devraient être conseillés d'avoir une hystérectomie. Les patients dans qui le carcinome endometrial se développe avec le hyperplasia concomitant sont pour être plus jeunes, meilleur-pour avoir différencié des tumeurs d'étape chirurgicaleinférieure, et pour avoir une meilleure cadence de cinq ans de survie. Cependant, la présence du hyperplasia endometrialne semble pas être un facteur pronostique indépendant dans l'analysemultivariable. Classification de l'organisation mondiale de la santé de hyperplasia d'Endometrial : I. Hyperplasia : 1) 2) complexe simple - adénomateux
II. Hyperplasia atypique : 1) 2) complexe simple - adénomateux atypique 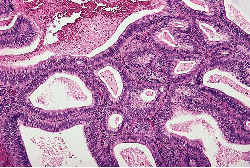 Divers types de hyperplasia endometrial : A, simple sans atypia. | 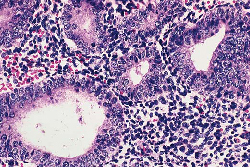 Divers types de hyperplasia endometrial : B, simple avec l'atypia. | 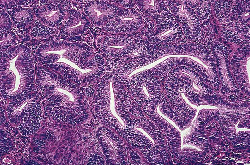 Divers types de hyperplasia endometrial : C, complexe. |
Le hyperplasia d'Endometrial le plus comparateur estvu pendant la période perimenopausal. Cependant, il peut également être produit dans de plus jeunes patients, même les adolescents. Certaines de ces derniers se développent comme résultat de stimulation estrogenic dans le syndrome polycystic d'ovaire et dans des néoplasmes ovariens desécrétion. La distinction entre un cas de hyperplasia grave et un adénocarcinome bien-différencié peut être très difficile ; en grande partie à cause du fait le hyperplasia et le carcinome endometrial représentent différentes remarques dans un continuum de la maladie aux niveaux génétiques morphologiques, d'ultrastructure, immunocytochemical, et moléculaires. Les dispositifs microscopiques favorisant le carcinome incluent le pleomorphism marqué avec la perte de polarité, la ramification complexe des glandes disposées désordonnées, les formations papillaires étendues, le modèle glandulaire confluent avec un aspectde solide ou de cribriform, et le stroma desmoplastic (4). Si la morphologie (en particulier morphometry nucléaire), immunohistochemistry quantitatifs, écoulement cystometry, ou d'autres techniques aideront ou changeront la morphologie conventionnelle dans ce problème difficile reste à voir. Critères microscopiques différentiels entre le hyperplasia d'Endometrial et l'adénocarcinome :Un endometrium ne devient pas nécessairement hyperplastic parce qu'il contient un changement metaplastic ; pareillement, un endometrium hyperplastic ne devient pas nécessairement malin parce qu'il est accompagné du metaplasia focal parce qu'il est accompagné du metaplasia focal de squamous ou d'un autre type. Une autre lésion qui est parfois confondue avec le hyperplasia (et qui peut réellement représenter un procédé hyperplastic localisé) est polype adénomateux, une lésion identifiée par son dense son stoma fibrotique dense et les navires à parois épaisses (5). Le hyperplasia sécréteur atypique de condition a été appliqué à un modèle des anomalies architecturales et d'atypia cellulaire dans un endometrium sécréteur, avec les glandes atypiques ressemblant à ceux vus en le 16ème à 17ème jour du cycle normal. Hyperplasia adénomateux - les critères microscopiques sont : Noyaux - réguliers et ovale, uniforme dans la taille, nucleoli petits et ronds, mitose nombreuse dans le stroma et glandes, cytoplasme abondant et amphophilic ; les glandes rayant l'épithélium est habituellement colomnaire grand, célibataire posées dilaté, irrégulier avec out-pouching et infoldings ; la taille du stroma est variable, habituellement abondant et cellulaire. Hyperplasia atypique - les critères microscopiques sont : Noyaux - irréguliers, grands et variables ; les nucleoli sont grands et irréguliers avec de nombreux mitoses ; le cytoplasme est parfois maigre, peut être très abondant avecl'éosinophilie dense ; les glandes rayant l'épithélium indique la stratification, perte de polarité, irrégulière avec orner intraglandular mais aucun jeter un pont sur ; la tailledu stroma est variable, limitée avec le encombrement. Adénocarcinome - les critères microscopiques sont : Noyaux - irréguliers, grands et variables ; les nucleoli sont grands, irréguliers et speculés ; les mitoses sont cytoplasme variable et maigre, pâles et amphophilic ; les glandes indiquent la perte de polarité, irrégulière avec le modèle de cribriform et jeter un pont sur intraglandular, la taille du stroma variables et limités. 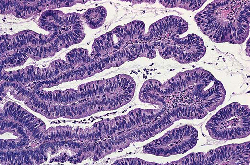 Adénocarcinome endometrial d'Endometrioid : A, puits a différencié. | 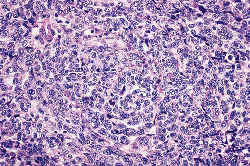 Adénocarcinome endometrial d'Endometrioid : B, modérément différencié. | 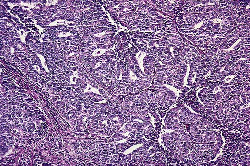 Adénocarcinome endometrial d'Endometrioid : C, mal différencié. | 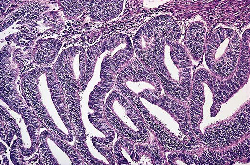 Adénocarcinome endometrial d'Endometrioid : D, avec le modèle villoglandular dela croissance. |
Rapport de hyperplasia et de carcinome d'Endometrial:Le rapport entre le hyperplasia et le carcinome a étéun sujet avec chaleur discuté (6). Sur la base de l'expériencecollective considérable qui s'est accumulée sur le sujet, les rapports suivants peuvent être sans risque faits : - La plupart des cas du carcinome endometrial du type d'endometroid sont précédés par une étape de hyperplasia. C'est particulièrement vrai dans les femmes plus jeunes et/ou dans les caisses des tumeurs différenciées meilleures, dans lesquelles cette séquence approche 100%.
- De façon générale, relativement peu de patients avec lehyperplasia développeront plus tard le cancer. Par conséquent, la seule présence du hyperplasia ne sert pas de base à l'hystérectomie.
- Plus le hyperplasia est plus grave, plus il est d'êtresuivi du carcinome plus probable. C'est particulièrement vrai en vue de les changements cytologic, même si ceux-ci assument encore une plus grande signification une fois couplés aux changementsarchitecturaux. Cette corrélation a été démontrée tous les deux utilisant l'évaluation morphologique conventionnelle et avec destechniques morphométriques.
- Dans le cas du hyperplasia simple (qui est souvent accompagné des changements cystiques), le risque est très petit. L'incidence a été citée moins de 0.4% d'une grande série. L'incidence du carcinome chez les femmes avec le hyperplasia complexe et atypique a été dans le voisinage de 15% et a atteint 30%de quelques séries.
Bien que le hyperplasia endometrial atypique constitue une menace du carcinome, ceci peut facilement être éliminé par des moyens médicaux (thérapie de progestogen) ou chirurgicaux (d'hystérectomie). La grande efficacité de la thérapie hormonale en contrôlant la plupart des cas de hyperplasia endometrial et en évitant l'hystérectomie dans lespatients postmenopausal chirurgicalement à haut risque a été à plusieurs reprises démontrée. Polypes D'Endometrial :La grande majorité de polypes endometrial ne sont pas des néoplasmes vrais mais représentent probablement les centres entourés du hyperplasia, probablement dus à une expression diminuée des récepteurs d'hormone dans le composant stromal. Excessivement, ils dépassent dans la cavité endometrial et montrent souvent les changements secondaires. Les glandes indiquent habituellement un certain degré de changement cystique. Elles peuvent être rayées par un actif pseudostratified l'épithélium contenant les figures mitotic ou dans le patient postmenopausal, par un épithélium plat et inactif. Les glandes et le stroma du polype sont insensibles à la stimulation de progestérone et maintiennent leur intégrité dans tout le cycle menstruel. Quelques lésions de polypoid montrent le hyperplasia simple ou complexe. En outre, les polypes endometrial avec un aspect typique coexistent souvent avec le hyperplasia endometrial. Tous les ces remarque d'observation à une pathogénie partagée pour ces deux lésions. Les polypes particulièrement endometrial contiennent les cellules stromal (bizarres) atypiques dispersées (7). Les polypes d'Endometrial se produisent avec la fréquence accrue après tamoxifen l'exposition. Ce sont caractéristiquement multiples, grands et fibrotiques, et peuvent exhiber le decidualization stromal et le metaplasia mucinous. Au niveau moléculaire, on dit qu'ils montrent une fréquence plus élevée des mutations de k-ras (8). Rarementdes polypes composés d'endometrium fonctionnel sont produits. Le diagnostic est fait sur les dispositifs bruts de la lésion plutôt que sur le modèle microscopique des glandes et du stroma et est impossible, donc, difficile ou même à faire sur un spécimen de D&C. La transformation maligne des polypes endometrial est une occurrence exceptionnelle mais bien documentée. Certaines de ces caisses présentent sous forme de carcinomasserous in situ ou invahissants. Carcinome D'Endometrial :On le croit actuellement que le carcinome endometrial peut être divisé dans deux types distincts sur la base de leur pathogénie : 1) l'occurrence plus comparatrice en raison de la stimulation estrogenic excessive et se développer sur un fond de hyperplasia endometrial, 2) de novo se développant. Le comportement clinique du carcinome endometrial d'endometrioid dépend en grande partie du degré de différentiation. Des tumeurs à haute teneur sont associées à plus de maladie d'avancer-étape. Les avances dans la biologie moléculaire ont mené au développement de la thérapeutique biologique visée quipeut avoir l'utilité potentielle dans le carcinome endometrial. L'activation de cascade d'AKT dans les cancers endometriald'endometrioid de la qualité 3 et les tumeurs mullerian mélangées malignes est une conclusion de roman. Apoptosis et croissance arrêtent que les résultats de l'inhibition d'AKT exposent des opportunités pour l'intervention thérapeutique (9). Quelques cas du carcinome endometrial, de l'endometrioid ou du type serous papillaire, ont été vus des années après irradiation pelvienne pour une autre condition, mais si ce sont spontanés ou induits par la radiation ne sont pas clairs. Les patients qui reçoivent tamoxifen pendant que le traitement à longterme pour le carcinome de sein sont à un risque accru pour le développement de l'adénocarcinome endometrial, de l'intérêt particulier est le fait que dans deux séries que un numéro significatif de ces caisses étaient les tumeurs à haute teneur a associé à un pronostic faible. Le carcinome d'Endometrial peut se développer dans n'importe quelle région anatomique du mucosa. Les tumeurs sedéveloppant dans de plus jeunes femmes ont une plus grande tendance d'impliquer le segment utérin inférieur. Excessivement, le carcinome de l'endometrium peut former les masses offrantes tout l'éventail de produits de polypoid ou infiltrer diffusément dans le myometrium. En général, l'invasion myometrial étendue est accompagnée de l'agrandissement utérin cliniquement discernable. Au microscope, approximativement 80% de tumeurs épithéliales malignes endometrial sont des adénocarcinomes conventionnels, qui sont habituellement divisés en bien-différencié (qualité I-50%), modéré-différencié (qualité II-35%), et pauvre-différencié (qualité III-15%). Les tumeurs différenciées meilleures récapitulent étroitement les dispositifs légers et à microscope électronique de l'endometrium non-néo-plastique, par conséquent du terme "endometrioid" qui est utilisé pour eux. Au-dessus d'un quart d'endometrioid les carcinomas ont lesfoyers papillaires, sur la surface ou dans les zones invahissantes. Ces tumeurs devraient être tranchant séparées des carcinomas serous papillaires beaucoup plus agressifs. Il devrait également noter que les parties les plus superficielles d'adénocarcinomes endometrial peuvent montrer des modèles simulant étroitement de divers états hyperplastic et metaplastic du mucosa endometrial. La fréquence et l'ampleur de l'invasion myometrial parle carcinome sont directement liées à la qualité microscopique de la tumeur. Le soin devrait être pris pour distinguer la véritable prolongation myometrial par le carcinome de l'expansion de la jonction endometrial-myometrial et des changements atypiques ou malins impliquant les centres préexistants de l'adénomyose ; la condition postérieure est identifiée par la présence du stroma endometrial autour des foyers glandulaires de prolifération intramyometrial. On lui a proposé que CD10immunostaining puisse aider dans cette distinction en accentuant lestroma endometrial lié à l'adénomyose quand présent. Cependant, une attention a été retentie de sorte que l'immunoreactivity CD10 puisse également être trouvé autour des centres de l'adénocarcinome invahissant (10). La prolongation du carcinome endometrial dans le cervix se produit dans plus de 10% si des cas, habituellement par invasion directe, maisprétendument aussi par implantation après D&C. Cette prolongation peut être excessivement évidente ou devenir évidente seulement à l'examen au microscope ; elle peut impliquer la surface seulement, le stroma fibreux, ou tous les deux. La présence et le type de prolongation cervicale ; quelles influences l'échafaudage de la tumeur mieux est trouvé par curettage partiel ; le soin devrait être pris en distinguantla véritable prolongation cervicale des fragments d'isolement de tumeur, ou bien une cadence élevé-faux-positive se produira. Les facteurs d'importance pronostique dans l'adénocarcinome endometrial sont les suivants : étape de tumeur ; niveau d'infiltration ; qualité microscopique ettype microscopique ; prolongation cervicale ; la dépendance d'oestrogène ; invasion de navire de lymphe ; invasion de vaisseau sanguin ; statut de récepteur d'hormone ; overexpression p53 ; Expression de HER2/neu ; récepteur épidermique de facteur de croissance ;ADN ploidy ; prolifération de cellules ; Gène de Rb ; et angiogenesis. La rechute de tumeur peut apparaître sous forme de répétition locale (50%), de métastases éloignées (28%), ou de toutes les deux (21%) ; l'intervalle médian a lieu entre 1 et 2 ans. Des répétitions locales peuvent être traitées avec succès avec la thérapie radiologique agressive. Carcinome utérin et Ovarien coexistant :Approximativement 8% de carcinomas endometrial sont accompagnés d'un carcinome ovarien simultané. Quand ils sont des types microscopiques semblables ; ce qui sont habituellement le cas - il devient difficile de décider s'il y a deuxtumeurs indépendantes ou si un des emplacements représente une métastase. Les dispositifs favorisant une nature metastaticpour la tumeur ovarienne incluent ce qui suit : une plus petite taille, une participation bilatérale, un modèle multinodular de croissance, une présence des implants extérieurs associés, et une invasion lymphatique ou vasculaire en avant dans le stroma ovarien. les études cytometric Immuno-histochimiques et d'ADN d'écoulement se sont avérées de la valeur limite seulement dans ce contexte. D'autre part, les études moléculaires faites pour l'évaluation du clonality (pertede heterozygosity, de mutations de PTEN, d'instabilité de microsatellite) ont fourni des informations plus convenables. Les résultats de ces évaluations combinées semblent indiquer que les deux situations se produisent mais qu'au moins dans le cas destumeurs d'endometrioid, il y a un plus grand numéro des néoplasmes utérins et ovariens primaires indépendants que des tumeurs endometrial métastasant à l'ovaire. Le Cancer de côlon de Non-Polyposis d'hérédité (HNPCC) ou lynchent le syndrome et le Cancer d'Endometrial :HNPCC également connu sous le nom de lynche syndrome est une maladie principalement héritée autosomal du système de dépannage de disparité d'ADN. Il a comme conséquence la susceptibilité génétique à beaucoup de types de malignités, maisles deux les plus comparateurs sont les cancers côlorectaux et endometrial. Presque tous les cancers côlorectaux de HNPCC-related et cancers endometrial démontrent l'instabilité de microsatellite, attendu que c'est une conclusion beaucoup moins comparatrice dans les cancers côlorectaux et endometrial sporadiques (11). Quelques centres préconisent le contrôle d'instabilité de microsatellite de tous les côlon et cancers endometrial, particulièrement ceux qui se produisent dans les patients sous l'âge 50. Le contrôle génétique est recommandé quand l'individu a une histoire personnelle ou des antécédents familiaux suggestifs d'un syndrome de susceptibilité decancer, quand le test peut être convenablement interprété, et quandles résultats d'essai influenceront la gestion médicale. On doit tenir compte que le cancer endometrial est le cancer supplémentaire-du côlon le plus comparateur dans ce syndrome et le risque ovarien de cancer est aussi bien élevé. Le risque cumulatif de vie de cancer endometrial dans ces patients estentre 40% et 60%, et le risque ovarien 12% de cancer. Si lepatient est exploré pour une autre raison, la considération devrait être donnée à la consultation concernant des risques et des prestations possibles d'une hystérectomie totale avec le salpingo-salpingo-oophorectomy bilatéral (12). Sommaire :Le carcinome de l'endometrium est la malignité gynécologique la plus comparatrice dans les pays industrialisés. Les cadences d'incidence les plus élevées sont aux Etats-Unis et au Canada, mais ces dernières années il y a eu un déclin dans l'incidence et la mortalité. Il se produit typiquement dans lesvieux individus, 80% des patients étant postmenopausal à l'heure du diagnostic. Cependant, il peut se produire dans n'importe quelle catégorie d'âge et a été même rapporté en association avec la grossesse intra-utérine. La différentiation entre le carcinome endometrial et endocervical est de plus grande importance. La distinction entre un cas de hyperplasia grave et un adénocarcinome bien-différencié peut être très difficile. Le hyperplasia persistant constitue une menace du carcinome et devrait être traité médicalement ou chirurgicalement. Des patients atypiques complexes de hyperplasia devraient être conseillés pour le gros risque de trouver un cancer concourant.Les femmes qui choisissent la gestion médicale conservatrice avec de la progestérone due à leur souhait pour maintenir le potentiel de grossesse devraient être au courant des risques. En outre, l'ultérieur très étroit avec des biopsies ou dilatation et curettage endometrial périodiques devrait être considéré. En portant un patient avec le hyperplasia complexe à la salle de fonctionnement, un chapitre congelé intraoperative est important. Le chirurgien devrait être disposé à exécuter l'échafaudage si eu besoin. Les deux emplacements évidents de la diffusion de gens dupays du carcinome endometrial sont le myometrium et le cervix, tous les deux avoir des connotations pronostiques importantes. Les emplacements les plus comparateurs de la répétition du carcinome endometrial sont le saut et le bassin vaginaux. Lesmétastases éloignées du carcinome endometrial sont plus comparatrices dans le poumon, le foie, l'os, le système nerveux central, et la peau. Les plus tard tendent à se produire dans la région de tête et de col, en particulier l'épicrâne. Occasionnellement, le carcinome lobulaire de sein metastatic est vu impliquer un polype endometrial tamoxifen-associé. References:
- Mutter GL, Nogales F, Kurman R et al. Endometrial Cancer: WHO classification of tumors: pathology and genetics, tumors of the breast and female genital organs. Lyon, 2002, IARC Press.
- Trimble CL. Atypical endometrial hyperplasia: a tough call. Int J Gynecol Cancer. 2005;15:401.
- Kurman RJ, Kaminski PF, Norris HJ. The behavior of endometrial hyperplasia. A long-term study of “untreated” hyperplasia in 170 patients. Cancer. 1985;56:403-12 (Level III).
- Mutter GL. Endometrial intraepithelial neoplasia (EIN): will it bring order to chaos? The Endometrial Collaborative Group. Gynecol Oncol. 2000;76:287-290
- Zaino RJ. Endometrial hyperplasia: is it time for a quantum leap to a new classification? Int J Gynecol Pathol. 2001;19:314-321
- Sivridis E, Giatromanolaki A. Prognostic aspects on endometrial hyperplasia and neoplasia. Virchows Arch. 2001;439:118-126
- Tai LH, Tavassoli FA. Endometrial polyps with atypical (bizarre) stromal cells. Am J Surg Pathol. 2002;26:505-509
- Rosi and Ackerman's Surgical Pathology. 9th edition 2004; volume two. Eds. Juan Rosi MD; 1582-1586.
- Rice LW, Stone RL, Xu M et al. Biologic targets for therapeutic intervention in endometrioid endometrial adenocarcinoma and mixed mullerian tumors. Am J Obstet Gynecol. 2006;194:1119-1128.
- Srodon M, Klein WM, Kurman RJ. CD10 immunostaining does not distinguish endometrial carcinoma invading myometrium from carcinoma involving adenomyosis. Am J Surg Pathol. 2003;27:786-789.
- Cohn DE, Frankel WL, Martin E, et al. Improved survival with an intact DNA mismatch repair system in endometrial cancer. Obstet Gynecol. 2006;108:1208-1215.
- Karlan BY, Berchuck A, Mutch D. The role of genetic testing for cancer susceptibility in gynecologic practice. Obstet Gynecol. 2007;110:115-167.
©
Le Centre pour la Santé et Éducation des Femmes
|