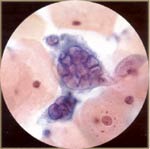
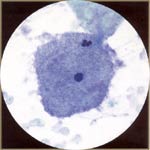
巴氏涂片Dr. Bruce R. Dziura 子宫颈抹片检查之前被用于临床实践中,子宫颈癌介绍是癌症的首要原因,有关美国女性死亡。没有其他的测试已被作为消灭子宫颈癌抹片检查成功。子宫颈癌仍然是妇女癌症死亡的主要病因有子宫颈抹片检查不普及。子宫颈癌及子宫颈抹片检查其前体的筛选是最成功的癌症检测策略不断发展。宫颈细胞学仍然是子宫颈癌根除极为有效的工具,因为它需要对宫颈上皮内瘤变(CIN)最早改变几年甚至几十年的进展外来癌症,多数情况下,宫颈自发回归,和大多数妇女被甄别更多一次以上 (1)。 本文件反映了新兴的临床和科研的进步。此信息不应该建造支配的待遇或程序独家应该遵循的道路。在实践中的变化,可能需要根据个别病人的,资源的需要,并限制特有的实践或机构的类型。 在美国妇产科学院'(司久岳)在巴氏试验检查频率的建议是:所有妇女谁是或谁已经达到18岁应该每年接受一次子宫颈抹片检查和骨盆检查。经过一个女人有三次以上连续,结果令人满意,正常的年度考试,巴氏试验可在低在她的医生(2)酌情风险女子那么频繁。 一些高风险因素已是与宫颈癌前病变和宫颈癌的发展。该组委会建议,在其中一个或多个风险因素的存在,更频繁的巴氏试验可能需要。高风险的因素包括:
在成本肿瘤阴道细胞学检查的成效后宫颈良性疾病的搬迁,未能证实。然而,定期细胞学评价阴道在这种情况下,基于上述风险因素是必要的。 收集方法: 在过去一段时间,在收集和制备方法,新的解释方法的调整,以及辅助考试,但被证实没有明显的下降,改善其特殊性的子宫颈抹片检查的灵敏度。最初,宫颈细胞样本,获得了后阴道池。它已经再三表明,这是一个贫穷的细胞来源,样本只应在企业Portio和endocervix收集。子宫颈细胞样本应获得使用无论是压舌板和宫颈刷或一个工具,可以收集无论从ectocervix和endocervix细胞。 幻灯片准备工作:传统方法:在实验室制备的传统方法是分散在载玻片上收集的材料,并立即进行纠正喷洒幻灯片或沉浸在小瓶它或者防腐剂。为了避免空气干燥的幻灯片,应立即修正错误的解释。有时涂片载玻片上放置厚,难以分析。 该液基薄层:液基系统使用专有固定剂的临床医师到地方收集装置。这些器件是激动的规定期限,并载有固定剂小瓶密封,标记,并提交给地方实际上是准备幻灯片实验室。美国食品和药物管理局(FDA)允许液基薄层技术会在市场推出的能够更好地探测到低等级和高等级鳞状(HSIL的和高度病变,分别上皮内病变),比准备(3)传统的方法。 看到SurePath系统:它也采用了专有的保存液在其中一个提供的收集装置被放置。液体和收集装置被送往实验室。 FDA已经批准了这项技术的使用,并允许它被视为等同于传统的巴氏试验销售。细胞收集和处理一些其他的方法,目前正在开发中。这些人还没有获得FDA的批准。 自动幻灯片解释:因为子宫颈细胞的解释是劳动密集,出现了极大的兴趣在计算机的发展为基础的系统,可以准确地读宫颈细胞学检查。幻灯片的FocalPoint探查已通过美国食品药品管理局的主要检查子宫颈细胞。该器件识别最多达25负的病变的,任何人需要审查(4)幻灯片%。由于计算机化解释可能减少周转时间,并有可能被节约成本,有一些公司正在开发的产品幻灯片解释。 2001年的贝塞斯达术语委员会建议,凡有一张幻灯片准备或解释使用任何形式的自动化,这一事实应是返回到临床报告中提到的。 各种诊断术语:
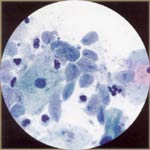
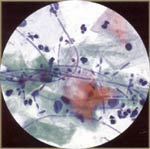
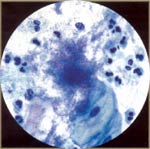
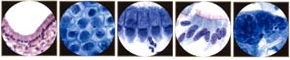
一,细胞学鳞状上皮:在正常成熟的宫颈鳞状上皮细胞,可从基底概念化分化/储备细胞parabasal细胞的中间细胞表面的细胞。这4个细胞是最常见的每天细胞学诊断问题的钥匙。胞质内提供有关的起源和功能的细胞分化的信息。为此,细胞质的功能是用来确定鳞状分化程度。鳞状分化的特点是不同的细胞质单元格边界和茂密的细胞质的积累。核提供了有关细胞的健康信息(无论是正常的,发炎,增生或肿瘤)。核特点确定在何处的恶性转化,或致癌连续,细胞可能。核大小,配置的变化,和染色质(hyperchromasia,粗化,并最终不规则分布)和核仁可见外观随后癌变的主要核功能。 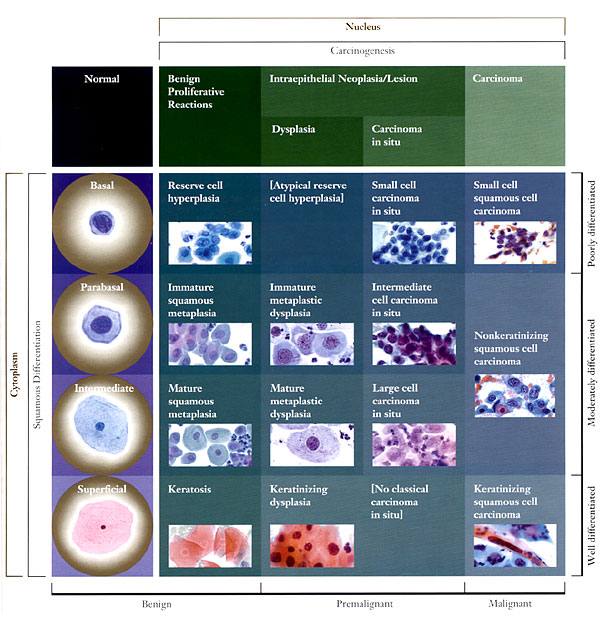 诊断分类矩阵 炎症的变化和具体感染: 瘙痒和阴道分泌物是最常见的原因,一名女子试图从她的妇科医生的意见。虽然子宫颈抹片检查可确定具体传染因子有用的,不应该用在更有效的诊断试验代替。许多事情可以引起炎症,对子宫颈抹片炎性改变的存在是对穷人的存在感染的指标。炎性改变可以模仿发育不良。持续性炎性改变病人的高作真正鳞状上皮异常的危险(宫颈上皮内瘤/鳞状上皮内病变)。 对发育不良的鉴别诊断队炎性改变:炎症原子核是大,但没有黑暗,或暗,但不是很大。红核表明炎症。发育异常核是大又黑。蓝核表明真正的发育不良。发育异常队炎症:程度的问题:多形性,较大的原子核,核不规则轮廓,更不正常染色质清晰和明确,更细胞疾病。晕:炎症队kilocytotic(5)。
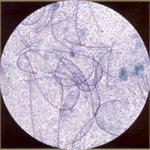
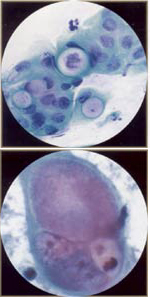
二。细胞学的腺上皮: 在女性生殖道腺上皮包括该endocervix,子宫内膜护岸及输卵管。子宫颈抹片检查是不如好一个腺体病变筛查,因为它是为鳞状病变。颈管细胞高大柱状,可分泌和纤毛。颈管细胞可以看到单独或带或说明书。请参见下面的图片: 子宫内膜细胞也可以形成三腺细胞三维集群,无需中央基质。这些细胞体积小,拥挤,以及核通常退化和hyperchromatic可以模仿原位癌。一个共同的子宫颈抹片检查,诊断的日常问题是区别于颈管细胞子宫内膜细胞。这可能是重要的,因为子宫内膜细胞的脱落是在月经周期的后半期不正常(尤其是过去40岁以上),或在绝经后妇女的任何时间。子宫内膜细胞异常脱落,附有一个子宫内膜增生或肿瘤的风险增加。见下图: 分子筛查宫颈癌:自巴氏(巴氏)引种试验超过60年前,出现了在美国子宫颈癌的死亡率下降70%,主要归因于执行和子宫颈细胞学检查计划的广泛接受。超过在美国谁开发宫颈癌的妇女有一半没有或没有甄别,筛选在过去的5年。然而,宫颈细胞学已经认识到,仅为51%,估计灵敏度的限制,在有必要重复定期子宫颈细胞产生的,以适应其限制。在美国,最巴氏试验利用液体为基础的技术与传统的细胞学比较。持续感染与致癌[高风险(人力资源)]人乳头状瘤病毒(HPV)的已被列为子宫颈癌(6)确定的根本原因,导致一些人认为现在是从细胞学检查移动到屏幕的HPV分子的DNA。这是重现性好,易于监督,并提供了一个客观的结果。这大大超过细胞学检查更敏感的探测高度宫颈上皮内瘤变。但是,HPV检测具有较低的特殊性,更昂贵的(7)。特异性较低可能会导致更下游的测试,如阴道镜和extirpative程序,包括循环电灼切除的患者,只有短暂感染的程序。 对加拿大宫颈癌筛查审判第一轮筛选,结果最近公布(4)。从此次测试的结果是一致的与以前的分裂样品和随机研究,揭示了更高的灵敏度(55%比为HPV DNA的测试,94.6%),而传统的宫颈细胞学检查,但特异性较低。由于这是第一轮筛选,提交人未能解决受负面HPV DNA检测得到保护的长度。另一位来自瑞典的子宫颈癌普查计划的研究报告最近报道,在子宫颈上皮内瘤变的发病率减少2 / 3的妇女在随后的检查谁最初与HPV DNA和常规细胞学只(8筛选)。他们的研究结果是一致的利用宫颈细胞学和HPV DNA检测其他试验。同时使用的测试病毒(HPV DNA和细胞学)大大提高了筛选的初始成本。液基细胞学减少了假阴性结果的数量相比,对女性的平均危险人群常规细胞学检查,虽然不是高危人群。这一技术还降低了不合格样本的比例相比,(3)常规涂片。根据对液体的潜力提高了灵敏度基细胞学与传统相比,细胞学,在为HPV DNA的检测灵敏度收益可能会减少。阿的HPV检测和液随机试验为基础的一个主要涉及2.5万名妇女宫颈细胞学检查在筛选呼吁阿提高细胞学(艺术)的随机试验,应该解决这个问题(6)。 最新公布的研究表明,HPV DNA的检查是例行的检查是在地平线上。然而,大型示范项目,将需要新的模式进行评估筛选,其中包括积极分流HPV DNA的检测与测试或重复也许可能通过宫颈细胞学其次。由负HPV DNA的检测提供的保护期长期等待检查数据,以确定最佳的筛查间隔。对自我的可能性收集阴道HPV DNA的样本可能进一步降低成本,增加获得检查是否快速,简便,准确和负担得起的HPV DNA的测试,开发(9)。子宫颈癌检查的最终目标是减少发病率和外来的成本效益,现成的测试全球子宫颈癌的死亡率。我们尚未达到这一目标。筛选潜在的新模式,包括积极分流HPV DNA的检测与测试或重复,也许可能通过宫颈细胞学其次。美国食品和药物管理局(FDA)2009年3月批准了第一的DNA测试,确定了病毒(HPV)引起之间的美国妇女(10)子宫颈癌多数人乳头状瘤病毒的两种。测试称为Cervista人乳头瘤病毒16/18,检测了人乳头瘤病毒16型和HPV型宫颈细胞的DNA序列18个。区分这些类型的HPV医护专业人员提供了更多的患者的后来宫颈癌的风险信息。一个积极的Cervista 16/18试验结果表明是否乳头瘤病毒16型,18或两者都在颈部样本中存在。 FDA还批准了Cervista乳头瘤病毒人力资源测试,这是第二次DNA检测,检测本质上是高风险的宫颈细胞样本类型HPV的。人乳头瘤病毒的Cervista人力资源测试使用的方法类似Cervista乳头瘤病毒16/18测试,以检测DNA的序列,这些类型的人类乳头瘤病毒。在女子30岁及以上或边缘细胞学妇女,Cervista乳头瘤病毒16/18测试可用于细胞学和Cervista乳头瘤病毒人力资源,共同评估测试颈椎疾病的危险。 摘要:虽然巴氏涂片可能会失败,多层次,具有讽刺意味的,最重要的错误是妇女不能达到当初子宫颈抹片检查。宫颈癌前面有一个长期疾病的侵袭前前驱,可以发现和治疗,这将使我们能够预防这种癌症。巴氏涂片只是一个子宫颈癌筛查,它具有低,但意义重大诊断错误率。阿"负面"报告没有保证的情况下宫颈癌。密切监视高危病人,包括多重感染和炎症的沉重,是重要的。所有抹片检查结果异常,应采取后续行动,非常重要的可疑病灶活检,应调查和可疑症状,即使巴氏是否定的。 参考文献:
|