Prevención del cáncer cervicouterino: Gestión de la neoplasia cervical de bajo gradoWHEC Boletín de la práctica clínica y directrices de gestión de los proveedores de atención médica. Educación subvención concedida por la Salud de la Mujer y el Centro de Educación (WHEC). El cáncer cervical es el cáncer más común en las mujeres, como los causados por el virus del papiloma humano (VPH). La mayoría de las mujeres sexualmente activas adquieren el VPH durante su vida. Aunque la infección desaparece en la mayoría de los casos, se conserva en algunas mujeres. la persistencia a largo plazo de HPV - en particular con tipos de alto riesgo - se ha establecido como una causa necesaria de las lesiones precancerosas. programas de cribado cervical han sido muy exitosos en los Estados Unidos, Europa y otras regiones, son capaces de lograr una cobertura amplia y sostenida. la prevención del cáncer cervicouterino ahora se puede hacer aún mejor. Las modificaciones sustanciales de la práctica son próximas, motivado por una mejor comprensión de la historia natural del VPH y la carcinogénesis cervical. Con base en el papel central de la persistencia de infecciones cervicales por cancerígenos genotipos del VPH en la carcinogénesis del cuello uterino, las pruebas de ADN del VPH se ha introducido en la detección del cáncer de cuello uterino. En 1999, los EE.UU. Food and Drug Administration (FDA) aprobó el primer cancerígenos o de alto riesgo del VPH prueba de ADN para la selección de la citología cervical equívoca y en 2003 para cotesting de mujeres de 30 años o más (Hybrid Capture 2; Qiagen Corporation, Gaithersburg, MD ). La American Cancer Society (ACS) en 2002 y un taller patrocinado por los Institutos Nacionales de Salud (NIH), Instituto Nacional del Cáncer (NCI), la Sociedad Americana de Colposcopia y Patología Cervical (ASCCP), y la AEC en 2004 publicó directrices para las pruebas de VPH coadyuvante con la citología cervical (cotesting) para la detección del cáncer de cuello uterino de la mujer de 30 años de edad en los Estados Unidos. La evidencia reciente ha demostrado que el riesgo de enfermedades malignas y premalignas de cuello uterino y las infecciones de VPH varía significativamente con la edad. Lo esencial de la prevención del cáncer de cuello uterino no han cambiado mucho en los últimos 50 años. La tecnología ha avanzado, pero sin alterar la estrategia básica o el rendimiento. Programas de detección de cáncer han tenido mucho éxito ya que el cáncer de cuello uterino por lo general se desarrolla lentamente durante décadas. rondas repetitivo de la detección de lesiones precancerosas de captura a medida que crecen, mientras que se puede tratar fácilmente. El propósito de este documento es discutir la relación de detección del VPH y citología anormal con diagnóstico histológico de las lesiones precancerosas de cuello uterino y el cáncer. El foco de esta discusión es sobre el manejo de células escamosas atípicas de significado socavado (ASCUS) y de bajo grado las lesiones intraepiteliales escamosas (SIL). Esta serie de Prevención del Cáncer Cervicouterino, también servirá como punto de partida para la comprensión de los efectos futuros de vacunación contra el VPH en los resultados de detección de cáncer cervical. El futuro de la prevención del cáncer de cuello uterino es probable que sea más eficaz, ya que se incluyen: la vacunación profiláctica de los adolescentes contra las infecciones de VPH cancerígenos; un mayor papel para las pruebas de VPH, la mejora en la colposcopia para aumentar la sensibilidad y la reducción en el número de pantallas de vida necesarios para prevención. Tabla de referencias: Adenocarcinoma in situ - AIS AntecedentesEn 2007, más de 13.000 mujeres fueron diagnosticadas con cáncer cervical en los Estados Unidos. El uso de Papanicolaou (Pap) ha sido acreditado con ayudar a prevenir la mortalidad por cáncer de cuello uterino y reducir las tasas de cáncer de cuello uterino en más de un 70% (1) . Sin embargo, en los Estados Unidos, de bajo grado las lesiones intraepiteliales escamosas (SIL), el paso inicial para la displasia cervical, anualmente se diagnostica en aproximadamente un millón de mujeres. La infección con la cepa de alto riesgo de VPH es considerada como el factor más importante en la iniciación de la carcinogénesis cervical. En consecuencia, la detección del VPH se ha generalizado y es una parte importante de la estratificación de riesgo y directrices de manejo clínico. La clave para el desarrollo de directrices eficaces para la gestión de las anomalías del cuello uterino es distinguir verdadero precursor del cáncer de cuello uterino benigno anormalidades cervicales con potencial premaligno poco. Ambos LSIL y CIN1 reflejan los efectos citológico e histológico de la infección con el VPH. La mayoría de estas lesiones no convertirse en cáncer. Sin embargo, hasta el 28% de las mujeres con citología LSIL puerto NIC 2 o NIC 3, aproximadamente dos tercios de los cuales se identifica por colposcopia (2) . Desde una perspectiva clínica, es importante distinguir que las lesiones intraepiteliales neoplásicas se convertirán en cáncer invasor si no se tratan. Sin embargo, las categorías diagnósticas actualmente disponibles tienen un valor predictivo sólo modestas, y ese valor disminuye a medida que las lesiones son menos graves. La probabilidad de progresión al cáncer es más alto y el tiempo hasta la progresión es más corto que el grado de aumento de la displasia. VPH y citología cervicalUna alta prevalencia de VPH, especialmente entre las mujeres jóvenes, no da lugar a enfermedades del cuello uterino en la mayoría de los casos. Cada vez menor, el riesgo de prevalencia de VPH de alto a través de aumento de público es consistente con otros estudios en los Estados Unidos y otros países desarrollados, en los programas de detección cervical son comunes (1) . Es probable que el sistema inmunológico elimina el virus del VPH con el tiempo y que el desarrollo de la neoplasia cervical en algunos individuos puede pertenecer a un fallo del sistema inmune o de otros factores genéticos o ambientales específicas de las personas. Los resultados que las tasas de cáncer de cuello uterino puede variar entre las razas, como los autores observaron (1) , se refieren a las diferencias en la historia natural de la infección entre las razas o las diferencias en el diagnóstico y la cura. En cualquier caso, el virus VPH parece estar involucrada en el desarrollo de la neoplasia cervical, y es de esperar, el programa de inmunización ahora en lugar de las mujeres jóvenes se reducirá este riesgo. Según la American Cancer Society (ACS), se estimaba que había 9.710 casos nuevos de cáncer de cuello uterino y 3.700 muertes por cáncer de cuello uterino en los Estados Unidos en 2006 (2) . La causa principal de cáncer cervical es el VPH, una infección de transmisión sexual, que varía en la prevalencia según la edad y el número de parejas sexuales. La prevalencia es mayor entre las mujeres jóvenes sexualmente activas que están expuestos por primera vez, y disminuye después de los 50 años. Las mujeres menores de 24 años de edad son generalmente capaces de borrar un VPH sin secuelas, pero esto es menos probable que al aumentar la edad de detección. La citología es una prueba muy eficaz para el cáncer cervical y las lesiones precancerosas que se ha utilizado desde mediados del siglo 20, mucho antes de que el vínculo con el VPH fue descubierto. Hasta hace poco, era la prueba de selección sólo está disponible para la displasia cervical. En febrero de 2003, los EE.UU. Food and Drug Administration aprobó el VPH y la prueba de ADN que podrían ser utilizados con la citología del cuello uterino para detectar las mujeres con riesgo de cáncer cervical y lesiones precancerosas. Más de 100 subtipos de VPH en la actualidad se han identificado, y más de 40 de estos subtipos se pueden encontrar en el cuello del útero o la vagina. La técnica de análisis de ADN del VPH detecta varios subtipos que se encuentran en el cáncer de cuello uterino. Sobre la base de la evidencia disponible, el Instituto Nacional del Cáncer, la Sociedad Americana de Colposcopia y Patología Cervical, y la AEC determinó que las mujeres de 30 años o más pueden ser examinados con tanto tamizaje cervical y la prueba de ADN del VPH al mismo tiempo. Las mujeres, por los cuales ambas pruebas resultan ser negativos, tienen un riesgo de neoplasia cervical intraepitelial 2 ó 3 que es de aproximadamente 1 de cada 1.000 (3) . Por lo tanto, recomendó que se re-examinados con más frecuencia de cada 3 años. Las mujeres con citología negativa, pero positiva VPH de alto riesgo deberían hacerse ambas pruebas nuevamente en 6-12 meses. Aquellos con citología anormal o persistente por VPH de alto riesgo deben someterse a una colposcopia. Para las mujeres menores de 30 años, la prevalencia del VPH es muy alta, aunque el riesgo de cáncer de cuello uterino es muy baja, por lo tanto la detección de VPH en las mujeres menores de 30 años daría lugar a pruebas adicionales innecesarios, tales como la colposcopia o repetir la detección cervical, con pocos hallazgos de importancia. La recomendación actual es realizar cribado cervical con reflejo de la prueba del VPH para detectar el VPH sólo con un frotis cervical que muestra células escamosas atípicas de significado socavado (ASCUS) (4) . En un bien organizado programa de cribado del cáncer de cuello uterino, la prueba de VPH es más sensible que la citología convencional para la detección de lesiones CIN 3 y el cáncer (5) . En este ensayo grande, aleatorio de Finlandia, la prueba de VPH como la eficacia del funcionamiento de la pantalla principal de cáncer cervical y fue más sensible que la citología convencional para la detección de neoplasia cervical intraepitelial grado 3 (NIC 3) o más. Las mayores fortalezas de este estudio son la aleatorización 1:1 de poco más de 58.000 mujeres y la capacidad de vincular los participantes del estudio a los resultados, durante un período de 5 años, utilizando la base de datos integral de la población finlandesa y registro de cáncer. Una de las preocupaciones que los médicos pueden tener es si los hallazgos son aplicables a una población de EE.UU. que ahora rara vez examinados utilizando la citología convencional (citología de base líquida es la norma). Esa preocupación debe ser disipado por un meta-análisis que no encontró diferencias en la sensibilidad de la citología basada en líquido en comparación con la prueba de Papanicolau convencionales (6) . A pesar de su gran tamaño, el estudio había limitado poder estadístico para mostrar el impacto de las dos modalidades de detección de la tasa de cáncer de cuello uterino, debido principalmente a que la tasa es tan baja en la población estudiada. Para determinar estos efectos, las opciones de detección que sea necesario repetir para otra ronda, con un seguimiento prolongado a 10 años. Aplicación clínica de la prueba de VPHCotesting es la norma: EE.UU. directrices de la ACS (2002) y ACOG (2003, 2009) los médicos ofrecen la opción de detección de las mujeres mayores de 30 años y con tanto la citología y la prueba de VPH - un enfoque conocido como "cotesting". Sin embargo, a pesar de que alrededor del 90% de las mujeres que tienen una respuesta negativa a ambas pruebas con seguridad puede renunciar a hacer más pruebas por lo menos 3 años, muchos médicos les pantalla con mayor frecuencia con cotesting, disminuyendo el costo-efectividad de esta opción (7) . Se recomienda: que siga las directrices actuales de EE.UU. y las mujeres de pantalla 30 años de edad con ambos las pruebas de Papanicolaou y del VPH y extender el intervalo de detección a 3 años para las mujeres que tienen resultados negativos en ambas pruebas. Numerosos estudios apoyan la conclusión de que la abrumadora prueba de VPH en la detección primaria del cáncer de cuello uterino aumenta significativamente la detección de CIN 3 o superior y debe reducir el riesgo posterior de la mujer de desarrollar cáncer cervical. Hay dos criterios principales para decidir si triaje VPH basado es clínicamente útil. En primer lugar, hace la prueba de triaje (prueba de VPH) identificar una proporción importante de mujeres que necesitan o no necesitan remisión a colposcopia caro y procedimientos de biopsia que justifican el costo de la prueba de triaje? Es decir, si la prueba de VPH es casi siempre negativo o positivo, hay poco valor en uso. Como ejemplo de esto último, el brazo de la prueba del VPH para las mujeres que se refiere a la-LSIL Triage estudio ASCUS (ALTS) con citología LSIL se interrumpió antes de terminar porque la mayoría de pruebas del VPH positivo (8) . El segundo criterio es, si las mujeres VPH-negativas pueden ser seguidos de forma segura en lugar de enviarse a la colposcopia. Según estos criterios, el VPH triaje de mujeres de 45 años y más o mayores de 50 años con LSIL puede ser racional debido a la menor porcentaje de los positivos de VPH (menos del 80%) están en el riesgo muy bajo de CIN3 y el cáncer entre los VPH mujeres con resultado negativo. Esto se observa en un ensayo clínico grande en Europa (9) . La discrepancia entre las observaciones y ALTS es que ALTS inscritos predominantemente mujeres jóvenes (edad media 24 años) (8) . prueba de VPH puede ser útil para la selección de remisión colposcópico para la citología LSIL en mujeres mayores, pero no para la citología ASC-H a cualquier edad (11) . resultados de la prueba del VPH para las mujeres con citología AGC no puede ser de utilidad para la selección, pero puede servir de guía a los médicos que su localización anatómica, cuello del útero o endometrio, puede haber un problema: las mujeres con citología AGC que prueba de VPH positivos excepcionales alto riesgo de lesiones precancerosas de cuello uterino y el cáncer mientras que los que la prueba del VPH negativos tienen un alto riesgo de cáncer de endometrio (10) . la prueba del VPH será cada vez más importante para distinguir a las mujeres en alto y bajo riesgo de las lesiones precancerosas de cuello uterino y el cáncer entre las mujeres vacunadas contra el VPH con la citología equívoca y ligeramente anormales. En la población HPV16/18-vaccinated, este estudio (11) observó menor número de interpretaciones de la citología HSIL y menos enfermedades asociadas a ningún resultado citológico anormal porque HPV16 preferentemente causas HSIL citología y VPH 16 y 18 de dos genotipos de VPH más cancerígenos. Protección parcial de vacunas contra el VPH contra los genotipos del VPH siguiente más cancerígenos, especialmente VPH31 y VPH45, puede reducir aún más la aparición de la citología HSIL. Por lo tanto, habrá un cambio profundo hacia la citología equívocos en las poblaciones vacunadas contra el VPH-. Marcadores moleculares de la displasia cervicalla evolución de la investigación en la patogenia molecular del cáncer de cuello uterino se han centrado en el desarrollo de marcadores moleculares para la detección del cáncer de cuello uterino. En concreto, la amplificación del cromosoma 3q brazo se ha demostrado en los carcinomas del cuello uterino y también se ha observado en otros tumores (12) . hibridación genómica comparativa (CGH) con muestras de archivo demostrado que la amplificación de ADN en el cromosoma 3 (región 3q24 3q28 a) se asoció con la carcinogénesis cervical. Se determinó posteriormente que una sonda de orientación para el componente de secuencias de ARN del gen de la telomerasa humana (TERC), localizado en región del cromosoma 3q26, podría utilizarse como una prueba de detección para la amplificación 3q y podría ayudar a evaluar la progresión de una lesión individual (13) . Se presume que debido a que un alto porcentaje de lesiones displásicas tener copias extra del gen TERC, TERC/3q puede tener un papel causal, aún no comprobadas, en la displasia a través de la inmortalización de células telomerasa-basada. Además, otros genes localizados en la región 3q26, como PIK3CA, que codifica una subunidad catalítica de la fosfatidilinositol 3-quinasa y se asocia con una serie de funciones relacionadas con el cáncer, incluyendo la apoptosis y el crecimiento celular, tienen la posibilidad de participar como el cáncer de cuello uterino oncogenes. Investigación que examina la asociación de 3q ganancia con la carcinogénesis cervical desplazado a la investigación de la posibilidad de que el aumento de 3q puede predecir la progresión de la enfermedad cervical. Este estudio (14) demostró que, si bien 3q ganar la progresión prevista en el 100% de los casos (CIN 1 / 2 avanza a CIN3), la ausencia de 3q ganancia fue también capaz de predecir el 70% de regresividad. Otra investigación demostró que biomarcador como 3q (3q26) están temporalmente asociados a la integración del VPH en el genoma del huésped (12) . Por lo tanto, una prueba que determina 3q estado debe ser de utilidad en el triage de los pacientes LSIL. Hasta hace poco, las pruebas de rutina para obtener 3q no era factible porque la evaluación requiere el análisis de un gran número (800) de los núcleos teñidos, de células escamosas, que es poco práctico por microscopía convencional. Sin embargo, el FISH onco cervical ® es una prueba cualitativa de fluorescencia de hibridación in situ (FISH) para determinar la adquisición de determinadas aneuploidías cromosómicas (en la región 3q26) en muestras citológicas. PESCADO onco se lleva a cabo en la citología cérvico-vaginal ejemplares, idénticos a los utilizados en el del Papanicolaou y la prueba de VPH. La prueba evalúa la amplificación de la región 3q26 por el uso de dos sondas de FISH, uno para el locus 3q26 y una sonda de control. Enumeración y la comparación de las sondas 3q26 y control, en relación con la morfología nuclear, el resultado en un número de copias 3q para cada uno de los núcleos analizados. Aunque varios factores contribuyen a la progresión de una lesión precancerosa a la malignidad, la ganancia de 3q26 es un marcador que el profesional médico puede usar, junto con otras pruebas, a la gestión de la ayuda LSIL paciente. 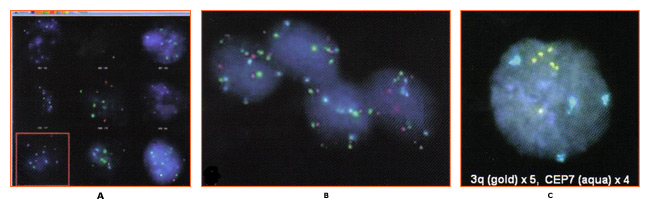 Figura 1: A. digitalizadas información de la célula y los datos para obtener 3q, la muestra: PESCADOS oncológica de cuello uterino, B. de la célula se detectan utilizando microscopia de luz transmitida y reflejada, 3q C. Resultado positivo para 3q ganancia (más de 2 núcleos con ganancia de> copias de ). Fotografías cortesía de Ikonisys Inc. La identificación de una relación entre el aumento en el cromosoma 3q26 región y el desarrollo de la displasia cervical es el resultado de una serie de estudios que confirmen la asociación y sugiere la posible utilidad clínica de esta observación. Sin embargo, la aplicación del análisis a base de pescado de muestras de citología líquida para obtener 3q en un entorno clínico es un reto. Tamizaje de todas las células presentes en la muestra de sus señales FISH es poco práctica mediante el análisis de microscopía tradicional. La naturaleza automatizada de la prueba permite un enfoque global de la muestra de análisis que no es posible de forma manual. Análisis de muestras de LSIL identifica hasta 20% de las muestras que presentan un nivel de 3q ganancia por encima de la observada en las muestras normales (29) . Un método completamente automatizado para la determinación de 3q ganancia en citología líquida puede ser la prueba necesaria para aplicar las pruebas de rutina (29) . Los estudios adicionales para validar la utilidad de esta tecnología son necesarios. Otros estudios con esta prueba basada en la presencia de células con más de cinco 3q26 señales FISH, permitirá una mejor evaluación de su desempeño clínico y su utilidad potencial, junto con las pruebas existentes, para el manejo de los pacientes. La detección de 3q ganancia en una muestra de LSIL archivo 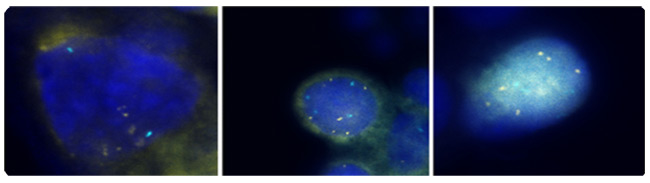 Figura 2: 3q fluorescencia de hibridación in situ (FISH) las señales son de color oro y el control centromérica 7 señales FISH, son de color aguamarina. Todas las tres células presentan más de 4 3q (oro) señales de FISH. Fotografías cortesía de Ikonisys Inc. Aplicación clínica de FISH onco cervical pruebaPESCADO onco cervical proporciona a los médicos información adicional que puede ayudarles a tomar decisiones informadas de manejo clínico más. ¿Qué LSIL progresará clínicamente en un grado superior? ¿Qué va a regresar a la normalidad? Aproximadamente el 10% de los pacientes diagnosticados con LSIL pasará a HSIL, el 60% va a regresar a la normalidad, y el 30% seguirá siendo LSIL (15) . PESCADO onco cervical ayuda a los médicos evaluar qué pacientes LSIL puede retroceder y sugieren casos de LSIL en mayor riesgo de enfermedad progresión. Entre los muchos cambios cromosómicos observados en el cáncer de cuello uterino, la alteración más consistente es detectado en el brazo del cromosoma 3q. Los estudios han demostrado que al menos el 90% de los casos de cáncer invasivo de cuello uterino tiene una ganancia en el brazo 3q (14) . La investigación adicional ha demostrado una correlación entre el aumento en el número de copias 3q26 como la severidad y el estado de progreso de la enfermedad del cuello uterino (13)(14) . Usando esta tecnología para ver la evolución de cada paciente, se ha demostrado que la sensibilidad de los loci 3q26 para predecir la progresión de CIN1/CIN2 a CIN3 fue del 100% y la especificidad, es decir, la predicción de la regresión fue del 70% (14) . PESCADO onco cervical proporciona información para la evaluación clínica de displasia antes de la colposcopia.  Figura 3: A. Un esquema de regresión que indica LSIL o progresión. obtener B. 3q puede ayudar en la categorización de los pacientes con diagnóstico previo de LSIL en la estratificación del riesgo. WNL, dentro de los límites normales; NILM, negativo para lesión intraepitelial o malignidad. Fotografía cortesía de Ikonisys Inc. Cuello del útero Zona de Transformación (TZ)Cancerígenos las infecciones por VPH son particularmente propensos a causar cáncer en las zonas de transformación (TZS) en dos tipos de epitelio se encuentran, por ejemplo, el cuello uterino, ano y orofaringe (16) . La zona de transformación (ZT) se define como la zona comprendida entre la unión escamoso original y la unión escamoso-colposcópico nuevo. La unión original lineal entre el epitelio escamoso y columnar se sustituye por una zona de metaplasia escamosa en diferentes grados de maduración. En el margen superior o craneal de esta zona es una clara demarcación entre el epitelio, que parece morfológicamente escamosas con la iluminación de un colposcopio magnifica, y el epitelio eritematosas, velloso, que aparece colposcopia columnar. Esta unión colposcópico se llama la unión escamoso nuevo. La evaluación clínica inicial para la mayoría de las mujeres es en la pubertad año post. Epitelio escamoso metaplásico maduro a menudo ha sustituido el límite distal o caudal del epitelio cilíndrico. La unión escamoso original se observa con mayor frecuencia en la clínica como una unión escamoso original que separa el epitelio escamoso y metaplásico. En la zona de transformación madura, este cruce se hace imposible de definir. Sólo la presencia de los folículos de Naboth y sugerencias orificios de las glándulas en el origen columnas originales de la metaplasia escamosa madura. neoplasia cervical casi siempre se origina en el TZ. Entender metaplasia escamosa es la clave para entender los conceptos de las vértebras cervicales TZ y la carcinogénesis cervical. Si la unión escamoso nuevo se ve en su totalidad en la ausencia de enfermedad premaligna, la incidencia de la enfermedad escamosa por encima o craneal a la unión escamoso nuevo es prácticamente nulo. Así, si la unión escamoso nuevo se ve en su totalidad, el examen colposcópico del cuello uterino se describe como satisfactoria. Si la unión escamoso nueva no se ve todos sus elementos, la colposcopia es descrito como insatisfactoria. La zona de transformación más define el límite distal del alto grado de neoplasia intraepitelial glandular, la lesión precursora del adenocarcinoma invasor del cuello uterino. Aunque las infecciones por VPH son muy comunes en los sitios de genitales como la vagina, el pene y la vulva, las tasas de cáncer inducido por el VPH son mucho más bajos debido a la falta de TZS. metaplasia escamosa continúa durante toda la vida de una mujer, y finalmente, el TZ se encuentra dentro del orificio interno. Por lo tanto, es fundamental para probar el TZ en la selección, sino una muestra centrada en el sistema operativo no siempre recogen las células óptima. La atrofia puede reducir los rendimientos de la célula también. Hay esperanza de que la prueba del VPH incluyendo las células endocervicales puede reducir de detección de falsos negativos en comparación con la citología. Sin embargo, el método de detección se utiliza lo que sea, sigue siendo un problema de diagnóstico, incluso cuando se realiza correctamente, colposcopistas no son fáciles de diagnosticar lesiones en el poco visibles TZ entre las mujeres posmenopáusicas. 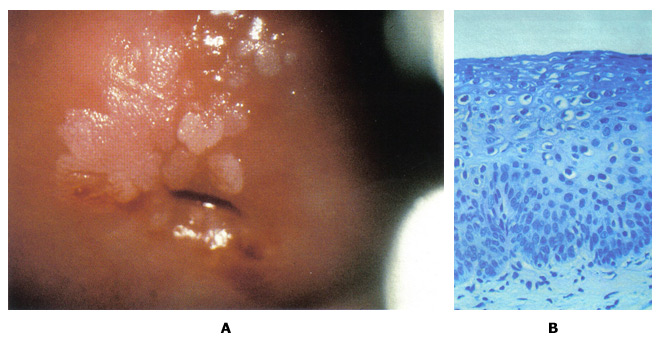 Figura 5: A. fotografía colposcópico del cuello uterino después de la aplicación del ácido acético que demuestran numerosas lesiones acetoblancas consistente con un bajo grado de lesión intraepitelial escamosa (SIL). B. Los hallazgos histológicos muestran la pérdida de la polaridad en el tercio inferior del epitelio y coilocitos numerosas, de acuerdo con neoplasia intraepitelial cervical de grado 1, con las características del VPH. Citología e Histología hallazgos e interpretacionesEn el Bethesda Directrices de 2001, ASC es subcategorías en células escamosas atípicas de importantes indeterminado (ASCUS) y células escamosas atípicas no pueden excluir HSIL (ASC-H). La diferencia en las directrices de gestión de estos dos hallazgos citológicos se relaciona con el riesgo inherente de CIN2, 3. ASCUS es la anormalidad más común de la citología de cuello uterino, lo que representa el 4,4% de todos los resultados de la prueba de Papanicolau. Aunque el riesgo de cáncer para cualquier paciente individual es muy baja (0,1 a 0.02%) (19) , y el riesgo de CIN2, 3 + también es baja (6.4 a 11.9%) (22) , porque hay muchas personas para con esta anomalía la citología, es el resultado de la citología para la presentación de aproximadamente la mitad de las mujeres con CIN2, 3. El primer paso en la evaluación de las mujeres con ASCUS es clasificar aquellos que están en mayor riesgo para una evaluación más intensiva (colposcopia) y la dirección de la prueba a más de seguimiento de rutina. prueba de triaje se puede realizar por una sola prueba de alto riesgo (oncogénicos) los tipos de VPH o por detección repetir la citología a los 6 meses y 12 meses. Cuando el índice de la citología muestra de ensayo se obtiene con sede en la citología líquida o cuando un ejemplar del VPH es co-recogidos, "refleja" la prueba del VPH es el método preferido (17) . Los datos de ALTS demostrado que dos exámenes de citología a los 6 meses y 12 meses en un umbral de ASCUS detecta el 88% del CIN2, 3 mientras que refiere el 63,6% de las mujeres a una colposcopia. prueba de VPH detecta solo 92,2% de la CIN2, 3 +, al referirse al 55% de las mujeres a una colposcopia. Gestión de la citología cervical normal con el VPH positivos de la prueba:El enfoque de gestión mejor para el VPH-positivo, negativo mujeres citología 30 años y más es repetir la citología y la prueba de VPH a los 12 meses (17) . Las mujeres cuyos VPH resultado sigue siendo positivo en pruebas repetidas a los 12 meses o cuyo resultado es la citología ASC o mayor deben someterse a una colposcopia, mientras que las mujeres cuyos resultados son negativos en ambas pruebas puede diferir de detección de 3 años. La incorporación de la prueba del VPH en la detección de rutina se debe reservar para las mujeres de 30 años y más (22) . En la investigación de los estudios de América del Norte y Europa, la sensibilidad mediante una combinación de pruebas de VPH y citología es significativamente mayor que la de cualquiera de las pruebas a solas con valor predictivo negativo del 99-100% (22) . Las mujeres que reciben los resultados negativos de ambos citología inicial y las pruebas de VPH tienen menos de 1 de cada 1.000 pacientes de riesgo de tener CIN2 o superior, y futuros estudios de seguimiento en Europa y los Estados Unidos han demostrado que el riesgo de CIN3 en desarrollo más de un 10 años del período es inferior al 2% (22)(23) . Los estudios de simulación demuestran que en mujeres de 30 años y mayores, los controles a intervalos de 3 años utilizando una combinación de citología y la prueba del VPH proporciona beneficios equivalentes o mayores que las previstas por revisión anual con la citología convencional. Incluso en mujeres de 30 años de edad, la mayoría de las mujeres VPH-positivo se VPH negativos durante el seguimiento (60% en un estudio prospectivo) (22) . En una población bien-seleccionados, el riesgo de CIN2 + en el VPH-positivo, negativo mujeres gama citología del 2,4% al 5,1% (23) . Gestión de la citología cervical ASCUS y LSIL en Adolescentes (antes de los 21 años):El cáncer invasivo de cuello uterino es muy poco frecuente en las adolescentes antes de los 21 años. Instituto Nacional del Cáncer SEER El programa informó que entre 1995 y 1999, la tasa de incidencia de cáncer invasivo del cuello uterino fue de 0 por cada 100.000 al año para las mujeres de 10-19 años y 1,7 por cada 100.000 al año para las mujeres de 20-24 años (1) . Debido a que la tasa de infección por el VPH ADN o positividad es mayor en la población adolescente, y porque la mayoría de las infecciones por VPH en adolescentes con o sin citología anormal se resuelven sin tratamiento, las directrices actuales no recomiendan el uso de las pruebas de VPH en la población bajo ninguna circunstancia , incluyendo triaje de ASCUS y el seguimiento de LSIL (17)(18). El ASCCP 2.006 guías de consenso para la gestión del ASCUS y LSIL en adolescentes (20 años y menores) recomiendan repetir la citología a intervalos de 12 meses por un período de 2 años. Si ASCUS o LSIL persistir por un período de 2 años, los médicos se les recomienda realizar una colposcopia (17) . Esta recomendación representa un cambio significativo de las pautas anteriores y se basa en estudios de historia natural de ASCUS y LSIL que demuestran una alta tasa de resolución de la enfermedad dentro de 2-3 años (18) . La evolución clínica muy similar de mujeres jóvenes con ASCUS y LSIL ASCCP ha llevado a recomendar un enfoque de gestión similares para ambos diagnósticos. Suponiendo que CIN2 o mayor ha sido descartada por trabajos prospectivos colposcopia de una población adulta con CIN1 demostrar que el riesgo de CIN2 o superior en desarrollo de todo un período de 2 años es de aproximadamente 10% (19) . En población adolescente, la tasa de progresión es mucho más baja, estimada en 3%, mientras que la tasa de resolución de CIN1 es extremadamente alta (superior al 90%) (18)(19). Por lo tanto, la gestión inicial de CIN1 sin tratamiento es obligatorio. Consideraciones especiales: menores de edad sometidos a un examen colposcópico puede resultar útil contar con la participación de los padres para el procedimiento. Sin embargo, los exámenes colposcópicos se consideran la evaluación de las enfermedades de transmisión sexual (ETS), y los menores son por lo general se les permite dar su consentimiento para el diagnóstico para el diagnóstico y tratamiento de enfermedades de transmisión sexual. Por esa razón, el consentimiento paterno, aunque prefiere, no se debe exigir. Si consentimiento de los padres no se obtiene el consentimiento para el examen se debe obtener de menores y se indica en el expediente médico. Cualquier proveedor de cuidado de la salud que ofrece esa atención debe estar plenamente informados de sus leyes estatales y locales norma establecida de la atención. Gestión de ASCUS y LSIL citología cervical en el embarazo:El embarazo en adolescentes no altera la detección y gestión de la citología anormal. y curetaje endocervical escisión procedimientos nunca debe realizarse durante el embarazo a menos que el cáncer invasor es altamente sospechosos (20) . La detección de embarazo, por lo tanto, se debe realizar antes de la evaluación y la gestión de la citología cervical anormal en adolescentes. En el embarazo, el único diagnóstico que pueden alterar la gestión es el cáncer invasivo. La presencia de cáncer pueden cambiar los objetivos del tratamiento o cambia la ruta y el calendario de entrega. Por lo tanto, el examen de colposcopia durante el embarazo debe tener como objetivo principal la exclusión de cáncer invasor. Gestión de LSIL y resultados ASCUS VPH-positivas durante el embarazo debe ser el mismo que en el estado no embarazadas, aunque la evaluación de estas condiciones puede aplazarse hasta después del parto. Gestión de la citología cervical ASCUS y LSIL con HPV-positivos (pacientes mayores de 21 años):Aunque un resultado de la citología de LSIL se cree que reflejan los efectos citopáticos de infección por VPH en lugar de una lesión premaligna cierto, las mujeres con LSIL permanecen en riesgo moderado de tener CIN2 +. En ALTS, el 27,6% de las mujeres con LSIL tenían CIN2 + ya sea en las biopsias dirigidas por colposcopia o en un estrecho seguimiento en los próximos dos años (19) . Esta tasa es prácticamente idéntica a la tasa de CIN2 + en las mujeres que se presentaron con resultados ASCUS VPH-positivas en la misma población (26,7%). Muchos estudios han demostrado que la prevalencia de la positividad del ADN del VPH y el CIN2, 3 disminuye con la edad en las mujeres con LSIL (19) . Bien revisadas, las mujeres posmenopáusicas con resultados negativos anteriormente son también de bajo riesgo para el cáncer invasor del cuello uterino. Esto sugiere que las mujeres posmenopáusicas con LSIL puede gestionarse a través de la prueba del VPH para la selección en el mismo protocolo que se utiliza en mujeres en edad reproductiva con ASCUS. La presencia de ASCUS es menos común en las mujeres posmenopáusicas, como es el riesgo de resultados patológicos significativos. Tasas de positividad de ADN del VPH también disminuyen drásticamente con la edad. Esto significa que la prueba de VPH cada año es más eficaz en las mujeres mayores porque se refiere una menor prevalencia de CIN2, 3 es mucho mayor entre las mujeres con ASC-H que las mujeres con ASCUS, por lo que ASC-H se debe considerar que representan HSIL equívocos. Seguimiento después de la evaluación colposcópica de ASCUS, ASC-H, o LSIL sin CIN2, 3: En ALTS, la colposcopia inicial identificó sólo el 58% de las lesiones CIN2 +. Para las mujeres no se constató que CIN2 + en la colposcopia inicial, la tasa de CIN2 + durante el seguimiento (aproximadamente 10-13%) no se vio afectada por los hallazgos en la colposcopia (resultados negativos no es digno de la biopsia, biopsia negativa o una biopsia CIN1). El ALTS evaluado diferentes colposcopia mensaje estrategias de seguimiento y se encontró que la prueba de VPH realizado 12 meses después de la colposcopia inicial y dos exámenes de citología a cabo en intervalos de 6 meses son igualmente efectivos (19) . Debido a los costes adicionales y la falta de aumento de la sensibilidad, la estrategia de la citología combinada además la prueba de VPH no se recomienda. En ausencia de CIN en la histología, diagnóstico por escisión o procedimientos ablativos son inaceptables para el tratamiento inicial de pacientes con LSIL. Seguimiento, ya sea con la prueba de VPH a los 12 meses o citología cervical a los 6 meses y 12 meses (umbral de ASCUS) es aceptable. Si el resultado de la prueba de ADN del VPH es negativo o si dos consecutivos repetir los resultados del examen de citología es negativa, volver a exámenes de rutina se recomienda. Si bien el resultado de la prueba de ADN del VPH es positivo o si el resultado de la citología es reportada como ASCUS o mayor, se recomienda la colposcopia (24) . Gestión de la citología cervical ASC-H:La prevalencia de CIN2, 3 es mucho mayor entre las mujeres con ASC-H que las mujeres con ASCUS, por lo que ASC-H se debe considerar que representan HSIL equívocos. Las mujeres con células escamosas atípicas no pueden excluir HSIL (ASC-H) tienen un riesgo del 20-50% de tener un CIN2, 3 y lesiones deben ser evaluadas con colposcopia inmediata. La mayoría de las mujeres con ASC-H son el ADN del VPH positivo (entre 67-84%) (21) , intermedio triaje lo que es inadecuado y la prueba del VPH no se recomienda. Si CIN2, 3 no es identificado por colposcopía, las mujeres mayores de 21 años y mayores deben ser controlados de una manera similar a las mujeres VPH positivas con ASCUS. Gestión de CIN1 Precedido por HSIL y AGC, de lo contrario no específica (NOS):De cualquier procedimiento de diagnóstico por escisión o la observación con colposcopia y citología cada 6 meses durante 1 año es aceptable para las mujeres mayores de 21 años con un diagnóstico histológico de CIN1 precedida de una HSIL o resultado de la citología AGC-NOS, siempre en el último caso que el examen de colposcopia es satisfactoria y toma de muestras endocervical es negativo. Un procedimiento de escisión de diagnóstico se recomienda para las mujeres con CIN1 precedida de una HSIL o los resultados de la citología AGC-NOS en los que el examen de colposcopia no es satisfactoria, excepto en el embarazo. El riesgo de CIN2 sin ser detectados, 3 o adenocarcinoma in situ (AIS), la lesión se espera que sea mayor en las mujeres con CIN1 precedida de una HSIL o resultado de la citología AGC que en las mujeres con CIN1 precedida de una ASC o resultado de la citología de LSIL. neoplasia intraepitelial cervical de grado 2,3 se identifica en el 84-97% de las mujeres con citología HSIL evaluados con una escisión con asa grande de la zona de transformación (LLETZ) (26) . Por lo tanto, las recomendaciones se hacen por separado para CIN precedida de HSIL o citología AGC. La integración de la vacunación contra el VPH y de proyección:En un mundo de recursos de salud limitados, vacunación contra el VPH y el cribado están compitiendo por la atención y los recursos. Como ha demostrado grandes ensayos aleatorios, las dos vacunas contra VPH licenciadas son muy eficaces en la prevención de nuevas infecciones con el VPH 16 y 18 (25) . Es posible que haya algún tipo de protección cruzada contra posibles VPH 31 y VPH45. La minoría de los cánceres se deben a otros tipos de VPH no están cubiertas. Las vacunas actuales no tratan las infecciones existentes o lesiones (25) . Se les debe dar antes de la exposición, en los programas de salud pública que esto implica que la vacunación de las adolescentes jóvenes es óptimo. No es responsable de combinar la vacunación contra el VPH y el cribado sin integración. La duración de la eficacia probada de la vacuna VPH profiláctica contra el VPH 16 y VPH-18 se aproxima ahora a una década y la cobertura de vacunación en aumento. Por lo tanto, la vacunación de los adolescentes en gran medida evitará que el primer paso en la carcinogénesis del cuello uterino (la infección por VPH aguda en los años posteriores a la iniciación de las relaciones sexuales), especialmente en nuevas vacunas en fase de evaluación final de abarcar más tipos de VPH. La eficacia de todas las pruebas de tamizaje cervical disminuirá debido a la reducción en la prevalencia de lesiones precancerosas (27) . La vacunación, especialmente a reducir la eficiencia de detección basados en la citología, porque las lesiones que siguen siendo cada vez se molesta parecidos (en particular ASCUS) no son causadas por los tipos de VPH cancerígenos y no corren el riesgo de progresión hacia el cáncer (28) . Por lo tanto, las diversas propuestas se encuentran bajo consideración, incluyendo un retraso de la detección inicial en vacunados mujeres jóvenes y un cambio en el énfasis de la citología a la educación primaria la prueba de VPH. Resumen de las recomendaciones:Las siguientes recomendaciones se basan en la evidencia científica consistente y de buena y opiniones de expertos para el manejo clínico de pacientes con citología cervical anormal (15)(17) :
Resumenla prevención del cáncer cervicouterino ahora se puede hacer aún mejor. Las modificaciones sustanciales de la práctica son próximas, motivado por una mejor comprensión de la historia natural del VPH y la carcinogénesis cervical. La mayoría de los programas de cuello uterino en el 2010 todavía se basan en la citología cervical, seguido por el diagnóstico de cribado anomalías detectadas mediante biopsia colposcópica. La sensibilidad combinada de citología y la prueba del VPH es muy similar a la prueba del VPH. Esto indica que la prueba del VPH con el tiempo podría ser utilizado como un análisis de la investigación principal y único seguido por citología o prueba de nuevos biomarcadores como un triaje para ser utilizado sólo para las mujeres VPH positivas. La detección del aumento de 3q y la amplificación de TERC en recolectada de forma rutinaria pruebas de Papanicolau pueden ayudar en la identificación de lesiones de bajo grado con un alto riesgo de progresión y en la disminución de cribado citológico de falsos negativos. El reto fundamental es repensar nuestro modelo de prevención actuales basados en la citología frecuentes y referencias colposcópico. Inevitablemente, los programas de futuro dependerá de la vacunación, mucho menos frecuentes y menos tratamientos para permitir la liquidación de la resolución de las infecciones por VPH. Reconocimiento: Salud de la Mujer y el Centro de Educación (WHEC) gracias Dr. Robert J. Walat, Director de Laboratorio Clínico, Ikonisys Inc. de New Haven, Connecticut (EE.UU.) para obtener valiosas sugerencias muy, opiniones de expertos y la asistencia con la serie sobre la prevención del cáncer cervicouterino. Recursos
Financiación: La serie sobre la prevención del cáncer de cuello del útero fue financiado por WHEC Iniciativas para la Salud Global. Este programa se lleva a cabo con los interlocutores de la Salud de la Mujer y el Centro de Educación (WHEC) para eliminar o reducir el cáncer de cuello uterino en todo el mundo. Póngase en contacto con nosotros si usted desea contribuir y / o sumarse a los esfuerzos. Referencias:
|