سرطان الثدي تقييم المخاطر[وهك] ممارسة نشرة وسريرية إدارة لمقدمي الرعاية الصحية. قدمت منحة للتربية وصحة المرأة وتربية مركز ([وهك]). سرطان الثدي البيولوجيا هو موضوع البحث المكثف ، وكانت هناك اختراقات كبيرة في السنوات الأخيرة. وقد أدى العلم نظرة ثاقبة البيولوجيا مستقبلات هرمون الاستروجين إلى تقدم كبير في مجال الوقاية من الاستروجين التي تستهدف والعلاج الكيميائي. وقد برزت زيادة كثافة الثدي كعامل خطر المهيمنة ، للكشف ، وتعديل لتطور لاحق من سرطان الثدي في النساء. ويمكن تحديد العوامل التي تزيد من خطر اصابة النساء أكثر نضجا للسرطان ، مثل كثافة الثدي ، في منتصف العمر. تقنيات التصوير محسن ، مثل تصوير الثدي الرقمي والتصوير بالرنين المغناطيسي ، يمكن نشرها على نحو فعال في مجموعة صغيرة من النساء المعرضة للخطر من أجل التوصل إلى نسبة أكثر توازنا وأكثر من مناسبة ، ليس فقط الفعالية من حيث التكلفة ولكن أيضا للاستفادة ضرر. فمن الحكمة عدم الاعتماد على تصوير الثدي الى "حل" المشكلة للكشف المبكر عن سرطان الثدي. سرطان الثدي تقييم المخاطر هو الجانب الروتيني للرعاية الصحية للمرأة ، و 3 نماذج متوفرة لمساعدة الأطباء في هذه المهمة : غيل ، كلاوس ، وتايرير Cuzick. أداة رابعة -- وشائعة بشكل متزايد والاختبارات الجينية ، التي يمكن أن تكون جزءا هاما من تقييم المخاطر الجينية لبعض الأفراد. النماذج المتاحة للأطباء لتقييم مخاطر تعرض الشخص لسرطان الثدي يمكن ان تنتج على نطاق واسع تقديرات متفاوتة ، والأطباء ويجب أن يفهم كل القيود المفروضة على نموذج لاختيار النموذج الانسب لمرضاهم. والغرض من هذه الوثيقة هو لمناقشة تطبيق السريرية لمختلف الأدوات المتاحة لتقييم المخاطر المرأة لسرطان الثدي وتطبيقها في الممارسة السريرية. ويقدم هذا الاستعراض أيضا إجراء فحص شامل لأهمية كثافة الثدي كعامل خطر المهيمنة لتطوير سرطان الثدي ، وتسليط الضوء على الدور الذي تؤديه الوراثة والهرمونات في الحفاظ على كثافة الثدي لدى النساء بعد انقطاع الطمث. ويمكن توجيه البحوث المستقبلية نحو الكشف عن الظروف الموجودة مسبقا (مثل طفرات الجينات) التي تعرض المرأة لخطر الإصابة بسرطانات شديدة العدوانية. واستعرض توصيات لاختبار الوراثية هنا ، مع التركيز بشكل خاص على مكونات المشورة الوراثية وتحديد هوية الأفراد للاختبار ، وتفسير نتائج الاختبار. خلفية :خطر الاصابة بسرطان الثدي مدى الحياة للمرأة في المتوسط ما يقرب من 12 ٪ (1) . عوامل الخطر لسرطان الثدي وصفا جيدا. ومعلوم ان استخدام هرمونات خارجية (الاستروجين والبروجسترون) لزيادة المخاطر ، وترتبط العوامل الهرمونية الذاتية مثل الأعمار في الحيض ، وانقطاع الطمث ، والولادة في المركز الأول بمعدل طفيف ، لكنه مهم ، وزيادة في مخاطر الاصابة بسرطان الثدي. العوامل البيئية ، مثل النظام الغذائي وتعاطي الكحول ، وإن لم تكن مفهومة تماما ، كما ترتبط مع خطر الاصابة بسرطان الثدي. وقد كان لخزعة الثدي ، وخصوصا أن خزعة أظهرت تضخم غير نمطية أو الأورام مفصص ، ويرتبط خطر كبير من الاصابة بسرطان الثدي (2) . وهناك تاريخ عائلي إيجابي من السرطان كما تشير عنصر وراثي لمخاطر الشخص. وأدرجت العديد من هذه العوامل في النماذج التي تناقش أدناه. ويتألف من ثلاثة أنسجة الثدي الرئيسي -- الدهون ، ليفي / النسيج الضام والأنسجة الطلائية. اختلافات في كمية النسبية لهذه الأنسجة نتيجة لتقلب بين الأفراد في مظهر الإشعاعي للثدي على تصوير الثدي. الدهون شعاعيا ويظهر الظلام على تصوير الثدي ، في حين الظهارة والنسيج الضام واللاسلكية الكثيفة ، ويبدو الضوء على تصوير الثدي. كثافة الثدي بالأشعة (مليون برميل يوميا) تعبر عن مظهر من الثدي على الماموجرام ويشير إلى أن نسبة الكثافة النسبية للإشعاعيا ، أي أبيض أو ضوء مناطق الثدي. وزيادة كثافة المرتبطة الثدي مع ارتفاع خطر الإصابة بسرطان الثدي مستقل لزيادة صعوبة قراءة صور الأشعة (3) . النساء البيض وزيادة خطر الاصابة بسرطان الثدي من النساء السود (على الرغم من النساء السوداوات شخصت اصابتهن بسرطان الثدي أكثر عرضة للموت من المرض). وقد تم تحديد عوامل الخطر الأخرى لسرطان الثدي أو المقترحة لكنها لم تدرج في سرطان الثدي أداة تقييم المخاطر لعدة أسباب : لأن أدلة على أن هذه العوامل تسهم في خطر الاصابة بسرطان الثدي ليست قاطعة ، وذلك لأن الباحثين لا يمكن تحديد ما إذا كانت هذه العوامل إضافة معلومات مفيدة إلى عوامل بالفعل في النموذج ، أو لأنه تم بيانات عن عوامل الخطر الأخرى التي لا تتوفر في البيانات المستخدمة لتطوير البحوث في النموذج. عوامل الخطر مثل ما يلي : في سن انقطاع الطمث ، واستخدام حبوب منع الحمل ، وارتفاع مؤشر كتلة الجسم ، واتباع نظام غذائي غني بالدهون والكحول والتعرض للإشعاع ، والملوثات البيئية. نشرت مؤخرا تشير البحوث إلى أن كثافة نسيج الثدي ، ويقاس من تصوير الثدي بالأشعة السينية ، ويمكن إضافة معلومات مفيدة ، ولكن مع نماذج المخاطر قياس كثافة نسيج الثدي لا تزال بحاجة إلى التحقق من صحة مع دراسات مستقلة إضافية (3) . وتشير الأبحاث أيضا إلى أن عوامل الخطر الأخرى ، مثل استخدام العلاج الهرموني ، قد تؤدي إلى تحسين الأداة. مقدمة :احتمال الاصابة بسرطان الثدي وأداة تقييم وضع المرأة في الأمم المتحدة للسكان 35 سنة فأكثر الدول سن (4) . وينبغي ألا تستخدم للنساء مع تشخيص سابقة من سرطان الثدي ، والنساء الذين تعرضوا للإشعاع الثدي لعلاج الأورام اللمفاوية هودجكين ، أو النساء الذين يقيمون في ، أو هاجروا حديثا من والمناطق مع انخفاض خطر الاصابة بسرطان الثدي ، مثل الصين أو اليابان في المناطق الريفية . أساليب أكثر دقة لمخاطر المشروع قد تكون متاحة للمرأة مع تحديد الطفرات نادرة معينة ، مثل التعديلات في سرطان الثدي الجينات BRCA1 و BRCA2. وكان سرطان الثدي تقييم المخاطر أداة المتقدمة وتم التحقق من صحة السكان في تتكون أساسا من النساء البيض غير اللاتينيين. هناك حاجة إلى مزيد من البحوث للتحقق من صحة أو صقل نموذج لغيرها من الجماعات العرقية والإثنية. وسرطان الثدي هو أداة تقييم المخاطر برنامج كمبيوتر تم تطويره من قبل علماء في المعهد القومي للسرطان وجراحة الثدي الوطني مساعد والأمعاء المشروع (NSABP) لمساعدة مقدمي الرعاية الصحية في مناقشة احتمال الاصابة بسرطان الثدي مع مرضاهم من النساء. أداة تسمح للصحة المهنية لمشروع تقدير المرأة فرد من خطر الاصابة بسرطان الثدي خلال فترة 5 سنوات من الوقت وعلى مدى حياتها ويقارن حساب المرأة خطر مع خطر متوسط لامرأة من نفس العمر. أداة للتقييم المخاطر ويمكن الاطلاع على سرطان الثدي في : http://www.cancer.gov/bcrisktool . فهم عوامل الخطر :على الرغم من كل هذه النماذج يوفر قصيرة الأجل وطويلة الأجل للخطر ، واستخدام خطر عمر يسمح المقارنة بين تقديرات المخاطر التي تولدها كل نموذج. وفهم من القيود في كل نموذج يسمح الطبيب لاستخدام أنسب نموذج لتقييم المخاطر وتقديم المشورة للمرأة في حالة معينة. للحصول على معلومات لمساعدة المرضى على فهم مخاطر سرطان زيارة http://understandingrisk.cancer.gov . وهذا الموقع الإلكتروني التفاعلي الخاص مساعدة المرضى على اتخاذ قرارات واعية حول كيفية خفض خطر. نموذج غيل :يتضمن هذا النموذج (5) :
النسبية خطر الإصابة بسرطان الثدي
وبالنسبة للنساء مع 0 أو 1 النسبية المتضررة ، وزيادة المخاطر مع التقدم في السن عند الولادة الحية الأولى. وبالنسبة للنساء مع 2 أو أكثر من أقارب الدرجة الأولى ، ومخاطر الانخفاض مع التقدم في السن عند الولادة الحية الأولى. وهذا النموذج لا يأخذ في الحسبان التاريخ العائلي في غيرهم من الأقارب من أمه وأخته. الأهم من ذلك ، فشل نموذج غيل لحساب تاريخ عائلي أبوي من سرطان الثدي. هذا النموذج يتنبأ خطر الإصابة بسرطان الثدي في 5 سنوات أو متوسط العمر المتوقع. ويمكن استخدام النموذج الجديد لخطر المشروع أكثر من 5 ، 20 ، 10 و 30 سنة فاصلة. وتوقع نموذج جديد للمخاطر من النموذج السابق في نساء مع كثافة عالية الثدي ، والتحليلات السابقة تشير إلى أن النموذج الجديد كان متواضعا أعلى دقة (6) . هناك حاجة لدراسات التحقق المستقل من قبل وينبغي استخدام هذا النموذج لتقديم المشورة ، وقبل إجراء تغيير دائم لسرطان الثدي أداة لتقييم المخاطر. نموذج كلوز :هذه العوامل في تاريخ سرطان الثدي تصل إلى 2 في 1 و / أو من الدرجة الثانية أو أقارب الأم والأب السن التي تم تشخيص هؤلاء الأشخاص مع سرطان الثدي (7) . وتستخدم هذه المعلومات لحساب المخاطر استنادا إلى العصر الحاضر وخطر مدى الحياة. عمر خطر الاصابة بسرطان الثدي على أساس التاريخ العائلي : كلاوس النموذجي (8)
نموذج تايرير - Cuzick :في الوقت الحاضر ، أداة بحث ، ومحاولات لمعالجة أوجه القصور في النماذج السابقة بما في ذلك عن طريق مجموعة متنوعة من عوامل الخطر (9) . نموذج يستخدم العمر ومؤشر كتلة الجسم (مؤشر كتلة الجسم) ، والهرمونات التناسلية العوامل ، أمراض الثدي ، والتاريخ العائلي واسعة النطاق لحساب شخصية خطر الاصابة بسرطان الثدي. أظهرت دراسة واحدة أن هذا النموذج ينتج أعلى نسبة من المتوقع لمراقبة حالات سرطان الثدي من فعل غيل ونماذج كلوز ، مشيرا إلى أن ذلك قد يسفر عن مزيد من التقييم الدقيق للمخاطر (10) . وهذا النموذج لم يتم بعد التحقق من صحة ، ولذا ينبغي أن تستخدم بحذر في عملية إعداد سريرية. وراثي الثدي وسرطان المبيض متلازمةما يقرب من 5 ٪ الى 10 ٪ من سرطان الثدي وراثية و 15 ٪ إلى 20 ٪ من حالات سرطان الثدي يرجح أن يكون العنصر العائلي وينتج عن التفاعل بين الجينات والبيئة (11) . وعلى الرغم BRCA1 و BRCA2 الجينات هي الأكثر شيوعا للفحص ، وأنها ربما لا جينات فقط المتورطين في سرطان الثدي العائلية : في ما يصل الى 70 ٪ من الحالات ، واختبار للشخص في الأسرة الأكثر عرضة لمرض السرطان وراثية تؤدي إلى نتيجة سلبية . الطفرات ترتبط BRCA2 BRCA1 ومع 45 ٪ إلى 85 ٪ من متوسط عمر خطر الاصابة بسرطان الثدي ، مع متوسط عمر 43 سنة من بداية لBRCA1 و 45 سنة للBRCA2 (12) . كلا BRCA2 ترتبط BRCA1 و 50 ٪ مع خطر> لسرطان الثدي الثاني الابتدائي. BRCA1 مقترن العمر 45 ٪ مخاطر الاصابة بسرطان المبيض ، في حين أن نصف BRCA2 هذا الخطر (13) . حدد الباحثون والمناطق التي BRCA2 التي ترتبط مع ارتفاع معدلات الاصابة بسرطان المبيض ، وفي الممارسة السريرية ، ومع ذلك ، فإن جميع الطفرات الضارة في كل الجينات وترد معدلات مماثلة من مخاطر الاصابة بالسرطان. الأسر التي لديها أو BRCA2 BRCA1 الطفرات وزيادة خطر الاصابة بسرطان البروستاتا. الأسر التي لديها طفرات BRCA2 معرضون لخطر الإصابة بسرطانات الثدي والبنكرياس الذكور و، الحنجرة ، والمرارة / سرطان القناة الصفراوية ، وسرطان الجلد (13) . من BRCA1 و BRCA2 الطفرات ويقدر معدل انتشار ليكون في الفترة ما بين 1 300-800 أشخاص من التراث الأوروبي ، و 1 في 40 شخصا من اليهود الاشكناز التراث. الاختبارات الجينية لBRCA1 و BRCA2 ، والتي كانت متاحة سريريا لعدة سنوات ، ويشمل تقييم الترميز المنطقة بأسرها من كل الجينات بحثا عن الحذف واسع. يمكن أن يكون معقدا تفسير الاختبارات الجينية ، خاصة إذا كانت أهمية التعديلات الوراثية التي تم تحديدها غير مؤكد. في مثل هذه الحالات هو المسمى الطفرة متغير "أهمية غير مؤكد" ، والتي لا يمكن استخدامها لاختبار أفراد الأسرة الآخرين. في عام 2009 ، وكلية لطب النساء والتوليد ([أكغ]) نشرت الأمريكية توصية بأن المرأة مع 20 ٪ إلى 25 ٪ من فرصة وجود أو BRCA2 الطفرات الجينية BRCA1 الخضوع لتقييم المخاطر وينظر في الاختبارات الجينية (14) . [أكغ] تحديد المزيد من النساء اللاتي لديهن بنسبة 5 ٪ إلى 10 ٪ من خطر تحور أو BRCA2 BRCA1 كمرشحين محتملين لتقييم المخاطر الجينية. [أكغ] عام 2009 لتوصيات الاختبارات الجينية لدى النساء هي :
قيمة التحليل والنسب الكامل :وبالنظر إلى أن BRCA2 ترتبط BRCA1 ومع مجموعة متنوعة من أنواع السرطان المرضى طلب ، ينبغي أن يكون حول جميع أنواع السرطان المعروفة والعمر عند التشخيص بين الأقارب. وينبغي أيضا أن يطلب من مرضى السرطان على وجه التحديد حول الحالي في الثاني والثالث من الدرجة الأقارب (الأجداد والعمات والأعمام وأبناء العمومة والأولى) ، وهذه المعلومات قد تكون مفيدة في تحديد نمط وراثي جسمي قاهر. ومن المهم للقبض على تاريخ العائلة الأبوية والسؤال عن اعتمادها. قد تكون بعض حالات غامضة من التاريخ العائلي لسرطان الثدي وراثي وسرطان المبيض. خفضت الأقارب الذين لديهم استئصال الرحم أو oophorectomy كبير من فرصهم في الاضطرار الثدي أو سرطان المبيض. حجم ونوع الجنس وتوزيع الأسرة تؤثر أيضا على انتشار السرطان وراثية داخل الأسرة ، على سبيل المثال ، أسرة صغيرة جدا مع عدد قليل من النساء سيكون لها عدد قليل جدا من الأعضاء الذين قد أعرب عن الأنماط الظاهرية (15) . وأخيرا ، غالبا ما يكون من المفيد مراجعة السجلات الطبية لأفراد الأسرة لوضع تاريخ عائلي من السرطان وراثية ، لأن ليس كل أنواع السرطان خاص بأمراض النساء متساوون في هذا الصدد. الجينية نتائج الترجمة الفورية :وهناك مبدأ رئيسي في الاختبارات الجينية للسرطان وراثي هو اختبار شخص في العائلة الذي يرجح أن يكون هذا السرطان. في بعض الأسر ، وهذا الشخص القريب الذي أعطيت له مهلة تشخيص سرطان الثدي. ويمكن اختبار ذلك الشخص تحديد ما إذا كان التحول موجود في الأسرة ، وإنشاء الخلفية التي لتفسير نتائج الاختبار الجيني للأقارب. إذا كان من المعروف أن عائلة طفرة جينية ، ثم تفسير لاختبار قريب آخر واضح ومباشر : نتيجة الاختبار إيجابية بالنسبة لتحور نفسه يرتبط بزيادة احتمال الاصابة بالسرطان. وهناك نتيجة سلبية يعني أن المريض في خطر الاصابة بالسرطان متوسط ، ويرتبط تاريخ عائلتها إلى وجود طفرة التي لم انها ورثت. إدارة المريض بعد نتائج غير حاسمة : السيناريوهات التالية لتوضيح صعوبة تفسير سلبي BRCA1 / 2 النتائج في عائلة ذات تاريخ طويل من مرض السرطان ، ولكن لا يعرف الطفرة. السيناريو 1 : يتم تشخيص المريض بسرطان الثدي في سن 41 عاما. تم تشخيص شقيقتها مع سرطان المبيض في سن 52 سنة. والمريض هو الشخص في هذه العائلة على الأرجح أن يكون طفرة جينية ، ولكن يظهر الفحص أنها سلبية BRCA1 و BRCA2. تفسير : هذا الاختبار لا يستبعد سرطان وراثي في هذه العائلة. كما أنه من غير الممكن استبعاد خطر الاصابة بسرطان المبيض بالنسبة للمريض ، نظرا لتاريخ عائلتها. وهكذا ، فإن اختبار جيني عن نتيجة غير حاسمة. وينبغي أن يستند تقييم المخاطر وخطة لإدارة المريض عن تاريخ عائلتها. 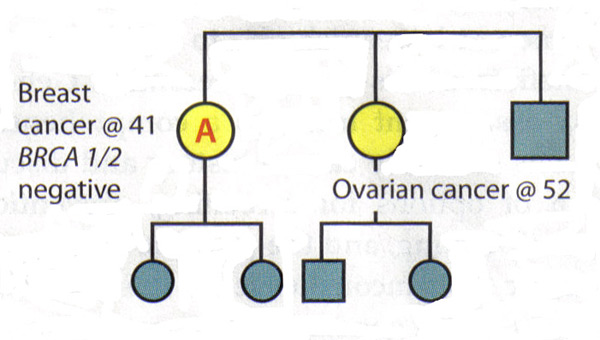 السيناريو 2 : تم تشخيص المريض أم بي في وقت متأخر وخالة مع سرطان الثدي وسرطان المبيض ، على التوالي. المريض طلبات باء الاختبارات الجينية للسرطان وراثي -- الأولى في الأسرة للقيام بذلك -- ويرى أنها BRCA1 و BRCA2 سلبية. تفسير : في حد ذاته ، وهذه النتيجة غير حاسمة. إذا كانت والدتها طفرة ، فإنه سيكون من الممكن الاستنتاج من النتائج السلبية التي باء المرضى معرضة للخطر في المتوسط. ومع ذلك ، منذ والدتها وعمتها حالة غير معروف وانه لم يعد من الممكن لاختبار لهم ، وتفسير هذه النتيجة غير واضحة. قد لا يكون هناك طفرة في الأسرة أو قد يكون هناك تحور أن المريض باء لم ترث. بدلا من ذلك لا يجوز ، وقد تم اختبار القيام به بشكل صحيح أو قد يكون هناك تحور في الجينات غير BRCA1 أو BRCA2. ولذلك ، ينبغي أن تدار المريض باء وفقا للتاريخ عائلتها. 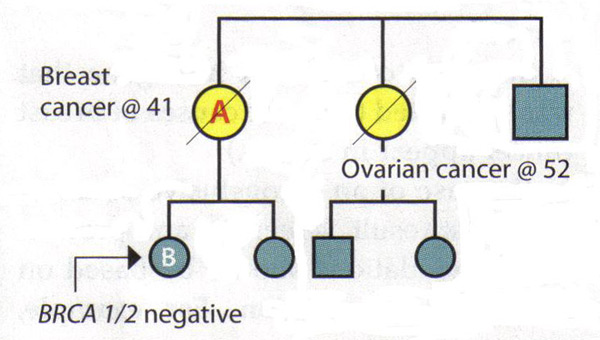 أسباب سرطان الثدي وراثي :ويمكن لنتائج سلبية في الفرد يعني عدة أشياء :
كثافة الثدي بالأشعة (مليون برميل يوميا) ، وخطر الاصابة بسرطان الثديكثافة الثدي بالأشعة (مليون برميل يوميا) تعبر عن مظهر من الثدي على الماموجرام ويشير إلى أن نسبة الكثافة النسبية للإشعاعيا ، أي أبيض أو ضوء مناطق الثدي. وقد استخدمت العديد من خطط التصنيف لتصنيف مليون برميل يوميا على مدى عقود من الزمن. وكان أول تصنيف لparenchymal نمط ولف أن تصنف مدى ونوع من الكثافة إلى 4 فئات (16) :
حاليا ، فإن المقياس الأكثر شيوعا السريرية الكثافة هو تصوير الثدي التقارير والبيانات نظم استقصاء المعلومات ، قاعدة بيانات طلبات العودة) طريقة الكثافة ، التي اقترحها الكلية الأمريكية للتصوير الشعاعي (3) (17) . استقصاء المعلومات ، قاعدة بيانات طلبات العودة هو قياس كثافة ذاتية الأشعة المستخدمة من قبل لتصنيف صور الأشعة على النحو التالي :
وتستخدم أساليب بمساعدة الحاسوب لتقدير التدابير الكمية من مليون برميل يوميا ، بما في ذلك كثافة في المئة (النسبة المئوية من الثدي عموما تظهر الأنسجة الكثيفة ؛ المشتريات) ، منطقة كثيفة المطلقة ، وكثافة منطقة غير (3) (16) . مليون برميل يوميا ، وخطر الاصابة بسرطان الثدي :تعتبر مرتفعة مليون برميل يوميا واحدة من أقوى عوامل الخطر لسرطان الثدي بغض النظر عن ما إذا كان هذا هو تقييم وقياس الكمي أو قاطع (16) . المرأة في أعلى فئات كثافة الثدي لديها 4 -- 6 أضعاف زيادة احتمال الاصابة بسرطان الثدي مقارنة مع النساء في أدنى الفئات. مليون برميل يوميا قد أظهرت أن تكون عامل خطر لسرطان الثدي أقوى من أي أشخاص آخرين ما عدا السن والطفرات الوراثية (16) . وكانت العلاقة بين مليون برميل يوميا وسرطان الثدي لدى كل من النساء الكبار والصغار تمر فحص تصوير الثدي بالأشعة السينية ، وكذلك في القوقاز ومنطقة القوقاز غير السكان. تأثير الهرمونات مليون برميل يوميا :وهناك أدلة قوية ومتسقة التي أثرت مليون برميل يوميا حسب العوامل الهرمونية مثل سن اليأس ، سن الحيض ، والمساواة ، والعمر عند الولادة الأولى ، واستخدام هرمونات خارجية (18) . الخارجية الهرمونات على مليون برميل يوميا هو أفضل ويتضح التأثير الإيجابي للجمعيات مليون برميل يوميا مع الهرمون بعد انقطاع الطمث (PMH) العلاج والجمعيات معكوس مع عقار تاموكسيفين (18) . هذه الجمعيات هي مهمة لأنها تشير إلى التباين بين الأفراد استجابة للعلاج الهرمون الذي يتجلى في التغييرات مليون برميل يوميا ، والتي قد تترجم إلى التفاضلية خطر الاصابة بسرطان الثدي. مع نضوب هرمون الاستروجين خلال انقطاع الطمث ، وأنسجة الثدي غدي الانحدار يمر. كما يتجلى ذلك من خلال انخفاض في مليون برميل يوميا خلال وبعد انقطاع الطمث. عندما تمت مقاطعة العملية التي PMH ، ودراسات تقييم مليون برميل يوميا عن طريق اتخاذ تدابير كمية تشير إلى أن هذه الهرمونات وترتبط بزيادة مطلقة من 3 ٪ الى 6 ٪ في مليون برميل يوميا (19) . في النرويجية الكشف عن سرطان الثدي برنامج (19) ، المستخدمين الحاليين للعلاج PMH كان يعني ارتفاع ملحوظ في المئة مليون برميل يوميا من المستخدمين للمستخدمين أبدا أبدا (ع للتيار <.001). وبالمثل ، فإن مرحلة مابعد انقطاع الطمث الاستروجين / البروجستين التدخلات (بيبي) الابتدائية ، والتي درست العلاقة بين PMH ومليون برميل يوميا ، كما شهدت زيادة مع الجمع بين العلاج بالهرمونات (20) . في مبادرة صحة المرأة (مبادرة الخوذ البيضاء) الدراسة ، تم اختيارهم بصورة عشوائية لاستقبال النساء يوميا يضاف إليها مجتمعة الاستروجين الخيول (أوروبا الوسطى والشرقية ، 0.625 ملغ) ، بالإضافة إلى خلات medroxyprogesterone (الآلام والكروب الذهنية ، 2.5 ملغ) أو وهمي. من 75 ٪ من النساء في أكثر نشاطا وPMH زيادة مليون برميل يوميا (18) . أخذت معا ، فإن هذه الدراسات تشير إلى أن ترتبط العلاجات مجتمعة الاستروجين والبروجستين ، في جرعات التقليدية مع زيادة كثافة الثدي ، بغض النظر عن نمط الإدارة البروجستين. والأهم ، وجمعيات من هذه العلاجات مع تغيير مواز مليون برميل يوميا مع الجمعيات خطر الاصابة بسرطان الثدي ، ومنها أن هناك زيادة في الاصابة بسرطان الثدي مع الجمع بين العلاج ولكن ليس مع هرمون الاستروجين وحده (21) . على الرغم من انخفاض جرعة نظم وأعرب عن أمله أن يكون أقل تأثير على كثافة الثدي ، وجدت دراسة حديثة لا فرق بين الجمعيات التقليدية وجرعة منخفضة من العلاج الهرموني مع كثافة المعادن بالعظام (22) . 1-2 أشهر وارتبط مع لوقف صغيرة فقط في انخفاض مليون برميل يوميا ، ووقف العلاج لهذه الفترة القصيرة لم يؤثر على معدلات أذكر الماموجرام (22) . 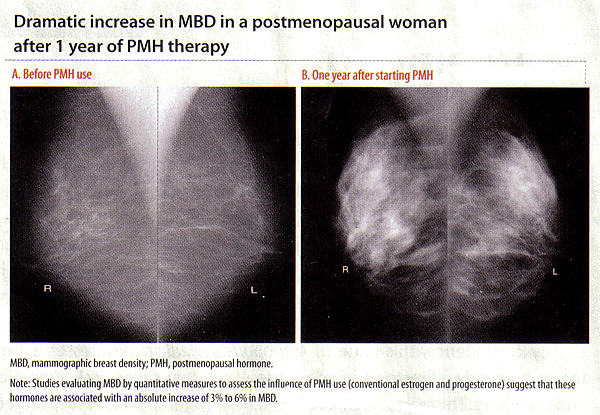 تأثير تاموكسيفين ، رالوكسيفين ، وموانع انزيمات اروماتيز مليون برميل يوميا على :ونظرا لعلاقة إيجابية بين PMH ومليون برميل يوميا ، فإن السؤال المنطقي هو ما إذا كان عقار تاموكسيفين ، رالوكسيفين أو مثبطات الاروماتيز خفض مليون برميل يوميا. تاموكسيفين : هي مستقبلات هرمون الاستروجين الانتقائية المغير (سيرميه) الذي يربط بشكل تنافسي لمستقبلات هرمون الاستروجين وكتل تركيب الاستروجين. وأدى تأثير antiestrogenic على الثدي في استخدامه كعلاج الغدد الصماء مادة مساعدة للنساء مع مستقبلات هرمون الاستروجين إيجابية بسرطان الثدي بعد انقطاع الطمث. كما تم استخدام تاموكسيفين كعامل قائية كيميائية للحد من خطر الاصابة بسرطان الثدي لدى النساء في خطر كبير. في الثدي الوطني المصاحب الجراحية والأمعاء المشروع (NSABP) تجربة سريرية عشوائية من النساء لمخاطر عالية ، 5 سنوات من العلاج وتبين تاموكسيفين الغازية للحد من خطر الاصابة بسرطان الثدي بنسبة 49 ٪ وغير الغازية خطر الاصابة بسرطان الثدي بنسبة 50 ٪ مقارنة مع الدواء الوهمي (23) . واختبرت دراسات عديدة آثار تاموكسيفين على مليون برميل يوميا باستخدام أساليب مختلفة لتقدير مليون برميل يوميا والسكان دراسة (أي النساء المصابات بسرطان الثدي المعروفة على تاموكسيفين أو مادة مساعدة النساء المعرضات للخطر عالية لسرطان الثدي في الوقاية الكيماوية لتاموكسيفين). وقد أظهرت هذه الدراسات أن النساء دائما على تاموكسيفين لا تشهد انخفاضا في ذات دلالة إحصائية مليون برميل يوميا. من هذه الدراسات ولاحظ البعض أن الانخفاضات في المئة مليون برميل يوميا في أكبر حدث في تواتر من قبل انقطاع الطمث في النساء بعد سن اليأس (24) . كان سمة مشتركة بين جميع هذه الدراسات على حقيقة أن ليس كل النساء على تاموكسيفين شهدت انخفاضا في كثافة الثدي مع العلاج ، ونسبة النساء تعاني من انخفاض في كثافة تتراوح بين 21 ٪ إلى 80 ٪. واعتبر ذلك عبر دراسات مختلفة مع طرق التقدير مليون برميل يوميا ، والسكان (ما إذا كانت المرأة المعرضة للخطر أو حالات السرطان) ، وكما ذكر أعلاه ، تتفاوت حالة انقطاع الطمث. وهذا يشير إلى الفرضية القائلة بأن انخفاض في تاموكسيفين مليون برميل يوميا الذي اثاره في جزء من المرأة أهمية سريرية ، مما أدى إلى عدد أقل من حالات السرطان بين النساء الحادث المعرضة للخطر وعدد أقل من حالات سرطان الثدي أو تكرار الأحداث المقابل بين الحالات. هذه المرأة أن تستفيد من المتبقية على تاموكسيفين. في المقابل ، قد أولئك الذين يرون قليلا أو حتى الحد من الزيادات في مليون برميل يوميا هم الذين سيستفيدون من أساليب علاجية بديلة. سيرميه عامل تم استخدام ورالوكسيفين : العضو الذكري للالوقاية الكيماوية من سرطان الثدي بسبب تخفيض تظاهروا في خطر الاصابة بسرطان الثدي بعد 5 سنوات من العلاج (23) . وقد أظهرت بعض الدراسات انخفاض مماثل في صفوف النساء مليون برميل يوميا في مقابل الوهمي رالوكسيفين ، حيث مثل الآخرين أظهرت التغييرات الطفيفة في مليون برميل يوميا مع استخدام رالوكسيفين (25) . في دراسة لرالوكسيفين ومليون برميل يوميا وفقا لتقييم كثافة الثدي الحجمي من حقل كامل الصور الرقمية ، ويرد عليه الحد الصغيرة في الحجمي مليون برميل يوميا في المجموعة رالوكسيفين (-4.1 ٪ متوسط 95 ٪ كاريتاس الدولية ، -6.9 ٪ -2.1 ٪) ، بالمقارنة مع زيادة في المشاهدة مليون برميل يوميا في جرعة PMH المجموعة المنخفضة (متوسط 15.0 ٪ ، 95 ٪ كاريتاس الدولية ، 4.8 ٪ -28.6 ٪ ع <.0001). الاروماتيز المانع (آيس) : كتلة التوليف المحلي لهرمون الاستروجين في مقتطفات من أورام الثدي البشرية وحاليا لعلاج فعال الغدد الصماء الأكثر إيجابية لهرمون الاستروجين المستقبلة للسرطان الثدي بعد انقطاع الطمث. واختبرت دراسات قليلة فقط هي التي لمنظمة العفو الدولية ، يتروزول ، ومليون برميل يوميا ، مع نتائج مختلطة. وتشمل هذه الدراسة 106 من النساء بعد سن اليأس الذين تم اختيارهم بصورة عشوائية إما ليتروزول همي أو بعد 5 سنوات من تاموكسيفين ، وجدت هذه الدراسة لا فرق بين المجموعات 2 مليون برميل يوميا في تغيير بعد 9-15 شهرا (26) . قد تكون متعلقة نتائج غير متناسقة من الدراسات من رالوكسيفين وان نظام التعريف الالى مع مليون برميل يوميا إلى أن يتم استخدام هذه العلاجات إلا في النساء بعد سن اليأس مع مليون برميل يوميا أقل خط الأساس ؛ إجراء تغييرات صغيرة من الصعب اكتشافها. ومع ذلك ، هناك حاجة لدراسات كبيرة مع الكثافة تدابير مدروسة جيدا ، ومتابعة لسرطان الثدي لتحديد ما إذا كان يمكن أن تستخدم مليون برميل يوميا والعلامات البيولوجية لهذه العلاجات وغيرها من الغدد الصماء. السريرية تطبيق مليون برميل يوميا ، وخطر الاصابة بسرطان الثدي :وقد أدرجت مؤخرا دراسات للاستقصاء المعلومات وقاعدة بيانات طلبات العودة قياس الكمية مليون برميل يوميا في خطر سرطان الثدي نماذج التنبؤ ، والتي أظهرت بعض التحسن في التنبؤ بالمخاطر (ج. تحسين إحصائية 0،01-0،06) (27) . نموذج معززة مع تدبير مليون برميل يوميا ولذلك فإن من الأفضل أن النموذج غيل الموجودة حاليا ولكن لا يزال ضعيفا للخطر فردية. زيادة مليون برميل يوميا كما أنه من المهم أن ندرك التحديات السريرية المرتبطة تقييم تصوير الثدي بالأشعة السينية للمرأة مع ، بما في ذلك الحاجة إلى تصوير الثدي بالأشعة السينية وكرر خزعات الثدي ، وصعوبة اكتشاف شذوذ سريريا كبيرة. ونظرا للجمعيات بين الهرمونات الخارجية وتغيير مليون برميل يوميا ، والسؤال الطبيعي هو ما إذا كان التغيير في مليون برميل يوميا هو علامة محتملة للخطر. وبعبارة أخرى ، إذا زادت مليون برميل يوميا تجربة المرأة مع استخدام PMH ، هم أكثر عرضة لسرطان الثدي من النساء اللواتي نقصان أو الحفاظ على مليون برميل يوميا بينما كان في PMH؟ أو إذا كان انخفاض مليون برميل يوميا امرأة على مادة مساعدة تاموكسيفين ، فهل هذا يعني أنها سوف يكون لها تخفيض خطر تكرار مقارنة مع امرأة لا يوجد لديه تغيير في مليون برميل يوميا في حين على تاموكسيفين؟ معظم الدراسات تشير إلى أن التغيير في مليون برميل يوميا يمكن أن تكون العلامات البيولوجية لسرطان الثدي الحد من المخاطر بالنسبة للمرأة التي تمر استراتيجيات الوقاية الكيماوية ويمكن أن يسمح لتحديد الهوية في وقت سابق من النساء اللواتي لن يستفيدوا من العلاج تاموكسيفين (28) . الدراسات جارية أيضا لدراسة تأثير تغير في مليون برميل يوميا مع استخدام PMH على خطر الاصابة بسرطان الثدي ، ومن المتوقع صدور النتائج في وقت قريب. في هذا الوقت ، ليس من الواضح ما إذا كانت الزيادات والانخفاضات في الناتج مليون برميل يوميا مع علاجات الغدد الصماء تغير ببساطة القدرة على الكشف عن سرطان الثدي الجديدة أو تتصل الفيزيولوجيا المرضية لسرطان الثدي. ولا بد من عمل إضافية لتحسين فهمنا للعوامل التي تساهم في تغيير ومليون برميل يوميا في ارتباطها بسرطان الثدي. أيضا ، من استنساخ ومدروسة جيدا ، كثافة التدابير التي يمكن أن بدقة قياس مليون برميل يوميا وهناك حاجة إلى تطوير للسماح للتغيير مقارنة مليون برميل يوميا عبر الدراسات وأنواع العلاج (28) . ملخص :سرطان تقييم المخاطر وإجراء استعراض شامل لوالمناقشة حول مخاطر تعرض الشخص للسرطان. وهذا يشمل الحصول على معلومات بشأن العوامل التي يمكن أن تخفف خطر الإصابة بالسرطان (على سبيل المثال ، واستخدام العلاج الهرموني ، واستخدام وسائل منع الحمل عن طريق الفم ، في سن الحيض والولادة الأولى). المكونات الأساسية الأخرى لتقييم المخاطر وتشمل مناقشة الأساس الجيني للسرطان ، تاريخ عائلي من السرطان ، والتاريخ العائلي للمرض السرطان ، احتمال متلازمة وراثية ، والخيارات المتاحة للفحص والوقاية. الاختبارات الجينية هي أداة يمكن أن تحسين تقييم المخاطر. قبل إجراء أي اختبار جيني ، ينبغي أن تناقش في النتائج الممكنة وآثارها على الفرد وعائلتها. هذا الاختبار له قيمة تكلفة الحد الأدنى لمريض غير مستعدة لتقاسم النتائج مع أقاربها. إذا كان من المناسب الاختبارات الجينية ، قد مستشار علم الوراثة أو غيرها من مقدمي الرعاية الصحية تسهيل الاختبارات الجينية عن طريق التحقيق في التغطية التأمينية ، وتقديم نتائج الاختبار والرعاية في إطار المتابعة ، ومساعدة المريض إبلاغ أقاربهم المعرضين للخطر. فهم التغير في الاستجابة للعلاج الغدد الصماء من الأهمية بمكان بحيث لا يمكن أن تدار من العلاج الأكثر فعالية للمرضى في الوقت المناسب. وهذا يشمل إقامة الخارجية الاستروجين للنساء صحية للحد من اعراض انقطاع الطمث ، وكذلك علاج سرطان الثدي بالنسبة للنساء مع المرض. مليون برميل يوميا قد يسهم في فهمنا للتقلب بين الفردية في الاستجابة للعلاج. هذه المعلومات يمكن أن تترجم بعد ذلك إلى الإعداد السريرية لتسهيل اتخاذ القرارات الشخصية بشأن الخيارات المتاحة لعلاج سرطان الثدي ، واستراتيجيات الحد من المخاطر. المراجع :
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||