Принципы медико-генетического консультирования и пренатальной диагностики
Доктор Фрэнсис H. Boudreau
Заведующий кафедрой акушерства и гинекологии
Св. Елизаветы медицинский центр, Бостон, Массачусетс (США)
В сотрудничестве с женского здоровья & образовательный центр (WHEC)
Наличие пренатальная диагностика для широкого спектра заболеваний была важным шагом вперед в области репродуктивной генетики. Ультразвуковой играет центральную роль в разработке различных подходов к пренатальной диагностики. Кроме того, интеграция генетики основе программы дородового диагноза с высшим ультразвуковой была показана для повышения точности диагностики по сравнению с ультразвуком в одиночку.
Целью данного документа является концентрация внимания на эпидемиологии генетических дефектов и включает описание различных пренатальная диагностика в использовании.
Эпидемиология
Всех беременностей выполнять базовые риск врожденных дефектов. Большинство генетиков цитатой цифру в 3% до 4% для крупных врожденных пороков развития. Важно сохранить этот базовый показатель в виду, когда консультирования пары относительно риска конкретного дефекта. Этиология на врожденные дефекты могут быть разбиты на 4 категории:
- Хромосомные
- Одного гена или менделевских расстройства
- Многофакторные расстройства
- Тератогенных или воздействия на окружающую среду
Пороки развития являются дефекты в структуре какого-либо органа или области тела в результате неразрывно ненормальный процесс развития. Такие пороки могут быть одно или несколько, они включают, например, врожденные дефекты вызваны дефектами одного гена. Деформации отклонения в форме, форме, или позиция вызвана механическими силами. Такая деформация часто встречаются пренатальной вследствие внутриматочной формования или ограничение. Факторы, ведущие к деформации могут быть внешними или внутренними. Срыв является морфологических дефектов в результате распада ранее нормальных тканей. Нарушения могут быть вызваны внешними силами, внутренними вмешательство в процесс развития сосудистых или оскорбления. Примерами нарушения включают ампутаций из-за амниотическая полосами и гастрошизиса porencephaly и, как полагают, в результате еще в утробе сосудистых оскорблений. Последовательность является структура несколько нарушений в результате одной первичной аномалии или механических факторов, а может быть пороки, деформации или срывов. Пример Поттер последовательности, в которой oligohydroamnios от любой причины приводят к аналогичным особенностями плода сжатия: характерные черты лица, ненормальное позиционирование рук и ног, и легочная гипоплазия. Синдром План нескольких аномалиям известно, имеют общие, конкретные этиологии. Примером может служить синдром Дауна, которая вызвана наличием дополнительных копий хромосомы 21. Ассоциацией используется, чтобы определить наличие двух или более компонентов, более широко, чем ожидалось, по случайности, но для которых этиология не было продемонстрировано. Типичным примером является Vater (позвоночного, Anal, трахео-пищевода и почек аномалии) ассоциации. Этот термин не подразумевает конкретного диагноза, а подсказки при поиске конкретной другие дефекты при выявлении одной из компонент объединения.
I. хромосомных аномалий:
Хромосомные происходить примерно в 0,5% новорожденных и это хорошо известно, что риск для многих хромосомными аномалиями с увеличением возраста матери продвижение (1). Исследования пренатального происхождения 21-й хромосомы с синдромом Дауна показали, что 95% случаев трисомии 21 связаны с материнской нерасхождение и лишь около 5% случаев содержать дополнительные отцовски 21. Хотя возраст матери очень сильно коррелирует с риском синдрома Дауна, большинство детей с синдромом Дауна рождаются у женщин моложе 35 лет. Много других хромосомных аномалий, также связаны с увеличением возраста матери, в том числе 13 и 18, 47, XXX; 47, XXY; и 47, XYY. Структурные хромосомные аномалии, такие как транслокации и удаление, а также синдромом Тернера (45, X) не кажутся возрастными.
Хромосомные аномалии ведущий известной причиной прерывания беременности, и по меньшей мере 95% хромосомных ненормальной концепций потерял раньше срока. Предполагается, что как минимум 10% до 15% от концепций хромосомных ненормальными. Исследования показывают, что выкидыши примерно 50% таких хромосомные аномалии трисомии, 20% monosomies, являются триплоидные 15%, а остальная часть тетраплоидов и структурные аномалии. Некоторые хромосомные аномалии, такие как трисомия 16, являются общими в момент зачатия, но никогда не видел в живых новорожденных детей.
Хромосомные аномалии в Liveborns (2):
| Типы ненормальность | Заболеваемость |
|---|---|
| Численный аберрации половых хромосом 47, XYY | 1 / 1080 новорожденных мальчиков |
| Аутосомно трисомии 13 | 1 / 19, 000 |
| Структурные Сбалансированный нарушения: Робертсоновских T (DQ; Dq) | 1 / 1500 |
| Несбалансированное структурными аномалиями: Робертсоновских | 1 / 14 000 |
II. Одноместные гена:
Одного гена или менделевских, нарушения происходят примерно в 1% новорожденных. Большое число менделевских расстройства были описаны, хотя в какой-либо конкретной беспорядков в целом встречается редко. Так, например, кистозный фиброз несущей частотой примерно 1 на 20, в результате чего болезнь частотой примерно 1 в 1600 году. Из признанных черт одного гена, более половины из них аутосомно-доминанта, примерно треть аутосомно-рецессивные, а остальные Х-хромосомой.
Аутосомно-рецессивный расстройства: возникает чаще всего в здоровых лиц, чьи оба родителя обладают таким же рецессивным геном. Риска для потомства таких родителей составляет 25% в каждой беременности, и эти нарушения чаще всего происходят не с историей семьи. Аутосомно-рецессивные расстройства часто являются серьезными, и многие из них метаболических расстройств. Перевозчики будут иметь в среднем 50% от активности фермента. Повышенный риск для родителей, которые являются двоюродными братьями и сестрами, чтобы родить ребенка с серьезными отклонениями составляет примерно 6%, или дважды фоне риска.
Аутосомно-Доминант расстройства: пострадавшие люди гетерозиготных аллелей ненормальные, которые они передают до 50% от их потомства, мужчина или женщина. Unaffected людей не передают расстройством. Возраст начала многие из этих заболеваний является переменной и людей с дефектным геном, который, следовательно предназначенные для развития заболевания, может протекать бессимптомно, пока также во взрослом возрасте. Лиц из групп риска могут иметь собственных детей до возраста, в котором они развиваются симптомы. Острота многих аутосомно расстройств существенно различаются, даже в рамках одной семьи. Вероятно, тяжесть в любом пострадавшим потомство трудно предсказать и, мягко пострадавшим родитель может иметь особое ребенка. Новые мутации для аутосомно-доминантное расстройства, как представляется, больше общего с увеличением отцовского возраста. Из-за большого числа аутосомно-доминирующие условия, которые могут возникнуть в результате такой мутации, никаких конкретных дородовое тестирование доступно. В нейрофиброматоза примерно в 50% случаев заболевания происходит за счет новых мутаций. В Ахондроплазия, гомозиготной форме смертоносной и может быть предсказано возникновение в 25% случаев пострадавшие с двумя родителями. Из такого потомства, 50% будет гетерозиготных и пострадавших, а 25% будет нормально.
Х-сцепленные заболевания: наиболее Х-хромосомой рецессивные расстройства, с hemizygous (имеющие только одну копию хромосомы X) мужчин пострадавшим женщинам и гетерозиготных носителей не изменяются. Женщина перевозчик будет передавать гена-мутанта, до 50% от ее потомство, и поэтому половина ее сыновей будет затронуто, и половина ее дочери будут носителями. Пострадавшим мужчины пройдет мутант Х-хромосоме, чтобы все его дочери (которые, таким образом обязать перевозчиков), и ни один из его сыновей (кто наследует только его Y хромосомы). Мышечной дистрофии Дюшенна может быть тяжелым или смертоносного ходе ранних этапах жизни, так что пострадавшим сыновья не размножаются. Х-сцепленные заболевания могут быть доминирующими, хотя этот тип наследования гораздо реже.
III. Многофакторные наследованию:
Изолированный врожденных дефектов, таких, как косолапость, расщелина губы и дефектов нервной трубки (NTDS) являются одними из наиболее распространенных генетических аномалий и наследуются на основе сочетания генетических и средовых факторов. Примером многофакторного чертами являются: hydrocephly, дефектов нервной трубки, расщелина губы с или без расщелина неба, расщелина неба, нарушения сердечной деятельности, диафрагмальная грыжа, пупочная грыжа, почечная бесплодие, Мюллеров дефектами синтеза, дефекты конечностей сокращение пилорического стеноза и косолапости эквиноварусная.
Повторение риск для родственников пострадавшего члена семьи, как правило, выше, чем население риска, наиболее многофакторных расстройств с риском повторения от 2% до 5% в первой степени родства. Этот риск возрастает, если затрагиваются более членов семьи. Существует также некоторое повышение риска многофакторных нарушения с родительскими родства. Многофакторные черт обычно попадают в одну из трех следующих категорий: постоянный или переменный порог сложных расстройств. Непрерывное черт, как правило, менее экстремальный в потомстве людей, страдающих из-за принципа статистической регрессии для среднего. Они, как правило измерению или количественных признаков, как высота или размера головы, и, как полагают, в результате индивидуальной малые эффекты многих генов в сочетании с факторами окружающей среды. Пороговое черт не появляются до определенного порога превышения ответственности. Расщелина губы и неба и стенозом привратника являются примерами порога черты. Некоторые черты порога имеют пристрастие к одному полу, указав, что мужчины и женщины имеют различные порог ответственности. Риск повторения для пороговых черт также выше, если дефект серьезный, снова указывает на наличие более аномальных генов или влияния. Например, риск повторения после рождения ребенка с двусторонней расщелиной губы и неба составляет 8%, по сравнению лишь с 4% после односторонней расщелиной губы без расщепления неба. Комплекс расстройств взрослой жизни чертами, в которых многие гены определения восприимчивости человека к экологическим факторам, с болезнью в результате самым неблагоприятным сочетанием обоих. К этой категории относятся общие заболевания, такие как болезни сердца и гипертонии (3).
IV. Тератогенам или воздействия окружающей среды:
Тератогенам или экологического воздействия, как полагают, причина врожденных аномалиях в менее чем 1% младенцев. Эта область является важной, так как эти воздействия являются потенциально предотвратить. Такие тератогенам включать лекарственные средства, воздействие агентов, таких как ионизирующая радиация, и побочных продуктов некоторые материнской метаболических расстройств, таких как диабет и фенилкетонурия.
Подробности см. в главе о: наркотики во время беременности и лактации
Показания для пренатальной диагностики:
Важно, что при угрозе пар быть информирован о всех своих репродуктивных функций. Прежде чем пытаться пренатальная диагностика наследственных заболеваний, любой, важно, чтобы установить или подтвердить направлены на устранение возможности из-за неправильного диагноза фенотипического, метаболические или генетической гетерогенности. В случае ферментативных или молекулярной диагностики, точного дефекта должен быть отражен в пробанда или пострадавшие родственники. Если умерший пробанда, гетерозиготности обоих родителей (или от матери к Х-хромосомой болезней), должны быть документально зафиксированы. В случае Dysmorphic синдром, все проявления беспорядков должны быть известны и искать на момент оценки.
Наиболее распространенными показаниями для дородовой диагностики исследований являются: передовые материнского возраста; ненормальной биохимический скрининг; предыдущего ребенка с хромосомными расстройством; сбалансированная транслокация перевозчика для хромосомного беспорядка; предыдущего ребенка с наследственным нарушением обмена веществ; гетерозиготных пары обнаружили перспективе за счет отбора программ; Предыдущее детей с расстройством обнаружить с помощью ультразвука.
Многофакторные расстройства: предыдущего ребенка с дефекта нервной трубки; повышенной материнской сыворотки альфа-фета-протеин (АФП) и предыдущего ребенка с дефектами развития или синдромом обнаружения пороков развития с помощью ультразвука.
Экологические недостатки: пренатального воздействия тератогенного наркотиков или инфекционного агента.
Использование материнского возраста 35 лет или старше в момент доставки или взрослых на момент доставки, а показания к инвазивным тестирование (амниоцентез или биопсия хориона), примерно в 20% случаев синдрома Дауна будет обнаружено. 80% случаев синдрома Дауна будет происходить в не проверенных группой. В попытке повысить уровень обнаружения синдрома Дауна, midtrimester материнской биохимический скрининг сыворотки был разработан обнаруживает, что примерно в 60% случаев синдрома Дауна среди населения в целом (4).
Для биохимического скрининга врожденных дефектов:
Некоторые из величайших достижений в области генетики в последние два десятилетия произошли в области биохимический скрининг на врожденные дефекты у плода. Ряд биохимических маркеров уже были изучены для использования в пренатального скрининга. К ним относятся:
Альфа-фета-протеин (АФП):
АФП онко-белка производства фетальной печени и яичного и является основным белком сыворотки в начале жизни плода. Первоначально она входит в амниотической жидкости с помощью диффузии через кожу незрелый плод, а затем через плода мочеиспускание. Небеременных женщин уровни АФП, что едва обнаруживаемые (1 U / L), тогда как нормальный средний уровень на 16 до 18 недель беременности от 18 до 40 U / л Материнской сыворотки AFP продолжает увеличиваться до 28 до 32 недель беременности. В плод с дефектом, например анэнцефалия или Спина-позвоночника, AFP входит в амниотической жидкости к увеличению сумм, что приводит к более высокому уровню материнской сыворотки также. Уровни АФП возводятся в амниотической жидкости и материнской сыворотки только при таких поражениях являются "открытыми", т. е. при нервных тканей подвергается или покрыта лишь тонкой мембраной. Практически 100% анэнцефалии поражений остаются открытыми; закрыты около 20% Спина-позвоночника случаях, как около 82% от encephaloceles (5). Дискуссии по поводу чувствительности и специфичности тестирования AFP, как правило, ограничено, чтобы открыть поражения, как это предполагалось, что закрытые повреждения не будут обнаружены.
В лаборатории, предоставляющие AFP проверка, результаты выражаются в виде кратных медианы (MoM), которая позволяет выражение измерений в общем пути. Распределение материнской сыворотки AFP (MSAFP) является лог-Гаусса, с медианного значения 1,0 для нормальной беременности, беременность за 3,8 с открытым Спина-позвоночника, и 6.5 для беременных, пораженных анэнцефалия. Два наиболее часто используемых для отключения MSAFP равны 2,0 и 2,5 MOM. На 2,0 м / м ложно-положительный диапазон размере от 4% до 6%, а уровень обнаружения открытых Спина-позвоночника колеблется от 85% до 90%. Что выше отсечки 2,5 MoM ложно-положительный снижает ставки на 2% до 3%, а уровень обнаружения уменьшается с 75% до 80%. Женщины с предварительным гестационного диабета MSAFP ценности, которые в среднем 20% ниже, во втором триместре беременности. Когда оценивается уровень MSAFP выше среза (или 2,0 или 2,5 м / м) точность знакомств. Если датировка на основе последнего менструального периода была использована для первоначального расчета, и ультразвуковые должна быть выполнена для точной знакомств. Амниоцентез может быть указано, чтобы установить причину повышенного AFP.
Причинами повышенной MSAFP: многоплодной беременности; гибели плода; фетальных материнской кровоизлияния плацентарной отклонений; аномалиями матки; материнской яичников или печеночной опухоли. Структурных дефектов плода: дефектов нервной трубки - Спина-позвоночника, анэнцефалия, encephaloceles; открытых вентральный дефекты стены - пупочная грыжа, гастрошизиса; врожденный нефроз; triploidy; двусторонние почечные бесплодие, врожденные расстройства кожи - эпидермолис буллезной, аплазия cutis; аутосомно-рецессивный поликистоз заболевания почек; крестцово-копчиковый тератомы; кистозный adenomatoid пороков развития легких.
Triple скрининговый маркер:
Ряд других биохимических маркеров уже были изучены для использования в анеуплоидия скрининга. Оба неконьюгированный эстриол (UE3) и человеческий хорионический гонадотропин (ХГЧ) добавить специфичность и чувствительность до второго триместра биохимический скрининг на синдром Дауна. Тройной скрининг маркер с AFP, UE3, ХГЧ и сейчас регулярно предлагают во время беременности. Большинство центров использования 1 / 270 риска синдрома Дауна в midtrimester как срез, над которым предлагается амниоцентез; этот риск эквивалентный 35-летняя женщина. Как AFP скрининга, материнской веса, расы, сахарный диабет, и число плодов настоящему все рассматриваемые в расчет риск.
Эмбриональной ткани отбора проб ДНК и методология:
Некоторые наследственные заболевания выражаются только в конкретной ткани, и, следовательно, отбор проб тканей, что необходимо, если пренатальная диагностика будет сделано. Фетальной печени, кожи эмбриона и плода, мышцы были получены ультразвуковая биопсия (6). По мере достижения прогресса в выяснении конкретным молекулярным дефектом в условиях постоянно растущего числа генетических заболеваний, пренатальная диагностика будет возможно путем анализа ДНК. Потому что ДНК присутствует в каждой клетке зарождения, минимально-инвазивные методы, такие как амниоцентез или биопсия хориона может заменить более инвазивных процедур, таких как отбор проб крови эмбриона или плода биопсии печени для пренатальной диагностики многих заболеваний.
Ультразвуковая оценка хромосомные аномалии
За последние полтора десятилетия, области генетической Эхография вышел. Пятнадцать лет назад амниоцентез было зарезервировано для женщин передовой возраста матери, в результате чего потенциал для выявления менее четверти анеуплоидия плодов. Теперь решение о том, пациент подвергается риску для плода анеуплоидия будет основана на сочетании возраст матери, несколько биохимических маркеров, а также полная оценка ультразвукового плода. Возможно, с помощью этого комбинированного метода, мы будем прогресса от потенциального выявлению 20% плодов с синдромом Дауна (т.е. тех, кто связан с материнской возраст> 35 лет), чтобы быть возможной скорости обнаружения 90% плодов с хромосомными аномалиями, рекомендовав амниоцентез только 5% до 10% беременных женщин.
Ультразвуковая руководствуясь Диагностические процедуры Акушерско
Синдром Дауна является самой распространенной хромосомной аномалии среди новорожденных жить и также оказался самый неуловимый sonographically синдром всех аутосомно trisomic синдромов. Представляется логичным, однако, что рассмотрение УЗИ плода сама по узнаваемых особенностей детей с синдромом Дауна было бы еще более чувствительны и специфичны для обнаружения пострадавшего плодов, чем возраст матери и сывороточный скрининг.
Сонографические скрининга на Синдром Дауна
Маркеры ультразвуковой анеуплоидии:
Во втором триместре ультразвуковое обследование часто регулярно проводится для выявления плода анатомических нарушений, о выводах основной аномалии, два или более мелкие структурные пороки увеличивает вероятность анеуплоидии и гарантирует, генетическое консультирование и рассмотрение амниоцентез (7). Количество структурные аномалии плода и не патологическое (или "мягкие") обнаружение маркеров на втором триместре беременности ультразвуковое экспертизу были также связаны с синдромом Дауна. Исследования показали, что во втором триместре ультразвуковое обследование можно определить от 50 до 75% плодов с синдромом Дауна, на положительные темпы отбора от 4 до 15%. Однако испытание на эффективность зависит от исследуемой популяции, выбор маркеров, гестационного возраста и опыта ultrasonographer. Общий подход заключается в использовании правдопобия для ультразвуковой маркеров (рассчитывается путем деления чувствительности ложных срабатываний), чтобы рассчитать риск женщины иметь плод с синдромом Дауна; риска, основанные на возраст матери или сыворотки скрининга умножается правдоподобия (8). В проспективном, демографические когорты исследования с участием женщин с результатами скрининга сыворотки указал, что повышение риска синдрома Дауна, наличие структурных аномалий или утолщенной затылочный кратным увеличением риска синдрома Дауна раз из девяти, а также отсутствие аномалия снижает риск на одну треть. При мягкой маркеров были обнаружены в сочетании с структурные аномалии, риск синдрома Дауна было больше увеличилось, в то время как вывод из мягкой маркерами (исключая толстые затылочный раза) не изменить существенным риском.
Значение мягкой маркеров обнаружен на обычном ультразвуковом обследовании в 20 недель гестации у пациента, который в противном случае, как представляется, при низком уровне риска по рождению ребенка с трисомии 21 или трисомии 18 является неопределенным, и опасение, что присутствие этих маркеры могут привести к инвазивных диагностических процедур, которые не являются необходимыми. И наоборот, нормальная ультразвуковое обследование может предоставить ложные заверения пациентов с риском, который увеличился на основе сывороточных маркеров или возраста. В первом триместре беременности, не визуализации носовой кости на ультразвуковом экспертиза была связана с повышенным риском синдрома Дауна и другими анеуплоидии. При использовании с первого триместра комбинированный скрининг у пациентов с повышенным риском из-за материнского возраста (средний возраст 35 лет), и расчетной ставки обнаружения трисомии 21 составил 93% при положительных темпов отбора на уровне 5% (9). Оценка носовых костей были включены в алгоритм скрининга в некоторых центрах, но она должна быть выполнена только обученным ultrasonographers.
Ультразвуковой выводов при трисомии 21:
Структурные аномалии: пороки сердца; кистозный hygromas; атрезия двенадцатиперстной кишки; вентрикуломегалия.
Non-патологические выводы, или "мягкие маркерами": толстые затылочный раза (> 6 мм); гипоплазии или отсутствует носовая кость; сосудистого сплетения кисти; эхогенна внутрисердечной фокус; почечная pyelectasis; краткий плечевой; краткий бедра; эхогенна кишечника; пуповина с двумя судов; гипоплазии средней фаланги пятого пальца; сандалового разрыв ног (разделение большого пальца)
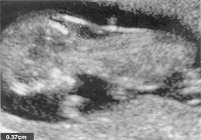
Увеличение прозрачности затылочный измерения составляет 3,7 мм на 12 недель плод с синдромом Дауна
Другое первого триместра ультразвуковой маркеров под следствием (например, венозном протоке по визуализации потока Доплера, плода недостаточность трехстворчатого клапана, и ненормальные лобно-верхнечелюстной и верхнечелюстной углом нижней челюсти) обычно не используются при проверке алгоритмов в повседневную практику (10). Предпосылки для более широкого применения этих мер включают в оценку населения с низким уровнем риска, использование данных о гестационного возраста и норм, которые являются специфическими для рас пациента или этнической группе, принятие стандартизированного подхода, соответствующей подготовкой и осуществлением качество программ оценки.
Резюме:
Ультразвуковой будет продолжать играть важную роль в развитии этих новых подходов к плода пренатальная диагностика и терапия. Наличие раннего первого триместра пренатальная диагностика может предоставить возможности для дородового лечения некоторых расстройств путем замены недостающих ферментов или сомножителей, по соматической генной замена или транспортировка стволовых клеток. Безопасного и надежного доступа к циркуляции плода открывает новую эру в пренатальной диагностике плода и эмбриона терапии.
Список литературы
- American College of Obstetricians and Gynecologists. ACOG Practice Bulletin. Invasive prenatal testing for aneuploidy. Obstet Gynecol 2007;110:1459-1467
- Nuaabaum RL, McInnes RR, Willard HF. Thompson & Thompson genetics in medicine. 7th ed. Philadelphia: Sunders/Elsevier, 2007
- The human genome. Science 2001;291:1145-1434
- Malone FD, D'Alton ME. First-trimester screening for Down syndrome. Obstet Gynecol 2003102:1066-1079
- Bahado-Singh RO, Oz UA, Mendilcioglu I et al. The mid-trimester genetic sonogram. Semin Perinatol 2005;29:209-214
- Simpson JL, Elias S. Genetics in obstetrics and gynecology. 3rd ed. Philadelphia, WB Saunders, 2003
- Alfirevic A, Sundberg K, Brigham S. Amniocentesis and chorionic villus sampling for prenatal diagnosis. Cochrane Database Syst Rev 2003;3:CD003252
- Smith-Bindman R, Chu P, Goldberg JD. Second trimester prenatal ultrasound for the detection of pregnancies at increased risk for Down syndrome. Prenat Diagn 2007;27:535-544
- Rosen T, D'Alton ME, Platt LD et al. First-trimester ultrasound assessment of the nasal bone to screen for aneuploidy. Obstet Gynecol 2007;110:399-404
- Driscoll DA, Gross S. Prenatal screening for aneuploidy. N Engl J Med 2009;360:2556-2562
Опубликован: 19 October 2009
Dedicated to Women's and Children's Well-being and Health Care Worldwide
www.womenshealthsection.com


