Manejo clínico de la endometriosis
WHEC Boletín Práctica Clínica y de gestión para proveedores de atención médica. Educación subvención prevista de Salud de la Mujer y el Centro de Educación (WHEC).
La endometriosis es un trastorno crónico y recurrente de reproducción con la variable de presentaciones clínicas. Gestión varía en función de la edad del paciente, los síntomas, la extensión de la enfermedad, los objetivos reproductivos, los riesgos del tratamiento, efectos secundarios, y las consideraciones de costos. Es relativamente frecuente crónica trastorno ginecológico que se presenta con dolor pélvico crónico o infertilidad. La presencia de viables, sensibles al estrógeno, endometrio-como glándulas y estroma asociados con una respuesta inflamatoria fuera del útero a nivel mundial se conoce como endometriosis. A pesar de nueve décadas han pasado desde que fue descrita por primera vez por Sampson, la endometriosis sigue siendo un trastorno desconcertante debido a sus diversas presentaciones clínicas y controvertidos orígenes etiológicos. Una vez que la endometriosis se diagnostica en una mujer en edad reproductiva, debe ser considerada como una enfermedad crónica con múltiples episodios recurrentes de dolor, infertilidad, y la prolongación de los intervalos libres de síntomas. El costo anual estimado para el tratamiento de la endometriosis es más de $ 20 mil millones. Tres subtipos de la endometriosis se diferencian por la inspección macroscópica y microscópica que consta de endometriomas (quistes ováricos), superficiales implantes endometriales (foco de la enfermedad principalmente en el peritoneo), y la endometriosis profunda infiltrante (nódulos rectovaginales). Cada forma puede tener su propia etiología u origen compartir con las otras formas de esta enfermedad crónica frecuente en ginecología.
El propósito de este documento es revisar los agentes utilizados en el tratamiento médico de la endometriosis y discutir el uso de la técnica de reproducción asistida (TRA) en pacientes con endometriosis que desean el embarazo. La etiología, la relación entre la extensión de la enfermedad y el grado de los síntomas, el efecto sobre la fertilidad, y el tratamiento más adecuado de la endometriosis siguen siendo incompletos. Esta revisión también se presenta la evidencia, incluyendo los riesgos y beneficios, para la efectividad de la terapia médica y quirúrgica de las mujeres adultas que son sintomáticos con dolor pélvico, infertilidad o ambos. Los enfoques más recientes que utilizan la variedad de tratamientos disponibles médicas y quirúrgicas se discuten, ya que se refieren específicamente a la población adolescente. La endometriosis es una enfermedad crónica relativamente común ginecológica que se presenta con dolor pélvico crónico o infertilidad. El efecto social de esta enfermedad es enorme, tanto en los costos monetarios y en la calidad de vida.
Incidencia:
Esta enfermedad afecta enigmática 6-10% de mujeres en edad reproductiva y se ha encontrado en las mujeres entre las edades de 12 y 80 años (1) . La edad promedio de diagnóstico es de aproximadamente 28 años (2) . La tasa de prevalencia del 38% (rango: 20-50%) se encuentra en las mujeres infértiles y en el 71-87% de las mujeres con dolor pélvico crónico (3) . A diferencia de muchas especulaciones, no hay datos que apoyen la idea de que la incidencia de la endometriosis está aumentando, a pesar de un mayor reconocimiento de las lesiones de endometriosis puede haber conducido a un aumento en la tasa de detección. También parece haber una predisposición racial en particular a la endometriosis. Una asociación familiar de la endometriosis se ha sugerido, y los pacientes con un primer grado afectado con relación tienen cerca de un 7 a 10 veces mayor riesgo de desarrollar endometriosis (4) . La herencia propuesta es característico de un mecanismo poligénico-multifactorial. Un número de polimorfismos genéticos han sido identificados. En los Estados Unidos, los costos estimados de diagnóstico de la endometriosis y el tratamiento del dolor y la infertilidad asociada ascendieron a US $ 22 mil millones en 2002 (7) . Teniendo en cuenta la tasa de recurrencia de la endometriosis se conoce con el tiempo, sin tratamiento médico, la mujer más probable que tenga su pista endometriosis hacia la progresión de la enfermedad en lugar de resolución. Además, la sensación de dolor no se correlaciona necesariamente con la identificación de las lesiones. Los mecanismos responsables de la expresión de síntomas en curso probable es compleja y multifactorial.
Fisiopatología:
La mayoría de los expertos coinciden en que la enfermedad es de etiología multifactorial. De larga data postulados incluyen la menstruación retrógrada con implantación en el menstruo reflujo estructuras pélvicas, celómicas células pluripotenciales mesoteliales que recubren el peritoneo someterse a la metaplasia en el tejido del endometrio y la implantación de las células a través de hematógena o linfática embolización. Sin embargo, un interrogante persiste: ¿por qué la enfermedad se desarrollan en algunas mujeres y en otros no? Una mayor comprensión de los mecanismos moleculares asociados a la endometriosis ha mejorado las teorías tradicionales. Los avances recientes respecto a la etiología de la endometriosis se debe aplicar con criterio en la práctica clínica para lograr un resultado óptimo del tratamiento. Retrógrada tejido trasplantado células de endometrio y de adherirse a las superficies peritoneales, establecer un suministro de sangre, e invadir las estructuras cercanas (5) . Están infiltrados por los nervios sensoriales, simpáticas, y parasimpático, y provocar una respuesta inflamatoria. Implantes endometriales segregan estradiol (E2), así como la prostaglandina E2 (PGE2), agentes que atraen a los macrófagos (proteína quimiotáctica de monocitos 1 [MCP-1]), péptidos neurotróficos (factor de crecimiento nervioso NGF ), enzimas para la remodelación de tejidos (metaloproteinasas de la matriz [MMPs]) y los inhibidores tisulares de las MMP (TIMP), y las sustancias proangiogénicos como el factor de crecimiento endotelial vascular (VEGF) y la interleucina-8 (6) . Las lesiones secretan haptogobin, lo que disminuye la adherencia de macrófagos y de función fagocítica. Las lesiones y los macrófagos activados, que son abundantes en el líquido peritoneal en mujeres con endometriosis, también secretan citocinas proinflamatorias (interleucina-1β, IL-8, IL-6 y factor de necrosis tumoral α-[TNF-α]). Local (y sistémica) de estradiol puede estimular la producción de la lesión de PGE2, que puede activar las fibras del dolor, mejorar la invasión de las lesiones neuronales, estimulando la producción de neurotrofinas NGF y otros, y promover el surgimiento de los nociceptores que contribuyen dolor inflamatorio persistente e inhibir la apoptosis neuronal. Factor de sangrado endometrial (EBAF) no se expresan con acierto y puede contribuir a la hemorragia uterina. Infertilidad resultados de los efectos tóxicos del proceso inflamatorio en gametos y embriones, la función comprometida fimbrial, y el endometrio ectópico que es resistente a la acción de la progesterona, y por lo tanto el endometrio es inhóspito para implantar un embrión (7) . HOXA10 y HoxA11 genes y αVβ3 integrina no están regulados por la progesterona, el endometrio y por lo tanto es inhóspito para la implantación de un embrión. Productos químicos disruptores endócrinos pueden contribuir a la resistencia a la progesterona y tal vez la disfunción inmune (7). ERFFI1 (inhibidor de la respuesta de receptores ErbB 1) se expresa constitutivamente y no hay exceso de señalización mitogénica.
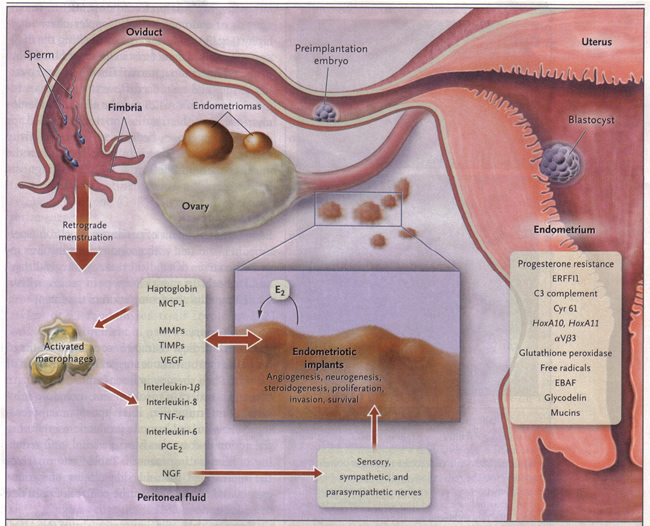
Figura 1. Fisiopatología del dolor y la infertilidad asociada a la endometriosis
Mecanismo del Dolor: Muchos estudios han señalado la presencia de un aumento de citoquinas proinflamatorias y factores de crecimiento en la endometriosis, que están estrechamente relacionados con la sensación de dolor (es decir, el factor de crecimiento del nervio, la prostaglandina, el estradiol) (8) . Esto puede explicar por qué la endometriosis mínima todavía puede causar mucho dolor. La evidencia actual indica que la endometriosis es un estado que resulta de hiperalgésico el procesamiento del dolor aumentada que es dictado por la forma en la médula espinal y el cerebro procesan el dolor de las lesiones y la información sensorial. Las fibras nerviosas periféricas que suministran las lesiones de endometriosis podría sensibilizar a las neuronas espinales del segmento y, finalmente, dar lugar a una sensibilización del sistema nervioso central, dando lugar a una respuesta exagerada del sistema nervioso central o fantasma-como el dolor de endometriosis, o ambos, a pesar de la ablación de las lesiones (9) . Esta sintomatología multidimensional de las órdenes de la endometriosis estrategias multidisciplinares de gestión.
Mecanismo de la subfertilidad: Los casos avanzados de endometriosis a menudo conllevan graves enfermedades adhesivo que podría suponer un deterioro evidente de la fertilidad mediante la reducción de la motilidad del tubo-ovárico, que en última instancia, impide la pick-up función. Si las formas más leves de la enfermedad incluso causar subferility no es cierto. Las mujeres infértiles con un mínimo de endometriosis leve tenían menores niveles séricos de la hormona antimulleriana en el día 3 que los pacientes infértiles con obstrucción tubárica (10) . En la endometriosis mínima o leve, el mecanismo biológico que causa la infertilidad sigue siendo difícil de alcanzar. Una vez más, una respuesta inmune mejorada puede ser el culpable de que perjudican la fertilidad en la enfermedad en estadio temprano (11) . Un ambiente hostil peritoneal puede conducir a la alteración de la función del esperma a través de aumento del daño del ADN espermático y un citoesqueleto comprometida ovocitos. Otra teoría atribuye la responsabilidad de un defecto de endometrio basa en los informes de la disminución de la expresión de varios marcadores biológicos de la implantación. Por desgracia, la endometriosis se asocia con un mayor riesgo de parto prematuro, complicaciones prenatales y preeclampsia.
Diagnóstico y Clasificación
Las manifestaciones clínicas de la endometriosis son variables e impredecibles en cuanto a presentación y el curso. La dismenorrea, dolor pélvico crónico, dispareunia, nódulos uterosacros, y una masa anexial (ya sea sintomática o asintomática) son algunas de las manifestaciones bien reconocidos. Un número significativo de mujeres con endometriosis son asintomáticas. El diagnóstico definitivo de la endometriosis sólo se puede hacer por histología de lesiones extirpadas en la cirugía. Ni los marcadores séricos, ni los estudios de imagen han sido capaces de suplantar a la laparoscopia diagnóstica para el diagnóstico de la endometriosis. La apariencia histológica consiste de glándulas endometriales y estroma con cantidades variables de inflamación y fibrosis (12) .
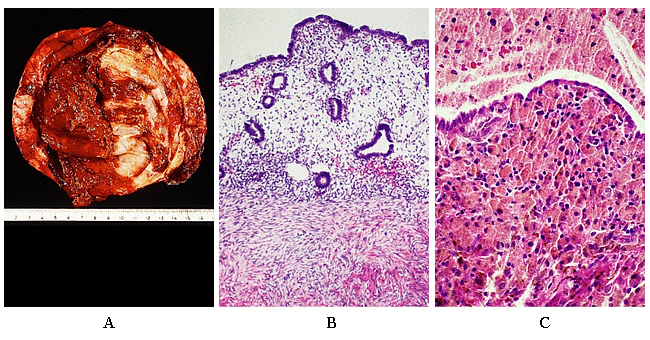
Figura 2. R: La superficie interior de un quiste en un caso de endometriosis ovárica. El color es típicamente marrón. B: la endometriosis ovárica. En este área de tejido del endometrio reproduce fielmente la apariencia de endometrio normal, tanto en términos de glándulas y estroma. C: aspecto común que resulta de una hemorragia repetida y la acumulación de macrófagos cargados de hemosiderina.
Sociedad Americana de Medicina Reproductiva; clasificación revisada de la endometriosis
Numerosos sistemas de clasificación han sido propuestos para describir la endometriosis anatómica y la severidad de la enfermedad. La Sociedad Americana de Medicina Reproductiva (ASRM) la clasificación, que es el sistema más utilizado, fue revisado por tercera vez en 1996, pero todavía tiene limitaciones (13) . El sistema no es un buen predictor del embarazo después del tratamiento a pesar de los ajustes a los puntajes y los puntos de corte para la etapa de la enfermedad. El sistema de la ASRM no se correlaciona bien con los síntomas de dolor y dispareunia o la infertilidad. El valor del sistema de ASRM revisado está en la grabación uniforme de los hallazgos operatorios y quizá para comparar los resultados de varias terapias.
| Peritoneum | Endometriosis | <1 cm | 1-3 cm | >3 cm |
|---|---|---|---|---|
| Superficial | 1 | 2 | 4 | |
| Deep | 2 | 4 | 6 | |
| Ovary | R-Superficial | 1 | 2 | 4 |
| Deep | 4 | 16 | 20 | |
| L-Superficial | 1 | 2 | 4 | |
| Posterior cul-de-sac obliteration |
Partial / Complete | |||
| 4 | 40 | |||
| Ovary | Adhesions | <1/3 Enclosure |
1/3-2/3 Enclosure |
>2/3 Enclosure |
| R-Filmy | 1 | 2 | 4 | |
| Dense | 4 | 8 | 16 | |
| L-Filmy | 1 | 2 | 4 | |
| Dense | 4 | 8 | 16 | |
| Tube | R-Filmy | 1 | 2 | 4 |
| Dense | 4* | 8* | 16 | |
| L-Filmy | 1 | 2 | 4 | |
| Dense | 4* | 8* | 16 |
*if the fimbriated end of the fallopian tube is completely enclosed, change the point assignment to 16. Denote appearance of superficial implant types as red [(R), red, red-pink, flame-like, vesicular blobs, clear vesicles], white [(W), opacifications, peritoneal defects, yellow-brown], or black [(B), black, hemosiderin deposits, blue]. Denote percent of total described as R_%, W_%, and B_%. Total should equal 100%.
- Stage I (minimal) 1-5;
- Stage II (mild) 6-15;
- Stage III (moderate) 16-40;
- Stage IV (Severe) >40
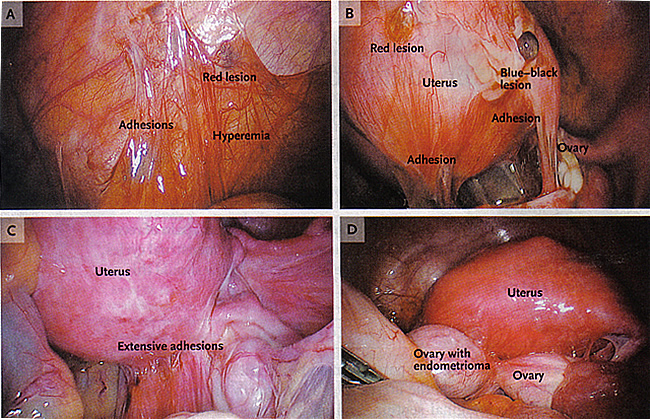
Figura 3. A: Muestra un implante endometriósico (lesión de color rojo), adherencias, y la hiperemia en el peritoneo. B: Los implantes peritoneales, como lesiones de color rojo y azul-negro y las adherencias. C: adherencias que distorsionan la anatomía pélvica normal. D: Un endometrioma adherida al útero posterior y distensión de la cápsula del ovario.
Objetivos de tratamiento de la endometriosis
La endometriosis tiene varias propiedades biológicas únicas. Se comporta como una enfermedad crónica y recurrente, debido a los implantes microscópicos que siguen activos después del tratamiento quirúrgico. Muchos pacientes tienen la enfermedad de reposo con episodios poco frecuentes de dolor, mientras que otros tienen dolor frecuente y recurrente. Estos diferentes patrones de síntomas a menudo no se correlacionan con el tamaño de la lesión o la extensión de la enfermedad. Los enfoques actuales para el manejo de la endometriosis son los síntomas orientado, dirigido principalmente a tratar el dolor pélvico crónico e infertilidad. Protocolos de gestión también puede estar dirigido a frenar la progresión de la enfermedad o prevenir la recurrencia. Medicina, cirugía, o un enfoque combinado puede ser elegido. Además, técnicas de reproducción asistida (ART) se utilizan con frecuencia para tratar la endometriosis asociada a infertilidad. Las estrategias de tratamiento para las mujeres con endometriosis varían según la edad del paciente, los objetivos del tratamiento, la paridad, la extensión de la enfermedad y el estado menopáusico. Para los pacientes jóvenes con enfermedad leve que no desean los niños, es recomendable utilizar la supresión médica para controlar los síntomas y reducir al mínimo las intervenciones quirúrgicas. Para las mujeres con una enfermedad grave que desean fertilidad, cirugía seguida de terapia antirretroviral es una opción razonable. Por último, la gestión de pacientes quirúrgicamente menopáusicas con endometriosis sintomática requiere un enfoque diferente, en el que el uso fuera de etiqueta de las nuevas terapias médicas, tales como inhibidores de la aromatasa, puede ser considerado.
Tratamiento médico de la endometriosis asociada a dolor
El dolor pélvico crónico representa el 10% de los pacientes ambulatorios visitas ginecológicas (14) . Una historia médica completa, quirúrgicos, sociales, y la familia se debe obtener de los pacientes que presentan este síntoma, y deben someterse a un examen físico que incluye un examen pélvico. El dolor focal y la ternura en el examen pélvico se asocia con la enfermedad pélvica en el 97% de los pacientes y con la endometriosis en el 66% de los pacientes (14). El dolor pélvico debido a la endometriosis suele ser crónica (que dura más de 6 meses) y está asociado con la dismenorrea (en 50% a 90% de los casos), dispareunia, dolor pélvico profundo, y dolor abdominal con o sin dolor de espalda y lomo. El dolor puede ocurrir de manera impredecible y de forma intermitente durante todo el ciclo menstrual o puede ser continuo, y puede ser sordo, palpitante o agudo, y exacerbada por la actividad física. La vejiga y del intestino de los síntomas asociados (náuseas, distensión y saciedad precoz) son típicamente cíclico. Con frecuencia el dolor empeora con el tiempo y puede cambiar de carácter, con frecuencia, las mujeres reportan ardor o hipersensibilidad, los síntomas que son indicativos de un componente neuropático. Los síntomas se superponen con los de varias otras condiciones ginecológicas (por ejemplo, enfermedad inflamatoria pélvica, adherencias pélvicas, los quistes ováricos o masas, leiomiomas y adenomiosis) y no ginecológicas condiciones y factores (por ejemplo, síndrome del intestino irritable, enfermedad inflamatoria del intestino, cistitis intersticial, dolor miofascial , la depresión, y una historia de abuso sexual), hace un reto diagnóstico. En la actualidad, el método definitivo para diagnosticar y clasificar la endometriosis y evaluar la recurrencia de la enfermedad después del tratamiento es la visualización durante la cirugía. La laparoscopia diagnóstica se utiliza comúnmente para el diagnóstico.
Tratamiento a largo plazo de los pacientes con dolor pélvico crónico asociados a la endometriosis consiste en ciclos repetidos de tratamiento médico, la terapia quirúrgica, o ambas cosas. En la mayoría de los casos, se repite el dolor dentro de 6 a 12 meses después de la finalización del tratamiento. Intervención quirúrgica conservadora se asocia con la recurrencia del dolor. Por lo tanto, el tratamiento médico se utiliza comúnmente para aliviar los síntomas de este trastorno crónico. Hay muchos aleatorios controlados con placebo que muestran la superioridad de estos fármacos sobre el placebo (15) . Al igual que con la cirugía, existe un importante "efecto placebo" y la recurrencia del dolor después de descontinuar el medicamento es alta. Tratamiento médico supresor no influye en la fertilidad. El director más importante a recordar es que el tratamiento médico es eficaz, pero que los síntomas tienden a recurrir con rapidez después de la terapia se detiene. Por lo tanto, primera línea de tratamiento médico debe centrarse en fármacos que pueden ser utilizados en el largo plazo (16).
Fármacos que se utilizan para el tratamiento de la endometriosis (16):
| Class of Drugs | Drug | Dosage |
| Androgen | Danazol * | 100-400 mg orally twice a day 100 mg per vagina daily |
| Aromatase inhibitor | Anastrozole Letrozole |
1 mg orally daily 2.5 mg orally daily |
| Estrogen - progestin combinations | Monophasic Estrogen-progestin* |
Low ethinyl estradiol dose continuously |
| Gonadotropin - releasing hormone agonist (GnRH) | Goserelin* Leuprolide depot* Nafarelin* |
3.6 mg SC monthly (10.8 mg IM every 3 mo) 3.75 mg IM monthly (11.25 mg IM every 3 mo) 200 mcg intranasally twice a day |
| Gonadotropin - releasing hormone agonist | Cetrorelix | 3 mg SC weekly |
| Progestin | Depo-subQ Provera 104* Dienogest Etonogestrel-releasing implant Levonorgestrel-releasing IUS Medroxyprogesterone acetate Norethindrone acetate* |
104 mg/0.65 mL SC every 3 mo 2 mg daily 1 for 3 years 1 for 5 years 30 mg orally daily for 6 months, then 100 mg IM every 2 weeks for 2 months, then 200 IM monthly for 4 months 5 mg daily |
SC, subcutaneously; IM, intramuscularly; IUS, intrauterine system.
* FDA-approved for endometriosis.
With add-back, i.e., norethindrone acetate 5 mg daily plus vitamin D 800 international units daily plus calcium 1.25 g daily.
Dienogest is a 19-nortestosterone derivative that is approved in the European Union for treatment of endometriosis. It is not available in the United States as a separate drug. It is available only in the oral contraceptive Natazia (Bayer HealthCare Pharmaceuticals; estradiol valerate/dienogest), which is a newer, four-phasic pack that contains dienogest.
Terapia quirúrgica: Abordajes quirúrgicos para aliviar el dolor relacionado con la endometriosis puede ser utilizado como terapia de primera línea o iniciado después del fracaso de los tratamientos médicos (17). Los procedimientos quirúrgicos incluyen la escisión, fulguración, o la ablación con láser de los implantes endometriósicos en el peritoneo, la escisión o el drenaje o la ablación de los endometriomas, la resección de nódulos rectovaginales, la lisis de adherencias y la interrupción de las vías nerviosas. Los ensayos aleatorizados y controlados han demostrado que a los 6 meses, la ablación laparoscópica de los implantes endometriósicos es de 65% de efectividad en la reducción del dolor, en comparación con una tasa de 22% de reducción del dolor asociado a la laparoscopia diagnóstica solos (18). Un estudio pequeño que comparó la ablación laparoscópica con el tratamiento de los agonistas de GnRH mostró una reducción del dolor similar con los dos enfoques (19). La recurrencia de la terapia del dolor que requiere es común (en el 30% a 60% de los pacientes) en un plazo de 6 a 12 meses después del tratamiento (19) . Una estrategia alternativa para el control de la endometriosis es el dolor relacionado con la interrupción de las vías nerviosas. Considerando que la ablación de un segmento de la ligamentos uterosacros no ha demostrado su eficacia, los ensayos aleatorizados y controlados han demostrado la superioridad de la ablación laparoscópica de tejido endometrial en combinación con la neurectomía presacra (extirpación del manojo de nervios dentro de los límites del triángulo interiliac) sobre la ablación laparoscópica sola en la mejora de la dismenorrea y la reducción del dolor severo línea media (20) . Historias de casos han demostrado que la histerectomía con salpingo-ooforectomía bilateral un alivio del dolor en el 80% a 90% de las mujeres con síntomas debilitantes que eran refractarios a las intervenciones quirúrgicas médicas u otras, el dolor se informó que se repitan en el 10% de las mujeres dentro de 1 a 2 años después de la cirugía (21) . Post-operatorio de reemplazo hormonal debe incluir tanto el estrógeno y un progestágeno, ya que el estrógeno por sí solo puede estimular el crecimiento de la enfermedad microscópica.
Tratamiento médico coadyuvante: En las mujeres con enfermedad avanzada (estadios III o IV), dismenorrea moderada a severa, y no cíclico dolor en la pelvis, después de la operación el tratamiento médico puede mejorar el manejo del dolor, proporcionando el control de la enfermedad recurrente o residual microscópica. Un meta-análisis de seis estudios clínicos aleatorizados que compararon 3 a 6 meses de tratamiento postoperatorio con un agonista de la hormona liberadora de gonadotropina (GnRH), danazol, o los anticonceptivos orales combinados con ningún tratamiento postoperatorio de placebo reveló una reducción significativa en las puntuaciones de dolor a la conclusión de de la terapia en los grupos de tratamiento activo, aunque los beneficios son incompatibles con mayor tiempo de seguimiento (18 meses) después de la discontinuación de la terapia (22) . El intervalo promedio entre la cirugía y la recurrencia de los síntomas que requieren una terapia alternativa fue significativamente mayor en pacientes que recibieron tratamiento postoperatorio con agonistas de la GnRH (> 24 meses) que para los pacientes que recibieron placebo (12 meses) (22) .
Tratamiento de la endometriosis asociada a infertilidad
A pesar de que las causas de la endometriosis asociada a infertilidad o subfertilidad permanecen en la oscuridad, una cosa es segura, sub-fértiles las mujeres tienen endometriosis en una mayor prevalencia, 20% -50%, a mujeres en edad reproductiva que no busca un tratamiento de fertilidad (23) . En un estudio de las mujeres infértiles, la distribución de la incidencia fue sorprendentemente robusto para la mínima a los casos leves a 68%, mientras que las mujeres con moderada a severa, la enfermedad constituye el 32% restante (24) . El sistema de clasificación actual no es útil para predecir las tasas de embarazos espontáneos (16). La tasa de fecundidad mensual para aquellas mujeres con endometriosis se 0.02-0.10 0.15-0.20 en comparación con las parejas fértiles, aunque la tasa no es necesariamente menor que en aquellos pacientes con subfertilidad de causa desconocida (16) . No hay evidencia de una asociación con la pérdida recurrente de embarazo. Uso de la terapia médica en la forma de la supresión ovárica para la etapa I o II, la endometriosis no mejora las tasas de fecundidad y no se les debe ofrecer (25) . Complementar el tratamiento después de la cirugía laparoscópica para el estadio III o IV de la endometriosis con GnRH no parece ser superior a la conducta expectante en términos de tasas de concepción natural en un niño de 5 años de seguimiento en un ensayo controlado aleatorio (26) .
El tratamiento quirúrgico de la endometriosis infertilidad relacionada con sí mejora las tasas de embarazo, pero la magnitud de la mejora no es clara. La escisión del endometrioma es más eficaz que el drenaje simple y la ablación de la pared del quiste. Debido a que la mayoría de los endometriomas pueden ser identificados por ecografía, el número de laparoscopias necesarios para lograr resultados es el mismo. Es importante en toda la cirugía para la eliminación de endometriomas de que se informe al paciente que la cirugía puede dañar los ovarios y reducir la reserva ovárica (27) . El valor de la escisión de la endometriosis profunda únicamente para mejorar el embarazo no está clara y puede afectar negativamente la fertilidad. Después de la cirugía inicial, sin éxito para la endometriosis asociada a infertilidad, fertilización in vitro (FIV) es la mejor opción en lugar de reintervención menos que el dolor sigue siendo un problema importante. Cirugía ovárica repetitivo se ha demostrado que tienen un impacto negativo significativo en los resultados de FIV (27) . La terapia de gonadotropina y la inseminación intrauterina, así como la fecundación in vitro, son tratamientos eficaces en mujeres con infertilidad y endometriosis (28) . En un gran ensayo aleatorio que comparó cuatro estrategias de tratamiento en 932 parejas en estadio I o II de endometriosis o infertilidad inexplicable, las tasas acumulativas de embarazo durante cuatro ciclos de tratamiento fueron los siguientes: la inseminación intracervical (10%), la inseminación intrauterina (18%), la terapia de gonadotropina y inseminación intracervical (19%), y la gonadotropina y la inseminación intrauterina (33%) (16), (29). La ablación de las lesiones de endometriosis con la lisis de las adherencias se recomienda para el tratamiento de la infertilidad relacionada con endometriosis a la etapa I o II.
Las principales directrices de las Sociedades Profesionales para el Diagnóstico y Manejo de la endometriosis relacionada con el dolor y la infertilidad * (7), (21), (28):
| Condition | Recommendation |
| Pain Diagnosis |
Surgery is preferred method for the diagnosis of pelvic pain and a pelvic mass (e.g. endometrioma), but it is not required before initiating empirical therapy, after consideration of other conditions in a differential diagnosis. There should be a low threshold for the evaluation of endometriosis in adolescents because the diagnosis is often missed in this age group. |
| Treatment | Initial treatment is a trial of non-steroidal anti-inflammatory drugs and hormonal therapy (combined oral contraceptives). All hormonal drugs that have been studied (combined oral contraceptives, progestins, GnRH agonists, and danazol) are similarly effective, but their side effects and costs differ. If a GnRH agonist is used, estrogen-progestin add-back therapy is recommended; GnRH agonists are not recommended for adolescents because of their effects on bone. The levonorgestrel intrauterine system is effective in selected patients. Laparoscopic uterosacral nerve ablation is not effective. |
| Infertility Diagnosis |
Both the male and female partner should undergo a full evaluation. |
| Treatment | Super-ovulation with intrauterine insemination provides benefit. Ovarian suppression is not effective in promoting spontaneous pregnancy. The use of GnRH agonist for 3-6 months before IVF and surgical ablation of endometriosis for stage I or II disease are beneficial. Excision of endometriomas >3cm in diameter is of benefit, although there is potential for diminished ovarian reserve. |
* Guidelines are from the American Society for Reproductive Medicine and the European Society of Human Reproduction and Embryology. GnRH denotes gonadotropin-releasing hormone; IVF denotes in-vitro fertilization.
Data on the diagnosis and management of chronic pelvic pain and the treatment of adolescents with pelvic pain are from the American College of Obstetricians and Gynecologists.
Reproducción Asistida y la endometriosis
En el tratamiento de la infertilidad asociada a la endometriosis, un enfoque por etapas que se utilizan habitualmente. Manejo de la endometriosis asociada a infertilidad implica una combinación de tratamiento expectante, la cirugía, la estimulación ovárica controlada (COS), la inseminación intrauterina, y avanzadas técnicas de reproducción asistida (ART). El uso de COS, con o sin inseminación intrauterina puede ser beneficioso para un curso corto de terapia en pacientes con endometriosis con la permeabilidad tubárica. Si COS no da lugar a un embarazo, la FIV es un paso prudente. Si la cirugía inicial no puede restaurar la fertilidad en pacientes con moderada (estadio III) o grave (estadio IV) relacionada con la endometriosis infertilidad, fertilización in vitro es una alternativa eficaz. La reproducción de los pacientes asintomáticos ofrece poco beneficio adicional cuando se trata de la infertilidad (30) . Los pacientes con endometriosis parece tener la respuesta ovárica a las gonadotropinas reducida y la necesidad de una mayor dosis de gonadotropinas para la FIV (30) . No está claro si la presencia o el grado de la endometriosis se asocia con deterioro de la calidad de los ovocitos o la fertilización y la tasa de implantación (31) . El efecto de la cirugía de la endometriosis en el resultado de sucesivos ciclos de FIV se ha estudiado, y los análisis de regresión han demostrado que el intervalo de tiempo entre la cirugía y la recuperación de los ovocitos no afecta a las tasas de implantación en pacientes con endometriosis sometidas a FIV (32) .
La endometriosis en adolescentes
Raros casos de endometriosis en pacientes premenárquicas se han descrito, pero la edad promedio al momento de presentación de la endometriosis es de 15,9 años (33). Aproximadamente el 70% de los adolescentes con dolor pélvico que no responden a terapia médica convencional tiene endometriosis (33) . La mayoría de los casos en los adolescentes puede ser diagnosticada sobre la base de la historia y examen físico. Los síntomas sugestivos de endometriosis que resultan en un diagnóstico de presunción incluyen dolor constante cíclico, dismenorrea, menstruaciones irregulares, y la dispareunia profunda. El dolor suele ser grave, perjudicial e interfiere con la escuela, los deportes y otras actividades sociales. El examen físico de un adolescente con endometriosis pueden variar de un examen normal de la pelvis o dolor generalizado masa anexial persistente. El hallazgo clásico de la endometriosis pélvica es un útero en retroversión fija con la cicatrización y posterior sensibilidad hacia el útero. La característica de nodularidad de los ligamentos útero sacros y del fondo de saco, se puede palpar en un examen rectovaginal en aproximadamente un tercio de las mujeres con la enfermedad. Los ovarios pueden estar inflamados y sensibles y con frecuencia se fija en los ligamentos anchos o pared pélvica lateral. El diagnóstico definitivo se realiza mediante la visualización laparoscópica de las lesiones de endometriosis. Los adolescentes suelen tener lesiones claras, rojo, blanco, marrón y amarillo-con más frecuencia que las lesiones de color negro o azul.
Dirección Médica: no esteroides anti-inflamatorios no esteroideos (AINE) y analgésicos se pueden utilizar otros para disminuir el dolor asociado con la endometriosis. AINE trabajar para limitar la producción de prostaglandinas, que son producidos en exceso en los implantes endometriósicos. También funcionan para interrumpir el mecanismo de retroalimentación positiva que implica la producción de prostaglandinas local que es responsable de más crecientes niveles de estrógeno en las células del endometrio ectópico (34) . El resultado es una disminución en la producción de estrógenos, sino también una disminución de la respuesta inflamatoria. Las píldoras anticonceptivas orales (ACO) son clásicamente tratamiento de primera línea en los adolescentes debido a la baja perfil de efectos secundarios y el beneficio secundario de la prevención del embarazo no deseado. ACO disminuir el endometrio y por lo tanto disminuir la cantidad de tejido que produce prostaglandinas. AO debe ser prescrito como un proceso continuo, no cíclico régimen. Esto disminuirá la hemorragia de retiro de números, lo que minimiza la aparición de los síntomas. Alternativamente, AO puede inducir amenorrea, resultando en la posterior regresión de los síntomas. El tratamiento con ACO es represivo, pero no curativa (35) .
Los agentes de progesterona incluyen acetato de medroxiprogesterona de depósito o, por vía oral 19-nortestosterona derivados, tales como acetato de noretisterona y norgestrel, y levonorgesterol liberadora de dispositivo intrauterino. Estos agentes de limitar la producción de estrógeno, decidualization causa de tejido endometrial ectópico, y, posteriormente, dar lugar a la atrofia de las células endometriales. Danazol disminuye el volumen de tejido endometrial ectópico mediante la inducción de estado de hiperandrogenismo. A pesar de ser muy eficaz, los efectos secundarios androgénicos son considerables e irreversibles. Los agonistas de GnRH crear un ambiente hipoestrogénico, hipogonadismo y la posterior baja regulación de la secreción de gonadotropinas que resulta en la producción de estrógeno disminuye. Los efectos secundarios que limitan el uso de agonistas de GnRH incluyen sofocos, insomnio, disminución de la densidad ósea. Add-back con acetato de noretisterona se recomienda para evitar graves secuelas a largo plazo (36) . Aromatasa media de la conversión de androstenediona a estrona y la testosterona en estradiol (34), (37) . Inhibidores de la aromatasa bloquean el estrógeno local producida por los tejidos del endometrio, destruyendo así el centro de coordinación de retroalimentación para el crecimiento del endometrio ectópico. Aunque no hay ensayos controlados aleatorios que compararon inhibidores de la aromatasa con el tratamiento médico tradicional de la endometriosis, los estudios experimentales que utilizan inhibidores de la aromatasa con el add-back progestinas o ACO han demostrado una reducción significativa en la endometriosis asociada a dolor pélvico (37).
Tratamiento quirúrgico: Sólo el tratamiento conservador en el que los órganos reproductivos se conservan se indica en los adolescentes. La resección quirúrgica de enfermedad visible puede llevarse a cabo mediante técnicas de escisión, fulguración, y la ablación. Dependiendo de la localización, profundidad de la invasión, y el grado de cicatrización y la inflamación, las técnicas versátiles son aplicables. Conservación de la capacidad reproductiva es de suma importancia en la población adolescente. La ablación de los depósitos endometriales disminuye el dolor, con o sin ablación del nervio uterino laparoscópica. Neurectomía presacra, un procedimiento en el que los nervios simpáticos del útero se divide, puede disminuir el dolor abdominal, la línea media. La ablación de las células endometriales ectópicos también pueden aumentar la fertilidad futura de los adolescentes con endometriosis.
La endometriosis afecta a los órganos reproductivos no
Extrapélvica endometriosis ha sido reportada en una variedad de sitios, incluida la parte superior del abdomen, el diafragma, la pared abdominal (especialmente el ombligo), el perineo (cicatriz de episiotomía), y el tórax (38). Los sitios remotos de la endometriosis, como en el pulmón, el antebrazo, el muslo, la columna vertebral, y la nariz también han sido reportados (39) . Tal vez esto es resultado de trasplante de hematológica o linfática de las células endometriales. De hecho, el 30% de las mujeres con endometriosis tienen la enfermedad en los ganglios linfáticos de la pelvis (39) . El desarrollo real de la endometriosis probablemente depende más de un mecanismo de origen. Además, la endometriosis puede invadir todo el espesor del recto, el intestino grueso y delgado, la uretra o la vejiga. Los síntomas que están asociados con la endometriosis en estos sitios varían dependiendo de la ubicación y la profundidad de la infiltración y el incluir a las mujeres con episodios cíclicos de hematuria macroscópica, hemtochezia y hemoptisis. A pesar de una serie de enfoques terapéuticos han sido utilizados para las mujeres con endometriosis extrapélvico presunta, la eficacia informó de la supresión ovárica con agonistas de la GnRH parece apoyarla en la primera línea de tratamiento, excepto en los casos de obstrucción del uréter o el intestino, que son los mejores tratados quirúrgicamente (38) . Incluso en algunos casos de endometriosis rectovaginal, el tratamiento médico de supresión puede aliviar el dolor (40) . La experiencia con el manejo de estos casos se limita a una serie de casos, a menudo de un solo centro.
A largo plazo de seguimiento
Los síntomas pueden reaparecer en las mujeres, incluso después de la histerectomía y la ooforectomía. La endometriosis puede recurrir hasta en un 15% de las mujeres si los pacientes son tratados con terapia de estrógenos después de la ooforectomía bilateral (38) . En consecuencia, la terapia hormonal con estrógenos no está contraindicado después de la cirugía definitiva para la endometriosis. Aunque la verdadera tasa de recurrencia es desconocida, en los pacientes con síntomas recurrentes sometidos a un procedimiento quirúrgico, las lesiones de endometriosis puede ser demostrada. El sitio más común de lesiones recurrentes es el intestino grueso y delgado (38) . Estas lesiones se probable presentes en el momento de la cirugía y no extirpados. Estas lesiones pueden ser considerados una enfermedad persistente enfermedad más recurrente. La persistencia de la enfermedad en los estados hipoestrogénicas es más probable debido a la expresión local de la actividad de la aromatasa. El tratamiento es difícil ya menudo requiere cirugía. El uso de agonistas de la GnRH en esta situación de hipoestrogenemia no parece que sean de utilidad. Los inhibidores de aromatasa pueden ser considerados, pero no son uniformemente eficaz (41) .
Actualmente, hay datos limitados sobre el tiempo de la terapia de estrógeno después de la histerectomía con salpingo-ooforectomía bilateral para la endometriosis. Al parecer, no hay ninguna ventaja en términos de tasa de recurrencia, para retrasar el tratamiento con estrógenos después de la cirugía (42) . Hay pocos datos que indiquen que la terapia hormonal puede estimular el crecimiento de cáncer de ovario residual o tejido del endometrio después de la histerectomía total y salpingo-ooforectomía bilateral, si todas las enfermedades visibles se retiró (42) . También hay una preocupación por la posibilidad de estrógeno inducida por transformación maligna de los implantes de endometriosis residual. Esto ha llevado a algunos médicos para recomendar el agregado de rutina de un progestágeno a la terapia de estrógeno. Sin embargo, no hay evidencia basada en los resultados para apoyar esta recomendación. En las mujeres con menopausia quirúrgica o espontánea con el útero intacto, el tratamiento con progesterona es necesaria si se administran estrógenos. No parece haber un mayor riesgo de cáncer de ovario en pacientes con endometriosis, aunque no está claro por qué magnitud. Recientemente se ha informado que tiene una razón de tasas de 1,6 (intervalo de confianza 95% 1.12 a 2.9) (43) . Sin embargo, los precursores, tales como citológico o histológico atipia son poco frecuentes (44) .
Resumen
Numerosos tratamientos médicos están disponibles para tratar la endometriosis. La evidencia actual es insuficiente para apoyar la superioridad de un tratamiento sobre otro. Es importante tener en cuenta la preferencia del paciente en el enfoque de tratamiento y para proporcionar un asesoramiento adecuado sobre los riesgos, efectos secundarios y el costo, ya que la endometriosis es una enfermedad crónica que requiere tratamiento a largo plazo. Tratamiento médico supresor mejora los síntomas de dolor, sin embargo, las tasas de recidiva son altas después de la medicación se interrumpe. Se observa una clara mejoría a corto plazo en el dolor después del tratamiento quirúrgico conservador, sin embargo, como con el tratamiento médico, también existe una importante tasa de recurrencia del dolor. Ni la terapia médica ni quirúrgica de forma permanente a aliviar los síntomas asociados a la endometriosis. La terapia de combinación que implica la laparoscopia diagnóstica y terapéutica con el tratamiento médico es probable que proporcionan los resultados más óptimos. Varios informes muestran tasas de recurrencia oscila entre el 16% a 52%. Estas tarifas pueden ser diferentes en el resultado de los protocolos de tratamiento variables, diferentes métodos de diagnóstico de la recurrencia e inconsistente de seguimiento. Las evaluaciones periódicas de intervalo se recomienda para hacer frente a la naturaleza crónica de la endometriosis. Debido a la naturaleza crónica de la enfermedad y el impacto sobre la fertilidad en el futuro, el apoyo psicosocial es muy importante para esta población de mujeres. El tratamiento quirúrgico de la endometriosis infertilidad relacionada con sí mejora las tasas de embarazo, pero la magnitud de la mejora no es clara. La escisión de un endometrioma es superior a la simple drenaje y la ablación de la pared del quiste. Cuando el alivio del dolor del tratamiento con agonistas de la GnRH compatible con la terapia continuada, la adición de terapia add-back reduce o elimina la GnRH agonista inducida por la pérdida mineral ósea y proporciona un alivio sintomático, sin reducir la eficacia del alivio del dolor. Cuando el tratamiento médico ha fracasado, sometidos a tratamiento quirúrgico definitivo es apropiado en aquellos que no desean fertilidad futura.
Referencias
- Giudice LC, Kao LC. Endometriosis. Lancet 2004;364:1789-1799
- Kennedy S, Bergqvist A, Charon C, et al. ESHRE Special Interest Group for Endometriosis and Endometrium Guideline Development Group. ESHRE guideline for the diagnosis and treatment of endometriosis. Hum Reprod 2005;20:2698-2704
- Balasch J, Creus M, Fabregues F, et al. Visible and non-visible endometriosis at laparoscopy in fertile and infertile women and in patients with chronic pelvic pain: a prospective study. Hum Reprod 1996;11:387-391. (Level II-3)
- Bedaiway MA, Falcone T, Mascha EJ, et al. Genetic polymorphism in the fibrinolytic system and endometriosis. Obstet Gynecol 2006;108:162-168. (Level II-2)
- Giudice LC, Swiersz LM, Burney RO. Endometriosis. In: Jameson JL, DeGroot LJ, eds. Endocrinology. 6th ed. New York: Elsevier, 2010:2356-2370
- Bulun SE. Endometriosis. N Engl J Med 2009;360:268-279
- Giudice LC. Endometriosis. N Eng J Med 2010;362(25):2389-2398
- Lebovic DI, Mueller MD, Taylor RN. Immunobiology of endometriosis. Fertil Steril 2001;75:1-10
- Stratton P, Berkley KJ. Chronic pelvic pain and endometriosis: translational evidence of the relationship and implications. Hum Reprod Update 2011;17:327-346
- Lemons NA, Arbo E, Scalco R, et al. Decreased anti-Müllerian hormone and altered ovarian follicular cohort in infertile patients with mild/minimal endometriosis. Fertil Steril 2008;89:1064-1068
- Mansour G, Aziz N, Sharma R, et al. The impact of peritoneal fluid from healthy women and from women with endometriosis on sperm DNA and its relationship to the sperm deformity index. Fertil Steril 2009;92:61-67
- Walter AJ, Hentz JG, Magtibay PM, et al. Endometriosis: correlation between histologic and visual findings at laparoscopy. Am J Obstet Gynecol 2001;184:1407-1411; discussion 1411-1413. (Level II-3)
- Revised American Society for Reproductive Medicine classification of endometriosis: 1996. Fertil Steril 1997;67:817-821. (Level III)
- ACOG Practice Bulletin no. 51: chronic pelvic pain. Obstet Gynecol 2004;103:589-605
- Vercellini P, Crosignani P, Somigliana E, et al. Waiting for Godot: a commonsense approach to the medical treatment of endometriosis. Hum Reprod 2011;26:3-13
- Falcone T, Lebovic DI. Clinical management of endometriosis. Obstet Gynecol 2011;118:691-705
- Jacobson TZ, Duffy JM, Barlow D, et al. Laparoscopic surgery for pelvic pain associated with endometriosis. Cochrane Database Syst Rev 2009;4:CD001300
- Berkley KJ, Rapkin AJ, Papka RE. The pains of endometriosis. Science 2005;308:1587-1589
- Prentice A, Deary AJ, Goldbeck-Wood S, et al. Gonadotrophin-releasing hormone analogues for pain associated with endometriosis. Cochrane Database Syst Rev 2000;2:CD000346
- Proctor ML, Latthe PM, Farquhar CM, et al. Surgical interruption of pelvic nerve pathways for primary and secondary dysmenorrhea. Cochrane Database Syst Rev 2005;4:CD001896
- Idem. Treatment of pelvic pain associated with endometriosis. Fertil Steril 2008;90:Suppl:S260-S269
- Yap C, Funress S, Farquhar C. Pre- and post-operative medical therapy for endometriosis surgery. Cochrane Database Syst Rev 2004;3:CD003678
- Ozkan S, Murk W, Arici A. Endometriosis and infertility: epidemiology and evidence-based treatment. Ann N Y Acad Sci 2008;1127:92-100
- DHooghe TM, Debrock S, Hill JA, Meuleman C. Endometriosis and subfertility: is the relationship resolved? Semin Reprod Med 2003;21:243-254
- Hughes E, Brown J, Collins JJ, et al. Ovulation suppression for endometriosis. Cochrane Database Syst Rev 2007;3:CD000155
- Loverro G, Carriero C, Rossi AC, et al. A randomized study comparing triptorelin or expectant management following conservative laparoscopic surgery for symptomatic stage II-IV endometriosis. Euro J Obstet Gynecol Biol 2008;136:194-198
- Busacca M, Vignali M. Endometrioma excision and ovarian reserve: a dangerous relation. J Minim Invasive Gynecol 2009;16:142-148. (Level III)
- Practice Committee of the American Society for Reproductive Medicine. Endometriosis and infertility. Fertil Steril 2006;86:Suppl:S156-S160
- Barnhart K, Dunsmoor-Su R, Coutifaris C. Effect of endometriosis on in vitro fertilization. Fertil Steril 2002;77:1148-1155
- Mahutte NG, Arici A. Endometriosis and assisted reproductive technologies: are outcomes affected? Curr Opin Obstet Gynecol 2001;13:275-279
- Bedaiwy M, Shahin AY, AbulHassan AM, et al. Differential expression of follicular fluid cytokines: relationship to subsequent pregnancy in IVF cycles. Reprod Biomed Online 2007;15:321-325
- Bedaiwy MA, Falcone T, Katz E, et al. Association between time from endometriosis surgery and outcome of in vitro fertilization cycles. J Reprod Med 2008;53:161-165
- Laufer MR, Sanfilippo J, Rose G. Adolescent endometriosis: diagnosis and treatment approaches. J Pediatr Adolesc Gynecol 2003;163(3 Suppl):S3-S11
- Hartel Z. Dysmenorrhea in adolescents and young adults: etiology and management. J Pediatr Adolesc Gynecol 2006;19(6):363-371
- Doyle JO, Missmer SA, Laufer MR. The effect of combined surgical-medical intervention on the progression of endometriosis in an adolescent and young adult population. J Pediatr Adolesc Gynecol 2009;22(4):257-263
- Vercellini P, Fedele L, Pietropaolo G, et al. Progestogens for endometriosis: forward to the past. Hum Reprod Update 2003(9(4):387-396
- ACOG. ACOG Committee Opinion: Aromatase inhibitors in gynecologic practice. Obstet Gynecol 2008;112(2 Part 1):405-407
- ACOG Practice Bulletin. Management of endometriosis. Number 114, July 2010. Obstet Gynecol 2010;116:223-236
- Laufer MR. Current approaches to optimizing the treatment of endometriosis in adolescents. Gynecol Obstet Invest 2008;66 (Suppl 1):19-27
- Vercellini P, Somigliana E, Vigano P, et al. Surgery for endometriosis-associated infertility: a pragmatic approach. Hum Reprod 2009;24:254-269. (Level III)
- Bohrer J, Chen CC, Falcone T. Persistent bilateral ureteral obstruction secondary to endometriosis despite treatment with an aromatase inhibitor. Fertil Steril 2008;90:2004.e7,2004.e9. (Level III)
- Matorras R, Elorriaga MA, Pijoan JI, et al. Recurrence of endometriosis in women with bilateral adnexectomy (with or without total hysterectomy) who received hormone replacement therapy. Fertil Steril 2002;77:303-308. (Level I)
- Aris A. Endometriosis-associated ovarian cancer: a ten year cohort study of women living in the Estric Region of Quebec, Canada. J Ovarian Res 2010;3:2
- Bedaiwy MA, Hussein MR, Bicotti C, Falcone T. Pelvic endometriosis is rarely associated with ovarian borderline tumors, cytologic and architectural atypia: a clnicopathologic study. Pathol Oncol Res 2009;15:81-88
Publicado: 25 June 2012
Dedicated to Women's and Children's Well-being and Health Care Worldwide
www.womenshealthsection.com


