Клиническое ведение Эндометриоз
WHEC практики Бюллетень и клинических управления Руководство для медицинских работников. Образования гранта, предоставленного здоровья женщин-образовательный центр (WHEC).
Эндометриоз является хроническим и рецидивирующим репродуктивные расстройства с переменным клинических проявлений. Управление варьируется в зависимости от возраста больного, симптомов, степени заболевания, репродуктивных целей, лечения рисков, побочных эффектов и стоимости. Это довольно распространенное хроническое расстройство гинекологических, что обычно представляет с хронической тазовой боли или бесплодия. Наличие жизнеспособных, чувствительных к эстрогену, эндометрия, как желез и стромы связано с воспалительным ответом вне матки глобально называют эндометриоза. Несмотря на девять десятилетий прошло с тех пор она была впервые описана Сэмпсон, эндометриоз по-прежнему загадочным расстройством в силу своих разнообразных клинических проявлений и противоречивых этиологического происхождения. После эндометриоз диагностируется репродуктивного возраста женщины, ее следует рассматривать как хроническое заболевание с несколькими повторяющимися эпизодами боли, бесплодие, и более симптомов интервалы. Ежегодные затраты на лечение эндометриоза составляет более $ 20 миллиардов. Три подтипа эндометриоз различаются по валовой и микроскопический контроль, состоящий из эндометриоза (кисты яичников), поверхностных эндометриоидных имплантатов (фокус заболевания прежде всего, на брюшине), и глубоко проникает эндометриоза (ректовагинальной узелки). Каждая форма может иметь свой собственный этиологии или доли происхождения с другими формами этой болезни распространенных хронических гинекологических.
Цель этого документа заключается в анализе вещества, используемые в медицинских управления эндометриоз и обсудить использование вспомогательных техника воспроизведения (АРТ) для пациенток с эндометриозом желающих беременности. Этиологии, связь между степенью заболевания и степени симптомы, влияние на фертильность, и наиболее подходящее лечение эндометриоза остаются неполными. В обзоре также представлены доказательства, в том числе риски и выгоды, для повышения эффективности медицинской и хирургической терапии для взрослых женщин, которые являются симптомами с боли в области таза и бесплодия или обоих. Последний подход используя различные имеющиеся медицинские и хирургические методы лечения обсуждаются, поскольку они непосредственно относятся к подростковому населению. Эндометриоз является относительно распространенным хроническим заболеванием гинекологических, что обычно представляет с хронической тазовой боли или бесплодия. Социальный эффект этого расстройства является огромным, как в денежной стоимости и качества жизни.
Заболеваемость:
Эта загадочная болезнь поражает 6-10% репродуктивного возраста женщины и был обнаружен у женщин в возрасте от 12 до 80 лет (1) . Средний возраст постановки диагноза составляет около 28 лет (2) . Показатель распространенности на 38% (диапазон 20-50%) находится у бесплодных женщин и 71-87% женщин с хронической тазовой боли (3) . В отличие от долгих размышлений, нет никаких данных в пользу того, что заболеваемость эндометриозом растет, хотя и улучшенное распознавание патологии эндометрия, возможно, привело к увеличению скорости обнаружения. Там также, кажется, не особенно расовой предрасположенности к эндометриоз. Семейная ассоциация эндометриоза было предложено, и у пациентов с пострадавшим первой степени родства имеют почти 7 до 10-кратным увеличением риска развития эндометриоза (4) . Предлагаемая наследования характерна для полигенных-многофакторный механизм. Ряд генетических полиморфизмов были определены. В Соединенных Штатах, по оценкам, расходы на диагностику и лечение эндометриоза связанных боли и бесплодие составил $ 22 млрд. в 2002 году (7) . Учитывая известную частоту рецидивов эндометриоза в течение долгого времени, без медикаментозной терапии, больше женщин, вероятно, будет иметь свои эндометриоз трек на прогрессирование заболевания, а не разрешение. Кроме того, болевые ощущения не обязательно коррелирует с указанием повреждений. Механизмы, ответственные за выражение текущих симптомов вероятно, являются сложными и многофакторная.
Патофизиология:
Большинство экспертов согласны, что это заболевание является многофакторной в этиологии. Многолетний постулаты включают ретроградной менструации с обратным холодильником растворителем насаждения на тазовых структур, полостные широкого спектра действия мезотелиальной клеток, выстилающих брюшине проходит метаплазии в ткани эндометрия и имплантации клеток гематогенным путем или лимфатическую эмболизации. Тем не менее, загадка остается: почему заболевания развиваются у некоторых женщин, а в других нет? Более глубокое понимание молекулярных механизмов, связанных с эндометриозом расширил традиционные теории. Последние достижения в отношении этиологии эндометриоза должна применяться разумно в клинической практике для достижения оптимальных результатов лечения. Ретроградная пересаженные ткани эндометрия и клетки прикрепляются к поверхности перитонеальных, установить кровоснабжение, и вторгнуться в близлежащих структур (5) . Они проникли сенсорных, симпатических и парасимпатических нервов и вызывает воспалительную реакцию. Эндометриоидных имплантатов вырабатывать эстрадиол (E2), а также простагландина Е2 (PGE2), агенты, которые привлекают макрофаги (моноциты белка хемотаксиса 1 [MCP-1]), нейротрофические пептиды (фактор роста нервов [NGF]), ферменты для реконструкции тканей (матричных металлопротеиназ [ММП]) и тканевых ингибиторов ММП (TIMPs) и проангиогенных веществ, таких как фактор роста эндотелия сосудов (VEGF) и интерлейкина-8 (6) . Поражений выделяют haptogobin, что уменьшает адгезию макрофагов и фагоцитарной функции. Поражения и активированные макрофаги, которые в изобилии в перитонеальной жидкости у женщин с эндометриозом, а также выделять провоспалительных цитокинов (ИЛ-1β, ИЛ-8, интерлейкин-6 и фактора некроза опухоли-α [TNF-α]). Местные (и системные) эстрадиола может стимулировать поражение производства PGE2, который может активировать болевые волокна, повышения нейронов вторжения поражений, стимулируя производство NGF и других нейротрофинов, а также способствовать прорастания ноцицепторов, которые способствуют стойкие воспалительные боли и подавляют апоптоз нейронов. Эндометрия фактором кровотечений (EBAF) не правильно выразился и может привести к маточным кровотечением. Бесплодие результате токсического воздействия воспалительного процесса в половых клеток и эмбрионов, нарушение функции фимбриальные и эктопического эндометрия, которые устойчивы к действию прогестерона, и, таким образом, эндометрий, неблагоприятных для имплантации эмбриона (7) . HoxA10 и HoxA11 генов и V 3 интегрин не последнюю регулируются прогестерона, и, таким образом, эндометрий, неблагоприятных для имплантации эмбриона. Эндокринную систему химикатов может внести вклад в сопротивление прогестерон и, возможно, иммунной дисфункции (7) . ERFFI1 (ErbB рецепторов ингибитор обратной связи 1) конститутивно выразил и есть избыток митогенных сигнализации.
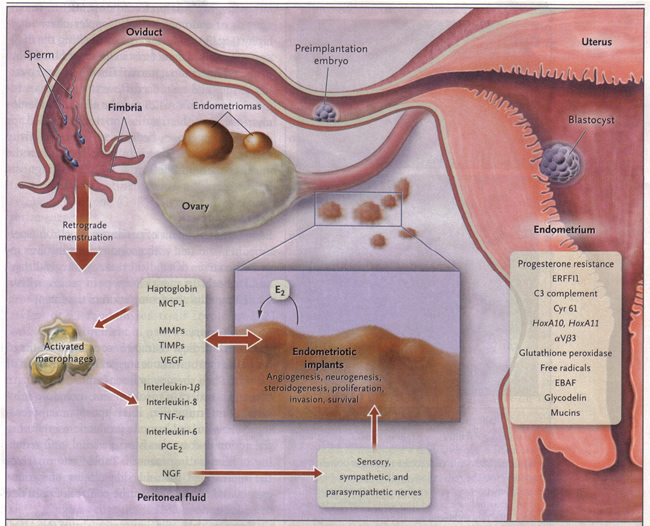
Рисунок 1. Патофизиология боли и бесплодие, связанных с эндометриозом
Механизм боли: Многие исследования отмечают наличие повышенного провоспалительных цитокинов и факторов роста при эндометриозе, которые тесно связаны с ощущением боли (например, фактор роста нервов, простагландинов, эстрадиол) (8) . Это может объяснить, почему минимальный эндометриоз может по-прежнему вызывают сильную боль. Имеющиеся данные показывают, что эндометриоз является hyperalgesic утверждают, что результаты обработки боли расширенная, что диктуется тем, как спинной мозг и головной мозг боли процесс с поражением и других сенсорной информации. Периферических нервных волокон поставки патологии эндометрия может внимания нейронов спинного мозга сегмента и в конечном итоге привести к центральной нервной чувствительности системы, что приводит к преувеличенным центральной нервной системы реагирования или призрачные эндометриоидных боль, или оба, несмотря на удаление поражений (9) . Это многомерная симптоматика эндометриоза гарантирует междисциплинарных стратегий управления.
Механизм Субфертильность: Расширенный случаев эндометриоз часто влечет за собой тяжелые заболевания клей, который может создать очевидные нарушения фертильности за счет снижения тубоовариальный подвижность, которая в конечном итоге препятствует пикап функции. Ли более легкие формы заболевания даже вызвать subferility не является бесспорным. Бесплодные женщины с минимальными мягкий эндометриоза была ниже сыворотки antimullerian уровни гормона на 3-й день, чем бесплодных пациенток с трубным препятствие (10) . В минимальный или умеренный эндометриоз, биологический механизм, вызывающий бесплодие остается неуловимым. Еще раз, расширение иммунный ответ может быть преступником по нарушая рождаемости в ранней стадии заболевания (11) . Враждебной перитонеальный окружающей среды может привести к нарушению функции сперматозоидов за счет увеличения повреждения ДНК спермы и ооцитов угрозу цитоскелета. Другая теория возлагает ответственность на дефект эндометрия на основе докладов снижение экспрессии в течение нескольких биомаркеров имплантации. К сожалению, эндометриоза связано с повышенным риском преждевременных родов, осложнений до родов и преэклампсии.
Диагностика и классификация
Клинические проявления эндометриоза являются переменными и непредсказуемый как проявления и течение. Дисменорея, хроническая тазовая боль, диспареуния, маточно-крестцовый узелков связок и придаточных массовой информации (либо симптомами или) относятся к числу хорошо известные проявления. Значительное число женщин, страдающих эндометриозом остается бессимптомным. Окончательный диагноз эндометриоза только может быть сделано по гистологии поражения удалена во время операции. Ни сывороточных маркеров, ни визуальных исследований удалось вытеснить диагностической лапароскопии для диагностики эндометриоза. Гистологический внешний вид состоит из желез эндометрия и стромы с разным количеством воспаление и фиброз (12) .
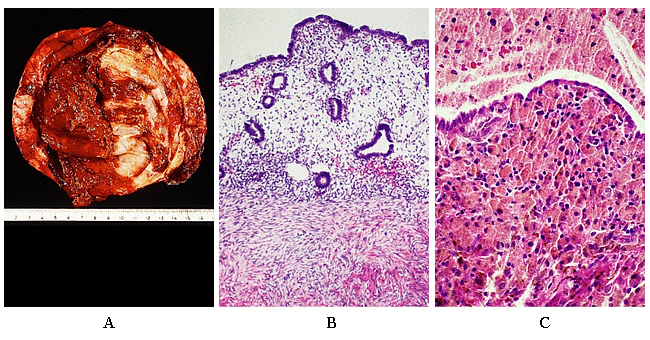
Рисунок 2. : Внутренняя поверхность кисты в яичниках при эндометриозе. Цвет, как правило, коричневого цвета. B: Эндометриоз яичников. В этой области ткани эндометрия воспроизводит внешний вид нормальный эндометрий, с точки зрения желез и стромы. C: Общий вид в результате повторяющихся кровоизлияния и накопление гемосидерина макрофаги.
Американского общества репродуктивной медицины, пересмотренная классификация эндометриоза
Многочисленные схемы классификации было предложено описать эндометриоз по анатомическим и тяжести заболевания. Американское общество репродуктивной медицины (ASRM) классификацию, которая является наиболее широко используемой системой, был пересмотрен в третий раз в 1996 году, но до сих пор ограничения (13). Система не является хорошим предиктором наступления беременности после лечения, несмотря на изменения в пункт оценки и сокращения точек для стадии заболевания. Система ASRM не коррелируют с симптомами боли и диспареуния и бесплодие. Значение ASRM пересмотрена система в форме записи оперативных результатов и, возможно, для сравнения результатов различных методов лечения.
| Peritoneum | Endometriosis | <1 cm | 1-3 cm | >3 cm |
|---|---|---|---|---|
| Superficial | 1 | 2 | 4 | |
| Deep | 2 | 4 | 6 | |
| Ovary | R-Superficial | 1 | 2 | 4 |
| Deep | 4 | 16 | 20 | |
| L-Superficial | 1 | 2 | 4 | |
| Posterior cul-de-sac obliteration |
Partial / Complete | |||
| 4 | 40 | |||
| Ovary | Adhesions | <1/3 Enclosure |
1/3-2/3 Enclosure |
>2/3 Enclosure |
| R-Filmy | 1 | 2 | 4 | |
| Dense | 4 | 8 | 16 | |
| L-Filmy | 1 | 2 | 4 | |
| Dense | 4 | 8 | 16 | |
| Tube | R-Filmy | 1 | 2 | 4 |
| Dense | 4* | 8* | 16 | |
| L-Filmy | 1 | 2 | 4 | |
| Dense | 4* | 8* | 16 |
*if the fimbriated end of the fallopian tube is completely enclosed, change the point assignment to 16. Denote appearance of superficial implant types as red [(R), red, red-pink, flame-like, vesicular blobs, clear vesicles], white [(W), opacifications, peritoneal defects, yellow-brown], or black [(B), black, hemosiderin deposits, blue]. Denote percent of total described as R_%, W_%, and B_%. Total should equal 100%.
- Stage I (minimal) – 1-5;
- Stage II (mild) – 6-15;
- Stage III (moderate) – 16-40;
- Stage IV (Severe) – >40
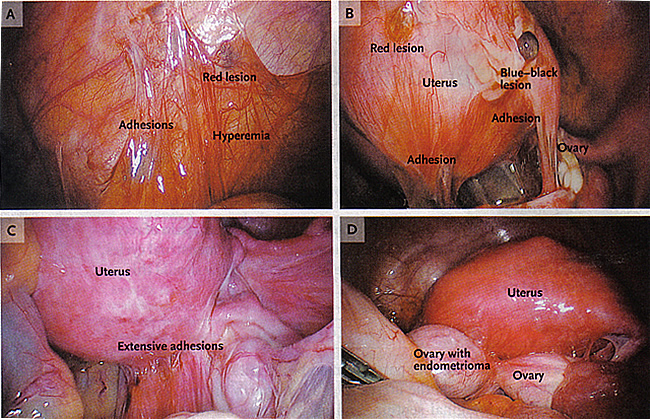
Рисунок 3. : Показывает эндометриоидных имплантатов (красные поражения), спайки, и гиперемия в брюшной полости. B: перитонеальный имплантатов, в том числе красный и сине-черный поражений и спаек. C: Обширные спаек искажающие нормальный тазовых анатомии. D: эндометриома приверженцем задней матки и растяжения капсулы яичника.
Управление Цели Эндометриоз
Эндометриоз имеет ряд уникальных биологических свойств. Он ведет себя как хроническое и рецидивирующее заболевание из-за микроскопических имплантатов, которые продолжают быть активными после хирургического лечения. Многие пациенты имеют покоя болезнь с редкими эпизодами боли, в то время как другие имеют частые, периодические боли. Эти различные модели симптом часто не связаны с поражением размера или степени заболевания. Современные подходы к управлению симптомом эндометриоза ориентированный, направленный в основном на лечении хронической боли в области таза и бесплодия. Протоколы управления также может быть направлено на замедление прогрессирования заболевания или предотвращения рецидива. Медицинские, хирургические или комбинированный подход может быть выбран. Кроме того, вспомогательных репродуктивных технологий (ВРТ) часто используются для лечения эндометриоза связанных бесплодия. Стратегии лечения женщин с эндометриозом варьироваться в зависимости от возраста пациента, цели лечения, четности степени заболевания, и статус менопаузы. Для молодых пациентов с легкой формой заболевания, не желая детей, желательно, чтобы использовать медицинскую подавления, чтобы контролировать симптомы и свести к минимуму хирургическое вмешательство. Для женщин с тяжелыми заболеваниями желающих плодородия, операции следует АРТ является разумным вариантом. Наконец, управление хирургическим менопаузы пациентов с симптомами эндометриоза требует иного подхода, в котором с использованием этикетки новых медицинских методов лечения, таких как ингибиторы ароматазы, могут быть рассмотрены.
Медицинское управление эндометриоза, боли, связанной с
Хроническая тазовая боль приходится 10% амбулаторных визитов гинекологический (14) . Полное медицинское, хирургическое, социальной и семейной истории должны быть получены от пациентов, которые представляют с этим симптомом, и они должны пройти медицинский осмотр, который включает в себя гинекологический осмотр. Фокусное боль и нежность на гинекологический осмотр связан с тазовой болезни у 97% больных с эндометриозом и у 66% пациентов (14) . Тазовой болью из-за эндометриоза, как правило, хроническое (в течение> 6 месяцев) и связано с дисменорея (в 50% до 90% случаев), диспареуния, глубокие тазовые боли, и боли внизу живота или без спина и поясница боль. Боль может возникать непредсказуемо и с перерывами в течение менструального цикла или оно может быть непрерывным, и это может быть тупая, пульсирующая или острые, и усугубляется физической активностью. Мочевого пузыря и кишечника, связанных симптомов (тошнота, вздутие живота, и раннее насыщение), как правило, циклический. Боль часто ухудшается с течением времени и может измениться характер, нередко женщины сообщают, жжение или повышенная чувствительность, симптомы, указывающие на нейропатической компонента. Симптомы совпадают с тем, ряд других условий гинекологических (например, воспаление тазовых органов, тазовые спайки, кисты яичников или массы, лейомиомы и аденомиоза) и не-гинекологической условий и факторов (например, синдром раздраженного кишечника, воспалительные заболевания кишечника, интерстициальный цистит, миофасциальные боли , депрессии и истории сексуального насилия), что делает диагностику сложной задачей. В настоящее время окончательный метод для диагностики и организовать эндометриоз и оценить рецидив заболевания после лечения визуализации в хирургии. Диагностическая лапароскопия широко используется для диагностики.
Длительное лечение пациентов с хронической тазовой боли, связанной с эндометриозом включает повторные курсы медикаментозной терапии, хирургическое лечение, или обоих. В большинстве случаев боль повторяется в пределах от 6 до 12 месяцев после завершения лечения. Консервативное хирургическое вмешательство связано с повторения боли. Таким образом, медикаментозное лечение обычно используется для облегчения симптомов этого хронического заболевания. Есть много рандомизированных плацебо-контролируемых исследований, показывающих превосходство этих препаратов по сравнению с плацебо (15) . Как и в хирургии, существует значительный "эффект плацебо" и повторения боли после прекращения препарата высока. Медицинские супрессивной терапии не влияет на рождаемость. Наиболее важные основные помнить, что медикаментозное лечение является эффективным, но, что симптомы, как правило, повторяются быстро после прекращения терапии. Таким образом, первой линии медикаментозной терапии должна быть направлена на препараты, которые могут быть использованы в долгосрочной перспективе (16).
Препараты, применяемые для лечения эндометриоза (16) :
| Class of Drugs | Drug | Dosage |
| Androgen | Danazol * | 100-400 mg orally twice a day 100 mg per vagina daily |
| Aromatase inhibitor | Anastrozole† Letrozole† |
1 mg orally daily 2.5 mg orally daily |
| Estrogen - progestin combinations | Monophasic Estrogen-progestin* |
Low ethinyl estradiol dose continuously |
| Gonadotropin - releasing hormone agonist (GnRH) | Goserelin*† Leuprolide depot*† Nafarelin*† |
3.6 mg SC monthly (10.8 mg IM every 3 mo) 3.75 mg IM monthly (11.25 mg IM every 3 mo) 200 mcg intranasally twice a day |
| Gonadotropin - releasing hormone agonist | Cetrorelix | 3 mg SC weekly |
| Progestin | Depo-subQ Provera 104* Dienogest‡ Etonogestrel-releasing implant Levonorgestrel-releasing IUS Medroxyprogesterone acetate Norethindrone acetate* |
104 mg/0.65 mL SC every 3 mo 2 mg daily 1 for 3 years 1 for 5 years 30 mg orally daily for 6 months, then 100 mg IM every 2 weeks for 2 months, then 200 IM monthly for 4 months 5 mg daily |
SC, subcutaneously; IM, intramuscularly; IUS, intrauterine system.
* FDA-approved for endometriosis.
†With add-back, i.e., norethindrone acetate 5 mg daily plus vitamin D 800 international units daily plus calcium 1.25 g daily.
‡Dienogest is a 19-nortestosterone derivative that is approved in the European Union for treatment of endometriosis. It is not available in the United States as a separate drug. It is available only in the oral contraceptive Natazia (Bayer HealthCare Pharmaceuticals; estradiol valerate/dienogest), which is a newer, four-phasic pack that contains dienogest.
Хирургическое лечение: хирургические подходы, чтобы уменьшить эндометриоз связанных боль может быть использован в качестве терапии первой линии или начаты после неудачной медикаментозной терапии (17) . Хирургические процедуры включают в себя удаление, бликование или лазерной абляции эндометрия имплантатов на брюшине, удаление или дренаж или удаление эндометриоза, резекция ректовагинальной узелки, лизис спаек, и прерывание нервных путей. Рандомизированные контролируемые испытания показали, что на 6 месяцев, лапароскопической аблации эндометрия имплантатов составляет 65% эффективность в снижении боли, по сравнению с 22% скорость уменьшения боли связаны с диагностической лапароскопии один (18) . Небольшое исследование по сравнению с лапароскопической аблации агонистами ГнРГ показал аналогичное снижение боли с этими двумя подходами (19) . Рецидив боли требует терапии часто (в 30% до 60% пациентов) в течение от 6 до 12 месяцев после лечения (19) . Альтернативной стратегией для управления эндометриоз связанных боли прерывание нервных путей. В то время как удаление сегмента маточно-крестцовый связки еще не доказали свою эффективность, рандомизированных контролируемых исследований показал превосходство лапароскопической аблации эндометрия ткани в сочетании с пресакральные и ретросакральные neurectomy (удаление нерва расслоение в пределах interiliac треугольник) по сравнению с лапароскопической аблации только в улучшении дисменорея и сокращения сильные боли средней линии (20) . Дело истории показали, что гистерэктомия с двусторонней удаление придатков матки при условии боли в 80% до 90% женщин с симптомами изнурительных которые поддаются медицинских или других хирургических вмешательств, боль, как сообщается, возвращаться в 10% женщин в течение от 1 до 2 лет после операции (21) . Послеоперационный гормональной должна включать в себя как эстроген и прогестаген, так эстрогена может стимулировать рост микроскопических болезни.
Добавочная Медикаментозная терапия: У женщин с поздней стадии заболевания (стадии III или IV), умеренной и тяжелой дисменореей, и нециклические тазовая боль, послеоперационная лекарственная терапия может улучшить боли, обеспечивая контроль периодически микроскопические или остаточной болезни. Мета-анализ шести рандомизированных исследований, которые сравнивали 3 до 6 месяцев послеоперационного лечения гонадотропин-рилизинг гормона агонистов (ГнРГ), даназол или комбинированные оральные контрацептивы, не послеоперационного лечения плацебо показало значительное снижение боли баллы при заключении терапии в лечении активных групп, хотя преимущества были несовместимы с более длительным периодом (до 18 месяцев) после прекращения терапии (22) . Средний интервал между операцией и требует повторения симптомов альтернативной терапии было значительно дольше пациентов, получавших послеоперационную лечения агонистами ГнРГ (> 24 месяцев), чем у пациентов, получавших плацебо (12 месяцев) (22) .
Управление Эндометриоз-Associated бесплодия
Несмотря на то причин эндометриоза связанных бесплодия или репродуктивной функции остаются неясными, одно можно сказать наверняка, к югу от женщин детородного возраста с эндометриозом на большую распространенность, 20% -50%, чем женщин репродуктивного возраста не стремятся лечения бесплодия (23) . В одном исследовании у женщин с бесплодием, частота распределения была на удивление надежной для минимальной до легких случаях на 68%, в то время как женщины с умеренной до тяжелой болезни составляют остальные 32% (24) . В настоящее время схема классификации не является полезным при прогнозировании скорости спонтанного беременности (16) . Ежемесячный плодовитость для тех, кто с эндометриозом 0,02-0,10 по сравнению с 0,15-0,20 в плодородной пары, хотя скорость не обязательно ниже, чем у пациентов с необъяснимыми репродуктивной функции (16) . Существует никаких доказательств связи с периодически потери беременности. Использование медикаментозной терапии в виде подавления яичников на стадии I или II эндометриоз не повышает плодовитость ставки и не должно быть предложено (25) . Дополнение лечения после оперативной лапароскопии на этапе III или IV эндометриоз с ГнРГ, кажется, не превосходит выжидательной тактики в отношении тарифов на природный концепция в течение 5-летнего периода наблюдения в рандомизированном контролируемом исследовании (26) .
Хирургическое лечение эндометриоза связанных бесплодия ведет к улучшению наступления беременности, но масштабы улучшения не ясна. Иссечение эндометриома является более эффективным, чем простой дренаж и удаление кисты. Поскольку большинство эндометриоза могут быть идентифицированы с помощью УЗИ, количество лапароскопия, необходимых для достижения результата то же самое. Важно все операции по удалению эндометриоза, что пациент будет проинформирован о том, что операция может привести к повреждению яичников и снижение овариального резерва (27) . Стоимость удаления глубоко проникают эндометриоз исключительно для улучшения беременности остается неясным и, возможно отрицательное воздействие рождаемости. После первых неудачных операции по поводу эндометриоза связанных бесплодия, экстракорпоральное оплодотворение (ЭКО) является лучшим вариантом, чем повторная операция, если боль все еще является важным вопросом. Повторные операции яичников было показано, что оказывает значительное негативное влияние на результаты ЭКО (27) . Гонадотропин терапия и внутриматочная инсеминация, а также ЭКО, являются эффективными лечения у женщин с бесплодием и эндометриозом (28) . В большом рандомизированном исследовании сравнение четырех стратегий лечения в 932 пар со стадией I или II или эндометриоз бесплодие неясного генеза, кумулятивный уровень беременности в течение четырех циклов лечения были следующими: интрацервикальное оплодотворения (10%), внутриматочная инсеминация (18%), гонадотропин терапии и интрацервикальное оплодотворения (19%) и гонадотропин терапия и внутриматочная инсеминация (33%) (16), (29). Удаление эндометриоидных поражений с лизис спаек рекомендуется для лечения бесплодия, связанные с I этап II или эндометриоз.
Основные направления от профессиональных обществ Диагностика и лечение эндометриоза связанных боли и бесплодие* (7), (21), (28):
| Condition | Recommendation |
| Pain† Diagnosis |
Surgery is preferred method for the diagnosis of pelvic pain and a pelvic mass (e.g. endometrioma), but it is not required before initiating empirical therapy, after consideration of other conditions in a differential diagnosis. There should be a low threshold for the evaluation of endometriosis in adolescents because the diagnosis is often missed in this age group. |
| Treatment | Initial treatment is a trial of non-steroidal anti-inflammatory drugs and hormonal therapy (combined oral contraceptives). All hormonal drugs that have been studied (combined oral contraceptives, progestins, GnRH agonists, and danazol) are similarly effective, but their side effects and costs differ. If a GnRH agonist is used, estrogen-progestin add-back therapy is recommended; GnRH agonists are not recommended for adolescents because of their effects on bone. The levonorgestrel intrauterine system is effective in selected patients. Laparoscopic uterosacral nerve ablation is not effective. |
| Infertility Diagnosis |
Both the male and female partner should undergo a full evaluation. |
| Treatment | Super-ovulation with intrauterine insemination provides benefit. Ovarian suppression is not effective in promoting spontaneous pregnancy. The use of GnRH agonist for 3-6 months before IVF and surgical ablation of endometriosis for stage I or II disease are beneficial. Excision of endometriomas >3cm in diameter is of benefit, although there is potential for diminished ovarian reserve. |
* Guidelines are from the American Society for Reproductive Medicine and the European Society of Human Reproduction and Embryology. GnRH denotes gonadotropin-releasing hormone; IVF denotes in-vitro fertilization.
†Data on the diagnosis and management of chronic pelvic pain and the treatment of adolescents with pelvic pain are from the American College of Obstetricians and Gynecologists.
Оплодотворения и эндометриоза
При лечении бесплодия связан с эндометриозом, поэтапный подход широко используется. Управление эндометриоза связанных бесплодия включает в себя комбинацию выжидательной тактики, хирургии, контролируемой стимуляции яичников (COS), внутриматочная инсеминация, и современные методы вспомогательной репродукции (АРТ). Использование COS или без внутриматочной инсеминации может быть полезным для короткого курса терапии у пациенток с эндометриозом с проходимости маточных труб. Если COS не приводит к беременности, ЭКО является разумным следующий шаг. Если начальные операции не может восстановить фертильность у пациентов с умеренной (стадия III) или тяжелой (стадия IV) эндометриозе связанных бесплодия, ЭКО является эффективной альтернативой. Репродукции для бессимптомных пациентов дает мало дополнительное преимущество, когда дело доходит до бесплодия (30) . Пациенты с эндометриозом, как представляется, снижение ответа яичников на гонадотропины и нуждаются в более высокой дозе гонадотропинов для проведения ЭКО (30). Остается неясным, является ли наличие или степень эндометриоза связано с нарушением качества яйцеклеток и оплодотворении и имплантации (31). Эффект при эндометриозе операция по итогам последующих циклах ЭКО были изучены, и регрессионного анализа показали, что интервал времени между операцией и ооцитов поиска не влияет на имплантацию ставки при эндометриозе пациентов ЭКО (32) .
Эндометриоз у подростков
Редкие случаи эндометриоза в premenarchal пациентов были описаны, но средний возраст, в презентации для эндометриоза составляет 15,9 лет (33) . Около 70% подростков с тазовой боли не реагирует на обычные медикаментозной терапии с эндометриозом (33) . В большинстве случаев у подростков может быть диагностирован на основании истории болезни и физического обследования. Симптомами эндометриоза, в результате предполагаемого диагноза включают постоянные циклические боли, дисменорея, нерегулярные менструации, и глубокая диспареуния. Боль, как правило, тяжелые, подрывных действий и вмешивается в школе, спортивных и других общественных мероприятий. Физическое обследование подростков с эндометриозом может варьировать от нормальной экспертизы обобщенные тазовых нежность или постоянного придатков массы. Классический вывод тазового эндометриоза является фиксированной загнутый матки рубцов и нежность кзади от матки. Характерной узелков в маточно-крестцовый связок и куль-де-мешок может быть пальпируется на ректовагинальной экспертизы в примерно одной трети женщин с болезнью. Яичников может быть увеличена и нежной, и часто крепится к широкой связки тазового или боковой стенки. Окончательный диагноз ставится лапароскопическим визуализации поражения эндометриоза. Подростки обычно имеют прозрачный, красный, белый и желто-коричневый поражения чаще, чем черные или синие поражений.
Медицинское управление: нестероидные противовоспалительные препараты (НПВП) и других анальгетиков может быть использован для уменьшения боли, связанной с эндометриозом. НПВП работать по ограничению производства простагландинов, которые производятся в избытке в эндометриоидных имплантатов. Они также работают нарушить механизм положительной обратной связи с участием местного производства простагландинов, который отвечает за дальнейшее повышение уровня эстрогена в внематочной клетки эндометрия (34) . В результате снижения выработки эстрогена, но и уменьшение воспалительной реакции. Оральные контрацептивы (ХОП) классически первой линии терапии у подростков из-за низких побочных эффектов и вторичные выгоды предотвращения нежелательной беременности. ХОП уменьшить эндометрия подкладка и тем самым уменьшить количество ткани, которая производит простагландины. ХОП необходимо назначать как непрерывного, циклического режима. Это позволит сократить число кровотечений вывод, что сводит к минимуму возникновение симптомов. Кроме того, ХОП может вызвать аменорею, в результате чего в последующем регресс симптомов. Лечение с ХОП является подавляющим, но не лечебные (35) .
Прогестерон агенты включают устные или медроксипрогестерона ацетата, оральный 19-нортестостерона производные, такие как ацетат норэтиндрон и норгестрел и levonorgesterol-рилизинг внутриматочной спирали. Эти агенты ограничить выработку эстрогена, причина децидуализацию внематочной ткани эндометрия, а впоследствии привести к атрофии эндометрия клетки. Даназол снижает объем эктопической ткани эндометрия, вызывая гиперандрогения государства. Несмотря на то, очень эффективны, андрогенные побочные эффекты являются значительными и необратимыми. Агонистами ГнРГ создать hypoestrogenic, гипогонадизмом окружающей среды и последующего вниз регулирование секреции гонадотропинов приводит к снижению выработки эстрогена. Побочные эффекты, которые ограничивают использование агонистов ГнРГ включают приливы, бессонница, снижение плотности костной ткани. Дополнения назад терапии норэтиндронацетат рекомендуется, чтобы избежать серьезных долгосрочных последствий (36) . Ароматазы посредником преобразования андростендиона в эстрон и тестостерона в эстрадиол (34), (37). Ингибиторы ароматазы блокируют местные эстроген производства тканей эндометрия, тем самым уничтожая координационного обратная связь для внематочной роста эндометрия. Несмотря на отсутствие рандомизированных контролируемых исследований, сравнивающих ингибиторы ароматазы с традиционной медикаментозной терапии эндометриоза, пилотные исследования с использованием ингибиторов ароматазы с дополнением назад прогестины или ХОП продемонстрировали значительное снижение эндометриоз связанных тазовой боли (37).
Хирургическое лечение: только консервативное лечение, в котором половые органы сохраняются указано в подростков. Хирургическое удаление видимых заболеваний может быть достигнуто путем иссечения, бликование и удаление методов. В зависимости от расположения, глубины инвазии и степени воспаления и рубцевания, универсальные методы применимы. Сохранение репродуктивного потенциала имеет первостепенное значение в подростковой популяции. Абляции эндометрия депозитов уменьшается боль, с или без удаления матки лапароскопическим нерва. Пресакральные и ретросакральные neurectomy, процедура, при которой симпатические нервы из матки делятся, может уменьшить среднюю линию боли в животе. Удаление внематочной клетки эндометрия могут также увеличить будущей фертильности у подростков, страдающих эндометриозом.
Эндометриоз затрагивающих без половых органов
Extrapelvic эндометриоз, как сообщается в различных сайтах, в том числе верхней части живота, диафрагмы, брюшной стенки (особенно пупка), промежности (эпизиотомия шрам), а грудная клетка (38) . Удаленные участки эндометриоза, как в легких, предплечье, бедро, позвоночник, и нос Сообщается также (39) . Возможно, это результат гематологических или лимфатическую трансплантации клеток эндометрия. На самом деле, 30% женщин с эндометриозом имеют заболевания тазовых лимфатических узлов (39) . Фактическое развитие эндометриоза вероятно, зависит от более чем один механизм происхождения. Кроме того, эндометриоз может вторгнуться на полную толщину прямой кишки, большого и малого кишечника, мочеточников и мочевого пузыря. Симптомы, связанные с эндометриозом на этих участках варьироваться в зависимости от местоположения и глубины проникновения и включать женщин с циклическим эпизодов макрогематурия, hemtochezia и кровохарканье. Несмотря на ряд терапевтических подходов были использованы для женщин с предполагаемым extrapelvic эндометриоз, сообщили эффективность подавления яичников с агонистом ГнРГ появляется поддержать его в качестве первой линии терапии, за исключением случаев обструкции мочеточника или кишечника, которые являются лучшими хирургическое лечение (38) . Даже в некоторых случаях ректовагинальной эндометриоз, подавляющее медикаментозная терапия может облегчить боль (40) . Опыт управления этих случаях ограничивается серии случаев, часто из одного центра.
Долгосрочные Последующие
Симптомы могут повторяться у женщин, даже после гистерэктомии и овариэктомии. Эндометриоз может повториться у 15% женщин, или не больные проходят курс терапии эстрогеном после двусторонней овариэктомии (38). Таким образом, гормональная терапия эстрогенами не противопоказано после радикальной операции по поводу эндометриоза. Хотя истинная частота рецидивов не известно, у пациентов с рецидивом симптомов проходит хирургическая процедура, патологии эндометрия может быть продемонстрировано. Наиболее распространенные места рецидивов является большой и тонкой кишки (38). Эти поражения, скорее всего, присутствующих на время операции и не вырезали. Эти поражения могут считаться стойкими заболеваниями, а рецидив заболевания. Сохранение заболевания hypoestrogenic государства, скорее всего, за счет местных выражение активность ароматазы. Лечение является трудным и часто требует хирургического вмешательства. Использование агонистов ГнРГ в этой ситуации hypoestrogenemia казалось бы, не на пользу. Ингибиторы ароматазы может быть рассмотрен, но не равномерно эффективным (41) .
В настоящее время имеются лишь ограниченные данные о сроках терапии эстрогеном после гистерэктомии с двусторонним удаление придатков матки при эндометриозе. Похоже, нет никаких преимуществ в плане рецидивов в задержке эстрогенов после операции (42) . Есть ограниченные данные показывают, что гормональная терапия может стимулировать рост остаточного яичника или ткани эндометрия после тотальной гистерэктомии и двусторонней удаление придатков матки при всех видимых заболеваний был удален (42) . Существует также обеспокоенность по поводу возможности эстроген-индуцированной злокачественной трансформации в остаточных имплантаты эндометриоза. Это привело некоторых медицинских работников рекомендовать процедуру добавления прогестина к терапии эстрогенами. Тем не менее, нет никаких результатов на основе доказательств в поддержку этой рекомендации. У женщин с хирургической менопаузой или спонтанное с интактной маткой, прогестин терапии не требуется, если эстроген вводят. Там, как представляется повышенный риск развития рака яичников при эндометриозе пациентов, хотя не ясно, по какой величины. Недавно он, как сообщается, имеют частоту соотношение 1,6 (95% доверительный интервал 1.12-2.09) (43) . Тем не менее, предшественников, таких как цитологическое или гистологическое атипии редки (44) .
Резюме
Многочисленные методы лечения доступны для лечения эндометриоза. Имеющиеся данные недостаточны, чтобы поддерживать превосходство одного над другим терапии. Это важно учитывать предпочтения пациента в лечении подход и предоставлять соответствующие консультации о рисках, побочных эффектов и стоимости, потому что эндометриоз является хроническим заболеванием, которое требует длительного лечения. Медицинские супрессивной терапии улучшает болевых симптомов, однако повторение ставки высоки после того, как лечение прекращается. Существует значительное краткосрочное улучшение боли после консервативного хирургического лечения, однако, как и медикаментозное лечение, есть также значительный уровень боли повторения. Ни медицинских, ни хирургическое лечение будет постоянно облегчать симптомы, связанные с эндометриозом. Комбинированная терапия с участием диагностические и лечебные лапароскопии с медицинским управлением, скорее всего, обеспечит наиболее оптимальные результаты. Различные отчеты показывают, частоты рецидивов от 16% до 52%. Эти различные ставки могут быть в результате переменная протоколы лечения, различные методы диагностики рецидивов и непоследовательной наблюдения. Регулярная оценка интервал рекомендуется обратиться хронический характер эндометриоза. В связи с хроническим характером заболевания и влияние на будущее рождаемости, психологическая поддержка чрезвычайно важна для этой популяции женщин. Хирургическое лечение эндометриоза связанных бесплодия ведет к улучшению наступления беременности, но масштабы улучшения не ясна. Иссечение эндометриома превосходит простой дренаж и удаление кисты. Когда облегчения боли от лечения агонистом ГнРГ поддерживает продолжение терапии, добавление дополнений назад терапия уменьшает или устраняет агонистом ГнРГ-индуцированного потеря костных минералов и обеспечивает облегчение симптомов без снижения эффективности обезболивания. Если медикаментозное лечение не удалось, проходит окончательное хирургическое лечение целесообразно в тех, кто не желает будущей фертильности.
Ссылки
- Giudice LC, Kao LC. Endometriosis. Lancet 2004;364:1789-1799
- Kennedy S, Bergqvist A, Charon C, et al. ESHRE Special Interest Group for Endometriosis and Endometrium Guideline Development Group. ESHRE guideline for the diagnosis and treatment of endometriosis. Hum Reprod 2005;20:2698-2704
- Balasch J, Creus M, Fabregues F, et al. Visible and non-visible endometriosis at laparoscopy in fertile and infertile women and in patients with chronic pelvic pain: a prospective study. Hum Reprod 1996;11:387-391. (Level II-3)
- Bedaiway MA, Falcone T, Mascha EJ, et al. Genetic polymorphism in the fibrinolytic system and endometriosis. Obstet Gynecol 2006;108:162-168. (Level II-2)
- Giudice LC, Swiersz LM, Burney RO. Endometriosis. In: Jameson JL, DeGroot LJ, eds. Endocrinology. 6th ed. New York: Elsevier, 2010:2356-2370
- Bulun SE. Endometriosis. N Engl J Med 2009;360:268-279
- Giudice LC. Endometriosis. N Eng J Med 2010;362(25):2389-2398
- Lebovic DI, Mueller MD, Taylor RN. Immunobiology of endometriosis. Fertil Steril 2001;75:1-10
- Stratton P, Berkley KJ. Chronic pelvic pain and endometriosis: translational evidence of the relationship and implications. Hum Reprod Update 2011;17:327-346
- Lemons NA, Arbo E, Scalco R, et al. Decreased anti-Mьllerian hormone and altered ovarian follicular cohort in infertile patients with mild/minimal endometriosis. Fertil Steril 2008;89:1064-1068
- Mansour G, Aziz N, Sharma R, et al. The impact of peritoneal fluid from healthy women and from women with endometriosis on sperm DNA and its relationship to the sperm deformity index. Fertil Steril 2009;92:61-67
- Walter AJ, Hentz JG, Magtibay PM, et al. Endometriosis: correlation between histologic and visual findings at laparoscopy. Am J Obstet Gynecol 2001;184:1407-1411; discussion 1411-1413. (Level II-3)
- Revised American Society for Reproductive Medicine classification of endometriosis: 1996. Fertil Steril 1997;67:817-821. (Level III)
- ACOG Practice Bulletin no. 51: chronic pelvic pain. Obstet Gynecol 2004;103:589-605
- Vercellini P, Crosignani P, Somigliana E, et al. “Waiting for Godot”: a commonsense approach to the medical treatment of endometriosis. Hum Reprod 2011;26:3-13
- Falcone T, Lebovic DI. Clinical management of endometriosis. Obstet Gynecol 2011;118:691-705
- Jacobson TZ, Duffy JM, Barlow D, et al. Laparoscopic surgery for pelvic pain associated with endometriosis. Cochrane Database Syst Rev 2009;4:CD001300
- Berkley KJ, Rapkin AJ, Papka RE. The pains of endometriosis. Science 2005;308:1587-1589
- Prentice A, Deary AJ, Goldbeck-Wood S, et al. Gonadotrophin-releasing hormone analogues for pain associated with endometriosis. Cochrane Database Syst Rev 2000;2:CD000346
- Proctor ML, Latthe PM, Farquhar CM, et al. Surgical interruption of pelvic nerve pathways for primary and secondary dysmenorrhea. Cochrane Database Syst Rev 2005;4:CD001896
- Idem. Treatment of pelvic pain associated with endometriosis. Fertil Steril 2008;90:Suppl:S260-S269
- Yap C, Funress S, Farquhar C. Pre- and post-operative medical therapy for endometriosis surgery. Cochrane Database Syst Rev 2004;3:CD003678
- Ozkan S, Murk W, Arici A. Endometriosis and infertility: epidemiology and evidence-based treatment. Ann N Y Acad Sci 2008;1127:92-100
- D’Hooghe TM, Debrock S, Hill JA, Meuleman C. Endometriosis and subfertility: is the relationship resolved? Semin Reprod Med 2003;21:243-254
- Hughes E, Brown J, Collins JJ, et al. Ovulation suppression for endometriosis. Cochrane Database Syst Rev 2007;3:CD000155
- Loverro G, Carriero C, Rossi AC, et al. A randomized study comparing triptorelin or expectant management following conservative laparoscopic surgery for symptomatic stage II-IV endometriosis. Euro J Obstet Gynecol Biol 2008;136:194-198
- Busacca M, Vignali M. Endometrioma excision and ovarian reserve: a dangerous relation. J Minim Invasive Gynecol 2009;16:142-148. (Level III)
- Practice Committee of the American Society for Reproductive Medicine. Endometriosis and infertility. Fertil Steril 2006;86:Suppl:S156-S160
- Barnhart K, Dunsmoor-Su R, Coutifaris C. Effect of endometriosis on in vitro fertilization. Fertil Steril 2002;77:1148-1155
- Mahutte NG, Arici A. Endometriosis and assisted reproductive technologies: are outcomes affected? Curr Opin Obstet Gynecol 2001;13:275-279
- Bedaiwy M, Shahin AY, AbulHassan AM, et al. Differential expression of follicular fluid cytokines: relationship to subsequent pregnancy in IVF cycles. Reprod Biomed Online 2007;15:321-325
- Bedaiwy MA, Falcone T, Katz E, et al. Association between time from endometriosis surgery and outcome of in vitro fertilization cycles. J Reprod Med 2008;53:161-165
- Laufer MR, Sanfilippo J, Rose G. Adolescent endometriosis: diagnosis and treatment approaches. J Pediatr Adolesc Gynecol 2003;163(3 Suppl):S3-S11
- Hartel Z. Dysmenorrhea in adolescents and young adults: etiology and management. J Pediatr Adolesc Gynecol 2006;19(6):363-371
- Doyle JO, Missmer SA, Laufer MR. The effect of combined surgical-medical intervention on the progression of endometriosis in an adolescent and young adult population. J Pediatr Adolesc Gynecol 2009;22(4):257-263
- Vercellini P, Fedele L, Pietropaolo G, et al. Progestogens for endometriosis: forward to the past. Hum Reprod Update 2003(9(4):387-396
- ACOG. ACOG Committee Opinion: Aromatase inhibitors in gynecologic practice. Obstet Gynecol 2008;112(2 Part 1):405-407
- ACOG Practice Bulletin. Management of endometriosis. Number 114, July 2010. Obstet Gynecol 2010;116:223-236
- Laufer MR. Current approaches to optimizing the treatment of endometriosis in adolescents. Gynecol Obstet Invest 2008;66 (Suppl 1):19-27
- Vercellini P, Somigliana E, Vigano P, et al. Surgery for endometriosis-associated infertility: a pragmatic approach. Hum Reprod 2009;24:254-269. (Level III)
- Bohrer J, Chen CC, Falcone T. Persistent bilateral ureteral obstruction secondary to endometriosis despite treatment with an aromatase inhibitor. Fertil Steril 2008;90:2004.e7,2004.e9. (Level III)
- Matorras R, Elorriaga MA, Pijoan JI, et al. Recurrence of endometriosis in women with bilateral adnexectomy (with or without total hysterectomy) who received hormone replacement therapy. Fertil Steril 2002;77:303-308. (Level I)
- Aris A. Endometriosis-associated ovarian cancer: a ten year cohort study of women living in the Estric Region of Quebec, Canada. J Ovarian Res 2010;3:2
- Bedaiwy MA, Hussein MR, Bicotti C, Falcone T. Pelvic endometriosis is rarely associated with ovarian borderline tumors, cytologic and architectural atypia: a clnicopathologic study. Pathol Oncol Res 2009;15:81-88
Опубликован: 26 June 2012
Dedicated to Women's and Children's Well-being and Health Care Worldwide
www.womenshealthsection.com


