Профилактике рака шейки матки: Управление низкосортных неоплазии шейки матки
WHEC практики Бюллетень и клинических управления Руководство для медицинских работников. Образования гранта, предоставленного здоровья женщин-образовательный центр (WHEC).
Рак шейки матки является наиболее распространенной формой рака у женщин, и вызванных вирусом папилломы человека (ВПЧ). Большинство сексуально активных женщин будет приобретать ВПЧ в течение жизни. Хотя пройдет инфекция в большинстве случаев он сохраняется в некоторых женщин. Долгосрочное сохранение ВПЧ - особенно с высоким риском типов - был создан в качестве необходимой причиной предраковых поражений. программы скрининга были очень успешными в Соединенных Штатах, Европе и других регионах, имеют возможность для достижения широкого и устойчивого покрытия. Профилактике рака шейки матки может теперь стать еще лучше. Существенные изменения практики предстоящих, мотивированные четкого понимания ВПЧ естественной истории и цервикального канцерогенеза. На основании центральную роль стойких инфекций шейки канцерогенными генотипы ВПЧ в цервикальном канцерогенезе, ДНК ВПЧ тестирование было введено в скрининга рака шейки матки. В 1999 году, продуктами и лекарствами США (FDA) одобрила первый канцерогенных или высокого риска ВПЧ ДНК-тест для сортировки в двусмысленное шейки цитологии и в 2003 году для cotesting женщин 30 лет и старше (Hybrid Capture 2; Qiagen корпорации, Gaithersburg, MD ). Американское онкологическое общество (ACS) в 2002 году и семинар в соавторстве с Национальных Институтов Здоровья (NIH)-Национальный институт рака (NCI), Американское общество кольпоскопии и патологии шейки матки (ASCCP), и АСУ в 2004 году опубликовал руководящие принципы для добавочной ВПЧ шейки цитологии (cotesting) для скрининга рака шейки матки среди женщин в возрасте 30 лет и старше в Соединенных Штатах. Последние данные показали, что риск злокачественных и предраковых заболеваний шейки и ВПЧ-инфекции значительно меняется с возрастом. Основы профилактики рака шейки матки не сильно изменилась в последние 50 лет. Передовые технологии, но без изменения базовой стратегии и производительности. Шейки программы скрининга рака были очень успешными, потому что рак шейки матки обычно развивается медленно, в течение десятилетий. Повторные раундов скрининга поймать предраковых поражений, как они растут, в то время как они могут быть легко лечится.
Целью данного документа является обсуждение отношений ВПЧ обнаружения и ненормальные цитологии с гистологических диагнозов шейки предраковых заболеваний и рака. Основное внимание в этой дискуссии по управлению атипичные клетки плоского эпителия подорвали значение (ASCUS) и низкой степени плоскоклеточной интраэпителиальной поражений (LSIL). Эта серия по профилактике рака шейки матки, будет также служить в качестве основы для понимания будущих последствий вакцинации против ВПЧ на шейном результаты скрининга рака. Будущее профилактике рака шейки матки, вероятно, будет более эффективным, поскольку оно будет включать в себя: профилактической вакцинации подростков против ВПЧ-инфекции канцерогенных; повышение роли ВПЧ; улучшения в кольпоскопия для повышения чувствительности, а также сокращение числа жизни экраны необходимы для профилактики.
Используемые сокращения:
Аденокарцинома на месте - АИС
Американское общество рака - ACS
Американского колледжа акушеров и гинекологов - оптическим
Американское общество по кольпоскопии и патологии шейки матки - ASCCP
Атипичная железистых клеток - AGC
Атипичные клетки плоского эпителия - ASC
Атипичные клетки плоского эпителия подорвали значение - ASCUS
Атипичные клетки плоского эпителия, не может исключить HSIL - ASC-H
Цервикальной интраэпителиальной неоплазии (легкой или класс 1) - CIN1
Цервикальной интраэпителиальной неоплазии (умеренная или класса 2) - CIN2
Цервикальной интраэпителиальной неоплазии (тяжелой или класса 3) - CIN3
Флуоресценция в гибридизация - FISH
Большой Иссечение Петля зоны трансформации - LLETZ
Низкий сорт плоскоклеточного эпителия поражения - LSIL
Высококачественный плоскоклеточного эпителия поражения - HSIL
Вирус папилломы человека - ВПЧ
Фон
В 2007 году более 13000 женщин был диагностирован рак шейки матки в Соединенных Штатах. Использование Папаниколау (Pap) мазка было начислено помогает предотвратить рак шейки смертности от рака и снизить уровень заболеваемости раком шейки более чем на 70% (1) . Тем не менее, в Соединенных Штатах, низкосортные плоскоклеточный интраэпителиальных поражений (LSIL), первый шаг к дисплазии шейки матки, ежегодно диагностирована у около одного миллиона женщин. Инфекция с высокой степенью риска штамма HPV считается самым важным фактором в инициации канцерогенеза шейки. Следовательно, ВПЧ скрининг получило широкое распространение и является важной частью стратификации риска и клинические руководства управления. Ключ к разработке эффективных руководящих принципов для управления шейки матки является отличить истинную шейки предшественника рака шейки матки доброкачественная с небольшим предраковые потенциал. Оба LSIL и CIN1 отражают цитологических и патологических эффектов заражения ВПЧ. Большинство из этих поражений не будет прогресса к раку. Однако, как много как 28% женщин с цитологическим гавани LSIL ЦИН 2 или ЦИН 3, примерно две трети из которых определяется по кольпоскопии (2) . С клинической точки зрения, важно различать, какой интраэпителиальной опухолевых поражений будет прогрессировать до инвазивного рака, если не лечить. Однако, диагностические категории в настоящее время имеют лишь скромные прогностическую ценность, и это значение уменьшается поражения становятся менее серьезными. Вероятность прогрессирования рака выше, и времени до прогрессирования короче, как степень дисплазии увеличивается.
ВПЧ и рака шейки цитологии
Высокая распространенность ВПЧ, особенно среди молодых женщин, не приводит к шейки болезни в большинстве случаев. Неуклонно снижается, с высокой степенью риска HPV распространенности через увеличение возраста согласуется с другими исследованиями в США и других развитых странах, где программы цервикального скрининга являются общими (1) . Вполне вероятно, что иммунная система очищает вирус ВПЧ в течение долгого времени, и что развитие неоплазии шейки матки у некоторых людей могут относиться к выходу из строя иммунной системы или других генетических или экологических факторов, характерных для этих лиц. Выводы, что темпы развития рака шейки матки отличаются между расами может, так как авторы наблюдали (1) , связаны с различиями в естественной истории инфекции между расами или различия в диагностике и лечения. Во всяком случае, вирус ВПЧ, как представляется, участвующих в развитии неоплазии шейки матки, и, надеюсь, программы иммунизации в настоящее время место для молодых женщин снизит этот риск.
По данным Американского онкологического общества (ACS), по оценкам, насчитывалось 9710 новых случаев рака шейки матки и 3700 случаев смерти от рака шейки матки в Соединенных Штатах в 2006 году (2) . Основной причиной рака шейки матки является ВПЧ, передающегося половым путем инфекция, которая изменяется в распространенности в зависимости от возраста и числа сексуальных партнеров. Распространенность является наиболее высокой среди сексуально активных молодых женщин, которые подвергаются воздействию в первый раз, и сужается после возраста 50 лет. Женщины в возрасте до 24 лет, как правило, в состоянии очистить ВПЧ без осложнений, но это становится все менее вероятно, с увеличением возраста обнаружения. Мазок из шейки матки является очень эффективным скрининг-тест на рак шейки матки и предраковых поражений, которые были использованы с середины 20-го века, задолго до того, ссылка на ВПЧ была обнаружена. До недавнего времени это был единственный скрининг-тест для дисплазии шейки матки. В феврале 2003 года в США продуктов питания и медикаментов одобрило и ДНК ВПЧ тест, который может быть использован с цервикальной цитологии для выявления женщин с повышенным риском рака шейки матки и предраковых поражений. Более 100 подтипов ВПЧ в настоящее время не выявлено, и более 40 из этих подтипов может быть найдена в шейке матки или влагалища. Тестирование ДНК ВПЧ техники обнаруживает несколько подтипов, которые находятся в рак шейки матки. На основании имеющихся доказательств, Национальный институт рака, Американского общества по кольпоскопии и патологии шейки матки, и САУ, что женщины в возрасте от 30 лет и старше могут пройти обследование с использованием как шейки матки и ВПЧ тест ДНК одновременно. Женщин, для которых оба теста окажутся отрицательными, есть риск цервикальной интраэпителиальной неоплазии 2 или 3, что составляет примерно 1 из 1000 (3) . Поэтому рекомендуется, чтобы они повторно отобранных не чаще, чем раз в 3 года. Женщинам с отрицательным цитологии, но положительного высокого риска ВПЧ должны иметь как испытания повторяются через 6-12 месяцев. Те, с аномальными цитологии или постоянного высокого риска ВПЧ должны пройти кольпоскопию. Для женщин в возрасте до 30 лет, распространенность ВПЧ является очень высокой, хотя риск рака шейки матки является очень низким, что скрининг на ВПЧ у всех женщин в возрасте до 30 лет может привести к ненужным дополнительных испытаний, таких как кольпоскопия или повторить шейки матки, с Несколько выводов значение. Текущая рекомендация для выполнения шейки матки вирусом папилломы рефлекс тестирование на ВПЧ только мазок из шейки матки, который показывает атипичные клетки плоского эпителия подорвали значение (ASCUS) (4) .
В хорошо организованной шейки программы скрининга на рак, ВПЧ тест является более чувствительной, чем обычные цитологии для выявления CIN 3 поражения и рак (5) . В этой большой, рандомизированного исследования из Финляндии, ВПЧ тест функционировала эффективно, как основного экрана для рака шейки матки и более чувствительны, чем обычные цитологии для обнаружения цервикальной интраэпителиальной неоплазии класса 3 (ЦИН 3) или выше. Самых сильных сторон этого исследования 1:1 с рандомизации чуть более 58000 женщин и способностью связывать участников исследования к результатам, за 5-летний период, используя всеобъемлющие финской базы данных населения и рак реестра. Одно из опасений, что врачи, возможно, является ли выводы применимы к населению США, что в настоящее время редко экранированный с использованием обычных цитологии (жидкость-цитология является нормой). Эта обеспокоенность должна быть развеяны больших мета-анализа, что не было выявлено различий в чувствительности жидких-цитология по сравнению с обычными тестирование Пап (6) . Несмотря на большой размер, исследование было ограниченным статистической мощности, чтобы показать влияние этих двух условий скрининга на скорость развития рака шейки матки, в первую очередь потому, что скорость настолько мала, в экранированных населения. Чтобы определить, что воздействие, скрининг варианты должны быть повторены для очередного раунда, с последующей продлен до 10 лет.
Клиническое применение ВПЧ
Cotesting является стандартным: США руководящих принципов с ACS (2002) и оптическим (2003, 2009) предлагают врачам возможность скрининга женщин 30 лет и старше с использованием как цитологии и ВПЧ - подход, известный как "cotesting". Однако, хотя около 90% женщин, которые имеют отрицательный ответ на оба теста можете спокойно отказаться от дальнейшего скрининга в течение 3 лет, многие врачи экране их более часто с cotesting, снижение экономической эффективности этого варианта (7) . Мы рекомендуем: что вы следуете нынешние руководящие принципы США и экран женщин 30 лет и старше, как и ВПЧ Пап-тесты и расширить интервал скрининга до 3 лет для женщин, которые имеют отрицательные результаты на обоих тестах. Многочисленные исследования подтверждают вывод, что подавляющее ВПЧ в первичных скрининга рака шейки матки значительно увеличивается выявления ЦИН 3 или выше, а также уменьшать риск последующих женщины развития рака шейки матки.
Есть два основных критерия для принятия решения о ВПЧ основе сортировки является клинически полезным. Во-первых, делает сортировку тест (ВПЧ) определить значительная доля женщин, которые нуждаются или не нужно направление к дорогим кольпоскопия и биопсия процедур, которые оправдывают расходы на сортировку тест? То есть, если ВПЧ почти всегда отрицательный или положительный, мало значения в ее использовании. В качестве примера последнего тестирования руку ВПЧ для женщин, направленных в ASCUS-LSIL Сортировка исследование (АЗЦ) с цитологии LSIL было прекращено до завершения, потому что большинство испытания ВПЧ положительных (8) . Вторым критерием является ли ВПЧ-отрицательных женщин может быть безопасно следует, а не направлены на кольпоскопию. По этим критериям, ВПЧ сортировки женщин 45 лет и старше или 50 лет и старше с LSIL может быть рациональной из-за более низкий процент тех, ВПЧ положительные (менее 80%) находятся на очень низком риске CIN3 и рака среди ВПЧ- отрицательных женщин. Это наблюдается в больших клинических испытаний в Европе (9) . Расхождение между наблюдениями и ALTS является то, что ALTS поступил преимущественно молодых женщин (средний возраст 24 лет) (8) . ВПЧ может быть полезно для сортировки для кольпоскопические направление на LSIL цитологии у пожилых женщин, но не для ASC-H цитологии в любом возрасте (11) .
ВПЧ результаты тестов для женщин с цитологии АРУ не может быть полезным для сортировки, но может служить руководством для врачей в котором анатомические сайте, шейки матки или эндометрия, проблема может существовать: женщины с цитологии AGC которые ВПЧ тест положительный имеют исключительное высокие риски шейки предраковых заболеваний и рака а те, кто ВПЧ тест отрицательный имеют высокий риск развития рака эндометрия (10) .
ВПЧ будет становиться все более важно различать женщин на высокие и низкие риски шейки предраковых заболеваний и рака среди ВПЧ-вакцинации женщин с двусмысленным и слегка ненормальный цитологии. В HPV16/18-vaccinated населения, это исследование (11) наблюдается меньше интерпретации HSIL цитологии и меньше заболеваний, связанных с любой неправильный результат цитологического потому HPV16 преимущественно причин HSIL цитологии и ВПЧ 16 и 18 два самых канцерогенных генотипов ВПЧ. Частичная защита от вакцин против Следующим наиболее канцерогенным генотипов ВПЧ, особенно HPV31 и HPV45, могут еще больше уменьшить появление цитологии HSIL. Таким образом, будет глубокий сдвиг в сторону двусмысленные цитологии в ВПЧ-вакцинации населения.
Молекулярные маркеры дисплазии шейки матки
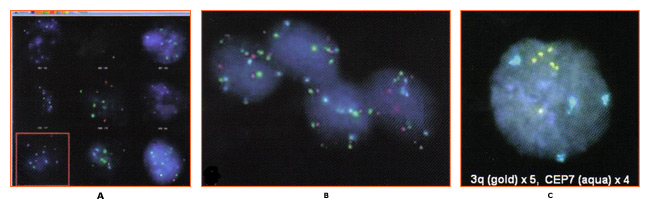
Научно-исследовательские разработки в молекулярном патогенезе рака шейки матки были направлены на развитие молекулярных маркеров для использования в скрининга рака шейки матки. В частности, усиление руку 3q хромосома была продемонстрирована в шейки матки и также наблюдается в других опухолей (12) . Сравнительный геномной гибридизации (CGH) с использованием архивных образцов показали, что амплификации ДНК на хромосоме 3 (регион 3q24 на 3q28) была связана с раком шейки канцерогенеза. Впоследствии было установлено, что датчик ориентации последовательностей для компонента РНК человеческого гена теломеразы (TERC), расположенного на хромосоме 3q26 регионе, могут быть использованы как скрининг-тест для 3q усиления и может помочь в оценке прогрессирования отдельные поражения (13) . Высказано предположение, что из-за высокого процента диспластических поражений имеют дополнительные копии гена TERC, TERC/3q, возможно, причинные, еще не доказано роль, в дисплазии с помощью теломеразы-ячейкой на основе увековечение. Кроме того, другие гены локализованы в 3q26 региона, таких как PIK3CA, который кодирует каталитическую субъединицу фосфатидилинозитол 3-киназы и связано с рядом связанных с раком функций, включая апоптоз и клеточный рост, есть потенциал, чтобы быть привлечены как рак шейки матки онкогенов.
Исследования в области изучения ассоциации 3q усиления с шейки канцерогенеза смещается к исследованию возможности того, что 3q усиления может предсказать шейки прогрессирования заболевания. Это исследование (14) показали, что в то время как 3q получить предсказал прогрессии в 100% случаев (CIN1 / 2 прогрессирующих к CIN3); отсутствие 3q получить также был в состоянии предсказать, 70% регрессора. Другие исследования показали, что биомаркеров, таких как 3q (3q26) являются временно, связанных с ВПЧ интеграции в геном хозяина (12) . Таким образом, тест, который определяет статус 3q должны быть использованы в сортировке LSIL пациентов. До недавнего времени, рутинное тестирование на 3q получить не представляется возможным, поскольку оценки требуется анализ большого числа (800) окрашенных, плоскоклеточный ядра клетки, которая является непрактичным обычной микроскопии. Однако, онко FISH ® шейки тест качественный флуоресценции в гибридизация (FISH) тест для определения приобретение конкретных хромосомных aneuploidies (в пределах 3q26 область) в цитологических образцов.
онко FISH проводится на шейно-влагалищный цитологии образцы, идентичные тем, которые используются для Пап и ВПЧ. Тест оценивает усиление 3q26 региона путем использования двух рыб зондов, один для 3q26 локус контроля и зонда. Перечисление и сравнение 3q26 и контроля зондов, в связи с ядерной морфологии, результат в 3 квартале количество копий для каждого из ядер проанализированы. Хотя некоторые факторы способствуют прогрессированию предраковые поражения на злокачественные опухоли, 3q26 усиления маркер, что медицинский работник может использовать в сочетании с другими тестами, чтобы помочь пациенту LSIL управления.
nОпределение взаимосвязи между выигрыш в хромосоме 3q26 региона и развития дисплазии шейки матки привело в ряде исследований, подтверждающих ассоциации и предлагая возможные клинические полезность, что наблюдение. Однако, применяя FISH-анализа на основе жидких образцов цитологии за 3 квартал прибыль в клинических условиях является сложной задачей. Скрининг все клетки, присутствующие в образце для их FISH сигналов нецелесообразно с использованием традиционных микроскопии анализа. Автоматизированные характер анализа позволяет комплексный подход к анализу образцов, что не представляется возможным вручную. Анализ образцов LSIL определяет до 20% образцов, которые показывают уровень 3q усиления выше, что наблюдается в нормальных образцов (29) . Полностью автоматизированный метод определения 3q получить в жидком цитологии может быть анализа, необходимые для осуществления регулярного тестирования (29) . Дополнительные исследования для подтверждения полезности этой технологии не требуется. Дальнейшие исследования с использованием этого теста основан на наличие клеток с более пяти 3q26 FISH сигналы, позволит лучше оценить его клинической эффективности и ее потенциальную полезность, в сочетании с существующими испытаний, для улучшения управления пациента.
Обнаружение 3q получить в архивных образцов LSIL
n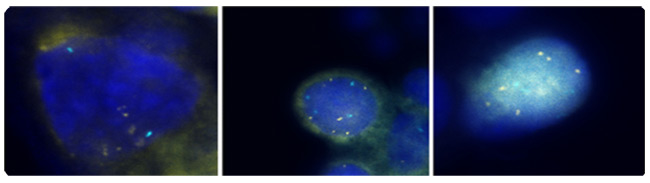
Рисунок 2: 3 квартал флуоресценции в гибридизация (FISH) сигналов цветного золота и контроля центромерным 7 FISH сигналы цветных Aqua. Все 3 клетки выставку более 4 3q (золото), рыба сигналов. Фотографии любезно Ikonisys инк
Клиническое применение онко FISH шейки испытаний
онко FISH шейки предоставляет врачам с дополнительной информацией, которая может помочь им в принятии более обоснованных клинических управленческих решений. Какие LSIL будет прогресса в клинике для более высокого класса? Какой будет регресс к нормальным? Приблизительно 10% пациентов с диагнозом LSIL будет прогрессировать к HSIL, 60% будет регресс к нормальной жизни, а 30% останется LSIL (15) . онко FISH шейки помогает врачам оценить, какие LSIL пациенты могут регрессировать и предложить LSIL случаях повышенного риска для болезни прогрессии. Среди многих хромосомные изменения, наблюдаемые при раке шейки матки, наиболее последовательным аномалия обнаружена в 3 квартале хромосомы руку. Исследования показали, что по крайней мере 90% инвазивных случаев рака шейки матки у выигрыш в 3 квартале руку (14) . Дополнительные исследования показали взаимосвязь между выигрыш в 3q26 число копий, как тяжести и стадии заболевания шейки прогресса (13)(14). Используя эту технологию, чтобы посмотреть на прогрессии отдельных пациентов, было показано, что чувствительность 3q26 локусов для прогнозирования перехода от CIN1/CIN2 к CIN3 составил 100% и специфичность, т. е. предсказание регрессии 70% (14) . онко FISH шейки предоставляет информацию для клинической оценки дисплазии до кольпоскопия.
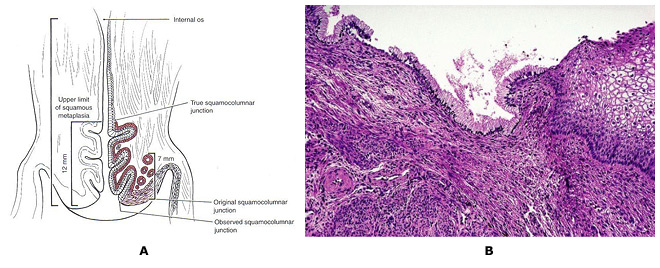
nШейки зоны трансформации (TZ)
Канцерогенные ВПЧ-инфекции особенно подвержены вызывать рак на преобразование зон (TZS), где два вида эпителия встречаются, например, шейки матки, анус и ротоглотки (16) . Преобразование зоны (TZ) определяется как область, лежащую между оригинальным перехода squamocolumnar и кольпоскопические новых перехода squamocolumnar. Оригинальный линейного сопряжения между плоскоклеточный и цилиндрического эпителия заменяется зоны плоскоклеточного метаплазии в той или иной степени созревания. В верхней или краниально края этой зоны резкое разграничение между эпителия, который появляется морфологически плоскоклеточный использования увеличенных освещения кольпоскоп, и эритематозная, ворсинок эпителия, который появляется colposcopically столбчатых. Это кольпоскопические перехода называется новый перехода squamocolumnar. Начальной клинической оценки для большинства женщин в пост-пубертатный лет. Пожилая плоскоклеточный метапластические эпителия часто заменяется дистальных или каудально предел цилиндрического эпителия. Оригинальный перехода squamocolumnar чаще всего проявляется клинически как squamocolumnar перехода разделяющая оригинальное плоскоклеточный и метапластические эпителия. Как зоны трансформации созревает, это соединение становится невозможно очертить. Только наличие nabothian фолликулы и железы отверстия намеки на оригинальные происхождения столбчатых зрелого плоскоклеточный метаплазии. Неоплазии шейки матки почти всегда происходит в TZ. Понимание плоскоклеточной метаплазии является ключом к пониманию понятия шейки TZ и цервикального канцерогенеза. Если новые соединения squamocolumnar видно в полном объеме в отсутствие предраковые заболевания, заболеваемость плоскоклеточным болезни выше или краниально к новой перехода squamocolumnar фактически равно нулю. Таким образом, если новый узел squamocolumnar видно во всей ее полноте, кольпоскопии шейки матки характеризуется как удовлетворительное. Если новые соединения squamocolumnar не видел его целиком, кольпоскопии описывается как неудовлетворительное. Зоны трансформации далее определяет дистальный предел полноценного железистой интраэпителиальной неоплазии, предшественник поражения с инвазивными аденокарцинома шейки матки.
nХотя ВПЧ-инфекции очень распространены в половых таких сайтах, как влагалища, пениса и вульвы, темпы ВПЧ-индуцированного рака значительно ниже из-за отсутствия TZS. Плоскоклеточный метаплазии продолжается на протяжении всей жизни женщины, и в конечном итоге, TZ расположен во внутренней ОС. Следовательно, она имеет решающее значение для образца TZ в скрининге, но выборки с центром в ОС не всегда собирают оптимального клеток. Атрофия может уменьшить ячейки дает также. Существует надежда, что ВПЧ в том числе канала шейки матки клеток может уменьшить ложно-отрицательных экранирования по сравнению с цитологии. Однако, в зависимости от метода скрининга используется, диагностических проблема остается, даже когда надлежащим образом выполняться, colposcopists не может легко диагностировать поражения на плохо видимых TZ у женщин в постменопаузе.
n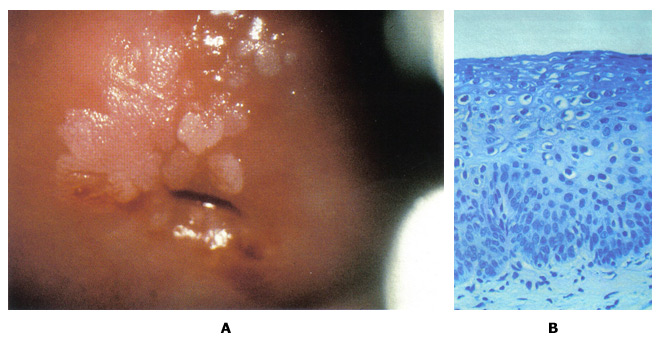
Рисунок 5: А. кольпоскопические фотографию шейки матки после применения уксусной кислоты демонстрации многочисленных поражений acetowhite в соответствии с низкой степени плоскоклеточной интраэпителиальной поражения (LSIL). В. Гистологические данные показывают, потеря полярности в нижней трети эпителия и многочисленные koilocytes, в соответствии с цервикальной интраэпителиальной неоплазии, 1-й степени, с особенностями ВПЧ.
Цитологии и гистологии выводы и интерпретации
В Bethesda 2001 руководящих принципов, ASC является subcategorized в атипичные клетки плоского эпителия неопределенного значительное (ASCUS) и атипичные клетки плоского эпителия, не может исключить HSIL (ASC-H). Разница в принципы управления для этих двух выводов цитологии относится к их неотъемлемого риска для CIN2, 3. ASCUS является наиболее распространенной аномалией шейки цитологии, на которые приходится 4,4% всех Пап результаты испытаний. Хотя риск заболевания раком для любого конкретного пациента очень низкая (0,1 +0,02%) (19) , и риск CIN2, 3 + и низкая (6.4-11.9%) (22) , поскольку Есть так много людей с этим цитологии ненормальность, это представление цитологии результате около половины женщин с CIN2, 3 +. Первым шагом в оценке женщин с ASCUS заключается в сортировке тех, кто при более высоком риске для более интенсивного оценки (кольпоскопия) и направляющей тест для более рутинных последующей деятельности. Сортировка может быть проведена проверка на одного теста с высокой степенью риска (онкогенные) типов ВПЧ или повторить цитологическое обследование через 6 месяцев и 12 месяцев. Когда цитологии тест индекс образца получается жидкость-цитология или когда образец ВПЧ совместно собраны, "Рефлекс" ВПЧ является предпочтительным подходом (17) . Данные ALTS показали, что две повторить цитологическое обследование через 6 месяцев и 12 месяцев на пороге ASCUS обнаружено 88% CIN2, 3 +, обращаясь 63,6% женщин кольпоскопия. ВПЧ только обнаружены 92,2% CIN2, 3 +, обращаясь 55% женщин кольпоскопия.
Управление нормальной шейки цитологии с ВПЧ положительный результат теста:
Лучший подход к управлению на ВПЧ-положительных, цитологии-отрицательных женщин 30 лет и старше является повторение цитологического и ВПЧ на 12 месяцев (17) . Женщины, чьи ВПЧ результат по-прежнему положительно на повторное тестирование через 12 месяцев или чьи цитологии результат ASC или больше должны пройти кольпоскопию, в то время как женщины, чьи результаты отрицательны на обоих тестов может отложить скрининга в течение 3 лет. Включение ВПЧ в рутинный скрининг должны быть зарезервированы для женщин в возрасте 30 лет и старше (22) . В скрининговых исследований из Северной Америки и Европы, чувствительность, используя сочетание ВПЧ и цитологию значительно выше, чем, что либо тест наедине с отрицательная прогностическая значений 99-100% (22) . Женщины, которые получают отрицательный результат от обоих начальных цитологии и ВПЧ имеют менее 1 в 1.000 риск наличия CIN2 или больше, и потенциальных последующих исследований в Европе и США показали, что риск развития CIN3 в течение 10 -летний период составляет менее 2% (22)(23) . Моделирование исследования показывают, что у женщин 30 лет и старше, скрининг на 3-летние интервалы, используя сочетание тестирования цитологии и ВПЧ обеспечивает преимущества равноценный или более высокий, чем те, которые предусмотрены ежегодный скрининг с обычными цитологии. Даже в женщин 30 лет и старше, большинство ВПЧ-позитивных женщин стать ВПЧ-отрицательных в течение последующих (60% в проспективном исследовании) (22) . В хорошо экранированных населения, риск CIN2 + в ВПЧ-положительных, цитологии-отрицательных женщин диапазоне от 2,4% до 5,1% (23) .
Управление шейки цитологии ASCUS и LSIL у подростков (в возрасте до 21 лет):
Инвазивным раком шейки матки встречается очень редко в девушек-подростков в возрасте до 21 лет. Института рака ГЭЭ программы Национального сообщил, что с 1995 по 1999 год заболеваемость инвазивным раком шейки матки была 0 за 100.000 в год для женщин в возрасте 10-19 лет и 1,7 на 100000 в год для женщин в возрасте 20-24 лет (1) . Поскольку скорость ДНК ВПЧ инфекции или положительности является самым высоким в подростков, и потому, что большинство ВПЧ-инфекции у подростков с или без резкого цитологии будет решить без лечения, действующими руководящими принципами не рекомендуется использование ВПЧ в этой группе населения при любых обстоятельствах , в том числе сортировка ASCUS и последующей деятельности в LSIL (17)(18). ASCCP 2006 консенсуса руководящие принципы для управления ASCUS и LSIL у подростков (20 лет и младше) рекомендую повторить цитологии в 12-месячным интервалом в течение 2 лет. Если ASCUS или LSIL сохраняться в течение 2 лет, врачи советуют выполнять кольпоскопия (17) . Эта рекомендация представляет значительные изменения от предыдущих принципов и основана на природных исследования истории ASCUS и LSIL, которые демонстрируют высокий уровень разрешения заболевания в течение 2-3 лет (18) . Очень похоже клинический исход молодых женщин с ASCUS и LSIL побудило ASCCP рекомендовать аналогичный подход к управлению обе эти диагнозы. Предполагая, что CIN2 или больше была исключена по кольпоскопии, перспективных исследований взрослого населения с CIN1 показывают, что риск CIN2 или более развивающихся протяжении периода 2 примерно на 10% (19) . В подростков, скорости развития значительно ниже, оценивается в 3%, тогда как скорость разрешение CIN1 чрезвычайно высока (более 90%) (18)(19) . Таким образом, начальная управления CIN1 без терапии является обязательным.
Особые соображения: несовершеннолетние проходят кольпоскопии, возможно, будет полезно иметь родительского участия в процедуре. Однако, кольпоскопические экзаменов рассматриваются оценки, передающихся половым путем заболеваний (ЗППП), и несовершеннолетних, как правило, разрешается согласия для диагностики для диагностики и лечения ЗППП. По этой причине родительского согласия, хотя предпочтительнее, не требуется. Если родительское согласие не получено, согласия на обследование должно быть получено от незначительных и указано в медицинской карте. Любой поставщик здравоохранения, который поставляет такой помощи должны быть полностью информированы о своих государственных законов и установленных местным стандартам медицинской помощи.
Управление шейки матки ASCUS цитологии и LSIL во время беременности:
Беременность в подростковом возрасте не изменяет отбора и управления аномальных цитологии. Endocervical кюретаж и иссечение процедуры не должны быть выполнены во время беременности, если инвазивного рака очень подозреваемых (20) . Скрининг на беременность, следовательно, должны быть выполнены до оценки и управления аномальных шейки цитологии у подростков. Во время беременности, только диагноз, который может изменить управление инвазивного рака. Наличие рака может измениться целей лечения или изменение маршрута и сроков доставки. Таким образом, кольпоскопия обследование во время беременности должно иметь своей основной целью исключения инвазивного рака. Управление LSIL и ВПЧ-положительных ASCUS результаты во время беременности должны быть такими же, как в небеременных государства, хотя оценки этих условий может быть отложен до его доставки.
Управление шейки цитологии ASCUS и LSIL с ВПЧ-положительных (пациентов 21 лет и старше):
Хотя цитологии результате LSIL, как полагают, отражают цитопатических последствия ВПЧ-инфекции, а не истинный предраковые поражения, женщины с LSIL остаются на умеренный риск за CIN2 +. В ALTS, 27,6% женщин с LSIL были обнаружены CIN2 + либо на colposcopically направлены биопсии или на внимательного наблюдения в течение следующих 2 лет (19) . Этот показатель практически не отличается от скорости CIN2 + в женщин, которые представлены с ВПЧ-положительных результатов в ASCUS же населения (26,7%).
Многие исследования показали, что распространенность как ДНК ВПЧ и положительности CIN2, 3 уменьшается с возрастом у женщин с LSIL (19) . Ну-экранированный, женщин в постменопаузе с ранее отрицательные результаты также с низким риском инвазивного рака шейки матки. Это говорит о том, что женщин в постменопаузе с LSIL может управляться с помощью ДНК ВПЧ для сортировки в тот же протокол, который используется в женщин репродуктивного возраста с ASCUS. Наличие ASCUS реже у женщин в постменопаузе, как риск значительных результатов патологического. ВПЧ ставки ДНК положительности также резко сократиться, как возраст женщины. Это означает, что ВПЧ ежегодно более эффективно у пожилых женщин, поскольку оно относится низкая распространенность CIN2, 3 значительно выше среди женщин с ASC-H, чем женщины с ASCUS, так ASC-H должна рассматриваться представляют двусмысленные HSIL.
Последующие после кольпоскопические оценки ASCUS, ASC-H, или LSIL, не CIN2, 3: В ALTS, начальная кольпоскопия определили только 58% от CIN2 + поражений. Для женщин не установлено, что CIN2 + на начальном кольпоскопия, скорость CIN2 + в течение последующих (примерно 10-13%) не изменялась на выводы на кольпоскопию (отрицательные выводы не стоит биопсии, отрицательные биопсии или CIN1 биопсия). ALTS оценивали различные пост-кольпоскопия последующих стратегий и обнаружили, что ВПЧ проводится через 12 месяцев после начальной кольпоскопия и цитологическое обследование два повтора осуществляется на 6-месячным интервалом одинаково эффективны (19) . Из-за дополнительных расходов и отсутствие повышенной чувствительности, стратегии комбинированных цитологии плюс ВПЧ не рекомендуется. В отсутствие ЦИН определены гистологически, диагностические иссечение или абляционного процедуры являются неприемлемыми для начального лечения пациентов с LSIL. Последующие меры либо с ВПЧ на 12 месяцев или шейки цитологии на 6 месяцев и 12 месяцев (ASCUS порога) является приемлемым. Если тест ДНК ВПЧ результат отрицательный или если две последовательные результаты цитологии повторить тест отрицательный, вернуться в рутинный скрининг рекомендуется. Если какой-либо тест на ДНК ВПЧ, результат положительный, или если результат повторить цитологии сообщается как ASCUS или выше, рекомендуется кольпоскопия (24) .
Управление шейки цитологии ASC-H:
Распространенность CIN2, 3 значительно выше среди женщин с ASC-H, чем женщины с ASCUS, так ASC-H должна рассматриваться представляют двусмысленные HSIL. Женщины с нетипичной плоскоклеточный рак, не может исключить HSIL (ASC-H) имеют 20-50% риск наличия CIN2, 3 поражения и должны быть оценены с немедленной кольпоскопии. Большинство женщин с ASC-Н ДНК ВПЧ положительный (от 67-84%) (21) , так что промежуточные сортировки неуместно и ВПЧ не рекомендуется. Если CIN2, 3 не выявленных кольпоскопия, женщины в возрасте от 21 лет и старше должны быть проверены в аналогии с ВПЧ-позитивных женщин с ASCUS.
Управление CIN1 Предшественник HSIL и АРУ, а не иным конкретным (NOS):
Либо диагностических эксцизионной процедуры или наблюдение с кольпоскопия и цитология на 6-месячным интервалом в течение 1 года является приемлемым для женщин 21 лет и старше с гистологической диагностики CIN1 предшествовать HSIL или AGC-NOS цитологии результате, если в последнем случае, что кольпоскопия экспертизы является удовлетворительным и канала шейки матки выборки является отрицательным. Диагностические эксцизионной процедура рекомендуется для женщин с CIN1 предшествовать HSIL или результаты AGC-NOS цитологии в которых кольпоскопия экспертизы является неудовлетворительным, кроме беременности. Риск незамеченными CIN2, 3 или аденокарцинома на месте (АИС) поражения, как ожидается, будет больше у женщин с CIN1 предшествовать HSIL или AGC цитологии результат, чем у женщин с CIN1 предшествовать ASC или LSIL цитологии результат. Цервикальной интраэпителиальной неоплазии класса 2,3 определяется в 84-97% женщин с HSIL цитологии результатов оценивается с большим вырезания петли зоны трансформации (LLETZ) (26) . Таким образом, отдельные рекомендации для ЦИН предшествовать HSIL или AGC цитологии.
Интеграция вакцинации против ВПЧ и скрининга:
В мире ограниченных ресурсов здравоохранения, Вакцинация против ВПЧ и скрининга конкурируют за внимание и ресурсы. Как показал крупных рандомизированных исследований, два лицензированных вакцин против ВПЧ являются весьма эффективными в предотвращении новых случаев инфицирования ВПЧ 16 и 18 (25) . Там могут быть некоторые возможные перекрестные защиты от ВПЧ 31 и HPV45. Меньшинство рака в связи с другими типами ВПЧ, не распространяется. Современные вакцины не относятся к существующей инфекции или повреждения (25) . Они должны быть предоставлены до воздействия; в программы общественного здравоохранения это означает, что вакцинация молодых девочек-подростков является оптимальным. Это не поддерживаемые объединить вакцинации против ВПЧ и скрининга без интеграции. Доказано продолжительность эффективности профилактических вакцин против ВПЧ 16 и ВПЧ-18 в настоящее время приближается десятилетие и охвата вакцинацией растет. Таким образом, вакцинация подростков будет в значительной степени предотвратить первый шаг в цервикальном канцерогенезе (острые инфекции ВПЧ в годы после начала полового акта); особенно в новых вакцин при окончательной оценки охватывают более типов ВПЧ. Эффективность всех шейки скрининг-тестов будет уменьшаться в связи с сокращением распространенности до рака (27) . Вакцинация особенно снизит эффективность цитологии-скрининг, поскольку повреждения, которые остаются в большей мере будет неприятность двойники (особенно ASCUS) не по вине канцерогенные типы HPV, а не на риск прогрессирования рака (28) . Таким образом, различные предложения находятся на рассмотрении, в том числе задержки первоначальный отбор у вакцинированных молодых женщин и переключатель акцента с цитологии к начальному ВПЧ.
Резюме рекомендаций:
Следующие рекомендации основаны на хороших и последовательных научных данных и мнения экспертов по клиническому ведению пациентов с патологической цитологии шейки (15)(17) :
- У подростков (в возрасте до 21 лет) с ASCUS или результаты LSIL цитологии, или CIN1 результатов гистологии предшествовать ASCUS или LSIL или AGC-не иначе конкретных (NOS) результаты цитологии, следить за рекомендуется на 12-месячным интервалом. При первом контрольном визите (через 12 месяцев), только подростков с HSIL или больше на повторять цитологии следует отнести к кольпоскопия. На 24-месячного наблюдения, тех, с ASCUS большей результат должен быть передан кольпоскопия. ДНК ВПЧ тестирования является неприемлемым для подростков. Если ВПЧ непреднамеренно выполнены, положительного результата не должны влиять на управление.
- Женщин 21 лет и старше ни с атипичной канала шейки матки, рак эндометрия, или железистых клеток Н.У.К., которые не имеют CIN или железистой неоплазии определены гистологически должны получать повторить цитологии тестирования в сочетании с тестирования ДНК ВПЧ в течение 6 месяцев, если они являются ДНК ВПЧ положительных и в 12 месяцев, если они ДНК ВПЧ отрицательный. Направление в кольпоскопия рекомендуется для женщин, которые впоследствии положительный результат теста на высокой степенью риска ДНК ВПЧ или которые были уличены в ASCUS или больше на их повторных испытаний цитологии. Если оба теста отрицательные, женщины могут вернуться в обычное тестирование цитологии.
- Рекомендовал ведения беременных с гистологии диагноз CIN1 является последующей без лечения. Лечение беременных женщин на CIN1 является неприемлемым.
- Женщин 21 лет и старше с ASCUS которые отрицательный результат на ВПЧ, или чьи ВПЧ статус неизвестен и который тест отрицательный нарушения использованием кольпоскопии, должны иметь тест повторить цитологии в 1 год. Женщины с ASCUS, которые тест повторить цитологии в 1 год. Женщины с ASCUS, которые два отрицательных результата на повторе цитологии на 6-месячным интервалом может вернуться в рутинный скрининг.
- Пременопаузе женщин 21 лет и старше с ASCUS результаты цитологии могут подвергаться немедленной кольпоскопии или могут подвергаться сортировке тестирование, чтобы определить, какие из них следует отнести к кольпоскопия. Сортировка может быть проведена проверка на один тест на один тест с высокой степенью риска (онкогенные) типов ВПЧ или повторить цитологическое обследование через 6 месяцев и 12 месяцев. Когда индекс образца цитологии испытаний был получен жидкий основе цитологического или при ВПЧ образца был одним из собранных, "Рефлекс" ВПЧ является предпочтительным подходом.
- Кольпоскопия рекомендуется в пременопаузе женщин 21 лет и старше с ASCUS который ВПЧ положительных, тех, с двумя последовательными ASCUS результаты цитологии или с LSIL, или женщины любого возраста с ASC-H.
- У небеременных женщин с ASC и LSIL цитологии результаты, которые проходят кольпоскопия, канала шейки матки выборки с использованием щетки или кюретки является предпочтительным для женщин, у которых нет поражений были выявлены и те с неудовлетворительными результатами кольпоскопии. Endocervical выборки является приемлемым для женщин с удовлетворительной кольпоскопии результаты и поражения, определенных в зоны трансформации. Endocervical оценки либо с кольпоскопию или путем отбора проб рекомендуется для всех небеременных женщин с результатами HSIL цитологии. Endocervical кюретаж неприемлемо у беременных женщин.
- В женщина 21 лет и старше с CIN1, которое сохраняется в течение не менее 2 лет, при продолжении последующих мер или лечения является приемлемым. Если лечение выбрано и кольпоскопия результат удовлетворительным, либо иссечение или абляция является приемлемым. Если лечение выбрано кольпоскопия экспертизы является неудовлетворительным, канала шейки матки кюретаж (ECC) положительно, или женщина была ранее получавших лечение, удаление рекомендуется и абляционного процедуры являются неприемлемыми.
- Для пременопаузе женщин 21 лет и старше с ВПЧ-положительных ASCUS, или ASC-H или LSIL цитологии результате в которых CIN2, 3 не определены, последующая деятельность без лечения рекомендуется использовать либо повторить шейки испытаний цитологии на 6 месяцев и 12 месяцев или ВПЧ тест на 12 месяцев-интервалов; повторить кольпоскопию показан для цитологического результате ASCUS или более высокого класса или аномалия положительные высокого риска ВПЧ результат теста. После двух последовательных отрицательных результатов цитологического или один отрицательный результат ВПЧ женщин могут вернуться в рутинный скрининг.
- Вакцинация против ВПЧ для женщин в возрасте 9-26 лет. В настоящее время никаких изменений в скрининге или управления аномальных шейки цитологии рекомендуется, если подросток был вакцинирован.
- 3q26 усиления может помочь выявить женщин с LSIL, которые не нуждаются кольпоскопия (30) .
Резюме
Профилактике рака шейки матки может теперь стать еще лучше. Существенные изменения практики предстоящих, мотивированные четкого понимания ВПЧ естественной истории и цервикального канцерогенеза. Большинство шейки программ в 2010 году по-прежнему полагаться на шейки цитологии последующим диагнозом скрининг-выявленных нарушений использования кольпоскопические биопсии. Комбинированные чувствительность тестирования цитологии и ВПЧ очень похож на ВПЧ в одиночку. Это означает, что ВПЧ может в конечном итоге быть использованы в качестве одного первичного анализа скрининг следует цитологии или новый тест биомаркеров, как сортировка, которые будут использоваться только для ВПЧ-позитивных женщин. Обнаружение 3q усиления и усиления TERC в плановом порядке мазка Папаниколау может помочь в выявлении низкой степени поражения с высоким риском прогрессии и в уменьшении ложно-отрицательных цитологического скрининга. Важнейшей задачей является переосмыслить наши нынешние модели профилактики на основе частых цитологии и кольпоскопические направления. Неизбежно, будущие программы будет зависеть от вакцинации, гораздо реже скрининга и лечения меньше разрешить оформление разрешения ВПЧ-инфекции.
Подтверждение: Здоровье женщин и образовательный центр (WHEC) благодаря д-р Роберт Дж. Walat, клиническая лаборатория директор Ikonisys Инк Нью-Хейвен, штат Коннектикут (США) за очень ценные предложения, мнения экспертов и помощь в серии о профилактике рака шейки матки.
Ресурсы
- World Health Organization
Colposcopy and Treatment of Cervical Intraepithelial Neoplasia: A Beginners' Manual - National Cancer Institute
The Pap Test: Questions and Answers
Финансирование: серии по профилактике рака шейки матки была профинансирована WHEC Инициативы по глобальному здравоохранению. Эта программа осуществляется с партнерами женского здоровья и образовательный центр (WHEC) для ликвидации / сокращения рака шейки матки во всем мире. Связаться с нами, если вы хотите внести свой вклад и / или объединить усилия.
Список литературы:
- Datta SD, Koutsky LA, Ratelle S, et al. Human papillomavirus infection and cervical cytology in women screened in the United States, 200-2005. Ann Intern Med 2008;148:493-500
- American Cancer Society. Cancer prevention and early detection, facts and figures 2006. Atlanta (GA): American Cancer Society; 2006
- ACOG Practice Bulletin. Human papillomavirus, No. 61. Obstet Gynecol 2005;105:905-918
- Wright TC, Massad LS, Dunton CJ, et al. 2006 Consensus Guidelines for the Management of Women with Abnormal Cervical Cancer Screening Tests. 2006 American Society for Colposcopy and Cervical Pathology-sponsored Consensus Conference. Am J Obstet Gynecol 2007;197:346-355
- Anttila A, Kotaniemi-Talonen L, Leinonen M, et al. Rate of cervical cancer, severe intraepithelial neoplasia, and adenocarcinoma in situ in primary HPV DNA screening with cytology triage: randomized study within organized screening program. BMJ 2010;340:1804-1811
- Arbyn M, Bergeron C, Klinkhamer P, et al. Liquid compared with conventional cervical cytology: a systematic review and meta-analysis. Obstet Gynecol 2008;111:167-177
- Saraiya M, Berkowitz Z, Yabroff KR, et al. Cervical cancer screening with both human papillomavirus and Papanicoalaou testing vs. Papanicoalaou testing alone: what screening intervals are physicians recommending? Arch Inter Med 2010;170:977-985
- Human papillomavirus testing for triage of women with cytologic evidence of low-grade squamous intraepithelial lesions: baseline data from a randomized trial. The Atypical Squamous Cell of Undermined Significance/Low-Grade Squamous Intraepithelial Lesions Triage Study (ALTS Group. J Natl Cancer Inst 2000;92:397-402
- Ronco G, Cuzick J, Segnan N, et al. HPV triage of low-grade (LSIL) cytology is appropriate for women over 35 in mass cervical cancer screening using liquid based cytology. Eur J Cancer 2007;43:476-480
- Castle PE, Fetterman B, Poitras N, et al. Relationship of atypical glandular cell cytology, age, and human papillomavirus detection to cervical and endometrial cancer risks. Obstet Gynecol 2010;115:243-248
- Castle PE, Fetterman B, Cox JT, et al. The age-specific relationship of abnormal cytology and human papillomavirus DNA results to the risk of cervical precancer and cancer. Obstet Gynecol 2010;116:76-84
- Rao PH, Arias-Pulido H, Lu XY, et al. Chromosomal amplifications, 3q gain and deletions of 2q33-q37 are the frequent changes in cervical carcinoma. BMC Cancer 2004;4 (www.biomedcentral.com/1471-2407/4/5 )
- Heselmeyer-Haddad K, Janz V, Castle PE, et al. Detection of genomic amplification of the human telomerase gene (TERC) in cytologic specimens as a genetic test for the diagnosis of cervical dysplasia. Am J Pathol 2003;163:1405-1416
- Heselmeyer-Haddad K, Sommerfeld K, White N, et al. Genomic amplification of the human telomerase gene (TERC) in pap smears predicts the development of cervical cancer. Am J Pathol 2005;166:1229-1238
- American Society for Colposcopy and Cervical Pathology (ASCP) Practice Recommendations. Available from http://www.asccp.org/edu/practice/cervix/premalignant/epidemiology.shtml Accessed 10 August 2010
- Schiffman M, Castle PE, Jeronimo J, et al. Human papillomavirus and cervical cancer. Lancet 2007;370:890-907
- American Society for Colposcopy and Cervical Pathology. Management of women with atypical squamous cells of undetermined significance (ASCUS). Hagerstown (MD): ASCCP; 2007. Available at: http://www.asccp.org/pdfs/consensus/algorithms_cyto_07.pdf Accessed 2 August 2010
- Moscicki AB, Shiboski S, Hills NK, et al. Regression of low-grade squamous intraepithelial lesions in young women. Lancet 2004;364:1678-1683
- Guido R, Schiffman M, Solomon D, et al. Post-colposcopy management strategies for women referred with low-grade squamous intraepithelial lesions or human papillomavirus DNA-positive atypical squamous cells of undermined significance: a two-year prospective study. ASCUS LSIL Triage Study (ALTS) Group. Am J Obstet Gynecol 2003;188:1401-1405
- Wright TC Jr, Massad LS, Dunton CJ, et al. 2006 Consensus Guidelines for the Management of Women with Abnormal Cervical Screening Tests. 2006 ASCCP-Sponsored Consensus Conference. J Low Genit Tract Dis 2007;11:201-222
- Sherman ME, Castle PE, Solomon D. Cervical cytology of atypical squamous cells-cannot exclude high-grade squamous intraepithelial lesion (ASC-H): characteristics and histologic outcomes. Cancer 2006;108:298-305. (Level I)
- Wright TC Jr, Schiffman M, Solomon D, et al. Interim guidance for the use of human papillomavirus DNA testing as an adjunct to cervical cytology for screening. Obstet Gynecol 2004;103:304-309. (Level III)
- Kjaer S, Hogdall E, Frederiksen K, et al. The absolute risk of cervical abnormalities in high-risk human papillomavirus-positive, cytologically normal women over a 10-year period. Cancer Res 2006;66:10630-10636. (Level II-2)
- ACOG Practice Bulletin. Management of abnormal cervical cytology and histology. Number 99; December 2008
- Paavonen J, Naud P, Salmeron J, et al. Efficacy of human papillomavirus (HPV)-16-18 AS04-adjuvanted vaccine against cervical infection and precancer caused by oncogenic HPV types (PATRICIA): final analysis of a double-blind, randomized study in young women. Lancet 2009;374:301-314
- Alvarez RD, Wright TC. Effective cervical neoplasia detection with a novel optical detection system: a randomized trial. Optical Detection Group. Gynecol Oncol 2007;104:281-289. (Level I)
- Fanco EL. Cuzick J, Hildesheim A, et al. Issues in planning cervical cancer screening in the era of HPV vaccination. Vaccine 2006;24 Suppl 3:S171-177
- Shiffman M, Wentzensen N. From human papillomavirus to cervical cancer. Obstet Gynecol 2010;116:177-185
- Seppo A, Jalali GR, Kilpatrick MW, et al. Gain of 3q26: A genetic marker in low-grade squamous intraepithelial lesions (LSIL) of the uterine cervix. Gyncol Oncol 2009;114:80-83
- Jalali GR, Herzog TJ, Dziura B, Walat RJ, et al. Amplification of the chromosome 3q26 region shows high negative predictive value for nonmalignant transformation of LSIL cytologic finding. Am J Obstet Gynecol 2010;202:1.e1-e5
Опубликован: 5 November 2010
Dedicated to Women's and Children's Well-being and Health Care Worldwide
www.womenshealthsection.com